Тема 3.3. Розчини електролітів. Електролітична дисоціація
План
- Положення теорії електролітичної дисоціації.
- Ступінь дисоціації. Константа дисоціації.**
3. Особливості розчинів сильних електролітів.***
1. Електроліти – речовини, водні розчини або розплави яких проводять електричний струм. Приклади: розчини молей, кислот і лугів
ТЕД (Арреніус):
1) дисоціація електролітів відбувається під дією полярних молекул розчинника
2) Дисоціюючи молекули розпадаються на катіони та аніони.
3) Дисоціація – оборотний процес.
4) Дисоціація багатоосновних кислот і багатокислотних основ відбувається ступінчасто.
Приклад: HCl ↔ H+ + Cl-
2. Лише частина електроліту дисоціює в розчині на йони і тому Арреніус ввів поняття ступеня дисоціації.
Ступінь дисоціації – відношення числа молекул електроліту, що розпалися в розчині на йони, до загального числа його молекул в розчині.
α = n / N,
де α – ступінь дисоціації;
n – кількість молекул, які про дисоціювали;
N – загальна кількість молекул
До рівноваги, яка встановлюється в розчині слабкого електроліту між молекулами та йонами, можна застосувати закони хімічної рівноваги і записати вираз константи рівноваги.
Наприклад, для дисоціації оцтової кислоти
СН3СООН ↔ Н+ + СН3СОО-
константа рівноваги має вигляд:
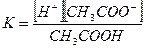
Константа рівноваги, що відповідає дисоціації слабкого електроліту, називається константою дисоціації.
Величина К залежить від природи електроліту і розчинника, а також від температури, але не залежить від концентрації розчину.
При ступінчатій дисоціації речовин дальший ступінь характеризується меншим розпадом, ніж попередній.
Якщо концентрацію електроліту, що розпадається на 2 йони, позначити через С, а ступінь його дисоціації у розчині через α, то концентрація кожного з йонів буде С α, а концентрація недисоційованих молекул С(1- α). Тоді рівняння константи дисоціації матиме вигляд:
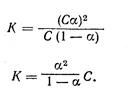
Це рівняння виражає закон розбавлення Оствальда.
Для розчинів, в яких дисоціація електроліту дуже мала, рівняння закону Оствальда спрощується. Оскільки в таких випадках α≤1, то величиною α у знаменнику правої частини рівняння можна знехтувати. Рівняння буде мати вигляд:
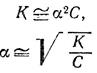
Це рівняння наочно показує зв'язок, що існує між концентрацією слабкого електроліту і ступенем дисоціації: ступінь дисоціації зростає при розбавлянні розчину.
3. Для оцінки стану йонів у розчині сильних електролітів користуються величиною, яка називається активністю.
Під активністю йона розуміють ту ефективну, умовну концентрацію його, відповідно до якої він діє під час хімічних реакцій. Активність йона а дорівнює його концентрації С, помноженій на коефіцієнт активності f:
α = fC
В розведених розчинах коефіцієнт активності йона в даному розчиннику залежить тільки від заряду іона та іонної сили розчину I, яка дорівнює півсумі добутків концентрації С кожного йона на квадрат його заряду z:
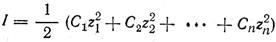
Контрольні запитання:
- Які речовини називаються електролітами?
- Сформулюйте основні положення ТЕД.
- Що називається ступенем дисоціації і константою дисоціації?
- Складіть рівняння електролітичної дисоціації речовин: H3PO4, Ba(OH)2, AlCl3.
- Визначте силу електроліту за значенням ступеня дисоціації, якщо з 400 молекул продисоціювало 160.
Література:
- Глинка Н.Л. Общая химия: Учебное пособие для вузов. – Л.: Химия, 1979. – Гл. VІІІ, §§ 82-87, с. 233-246.
- Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. І, Гл. 5, §§ 39-43, с. 49-52.
Тема 3.4. Гідроліз солей.
План
- Поняття про йонний добуток води.*
- Гідроліз солей.**
3. Поняття про константу гідролізу.***
1. Хоча вода і є слабким електролітом, але вона здатна на невелику дисоціацію:
Н2О ↔ Н+ + ОН-
За величиною електропровідності чистої води можна обчислити концентрацію йонів Гідрогену та гідроксид-йонів у воді. При 25С вона дорівнює 10-7 моль/л.
Константа дисоціації води:
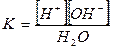
Перепишемо рівняння так:
[Н+][ОН-]=[Н2О]К
[Н+][ОН-]=КН2О
Це рівняння показує, що для води і розбавлених водних розчинів при незмінній температурі добуток концентрацій йонів Гідрогену і гідроксид-йонів є величина стала. Ця стала величина називається йонним добутком води.
КН2О = 10-7 ∙10-7 = 10-14
Водневий показник – від`ємний десятковий логарифм йонів Гідрогену:
рН = -lg[H+]
Для вимірювання рН існують різні методи. Найчастіше використовують індикатори.
2. Гідроліз солей – це процес взаємодії солі з водою внаслідок чого утворюється слабкий електроліт і змінюється рН середовища.
4 типи:
1) сіль утворена сильною основою та слабкою кислотою (Na2CO3), рН>7
І. Na2CO3 + H2O ↔ NaHCO3 + NaOH
2Na+ + CO32- + H2O ↔ 2Na+ + HCO3- + OH-
CO32- + H2O ↔ HCO3- + OH-
II. NaHCO3 + H2O ↔ Na2CO3 + NaOH
Na+ + HCO3- + H2O ↔ Na+ + H2CO3 + OH-
HCO3- + H2O ↔ H2CO3 + OH-
2) сіль утворена слабкою основою та сильною кислотою (CuCl2), рН<7
І. CuCl2 + H2O ↔ CuOHCl + HCl
Cu2+ + 2Cl- + H2O ↔ CuOH+ + H+ + 2Cl-
Cu2+ + H2O ↔ CuOH+ + H+
II. CuOHCl + H2O ↔ Cu(OH)2 + HCl
CuOH+ + Cl- + H2O ↔ Cu(OH)2 + H+ + Cl-
CuOH+ + H2O ↔ Cu(OH)2 + H+
3) сіль утворена слабкою основою та слабкою кислотою (NH4NO2), рН≈7
NH4NO2 + H2O ↔ NH4NO2 + HNO2
NH4+ + NO2- + H2O ↔ NH4NO2 + HNO2
4) сіль утворена сильною основою та сильною кислотою (NaCl) – гідроліз не відбувається
3. У розглянутих випадках гідролізується не вся кількість солі, яка є в розчині, а тільки її частина. Інакше кажучи, у розчині встановлюється рівновага між сіллю і кислотою та основою, що її утворюють. Частка речовини, що гідролізується, - ступінь гідролізу – залежить від константи цієї рівноваги, а також від температури і від концентрації солі.
Запишемо рівняння гідролізу у загальному вигляді. Нехай НА – кислота, МОН – основа, МА – утворена ними сіль. Тоді рівняння гідролізу матиме вигляд:
МА + Н2О ↔ НА + МОН
Константа рівноваги:
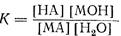
Концентрація води у розбавлених розчинах є практично сталою величиною. Позначаючи [Н2О]К = Кг дістанемо:
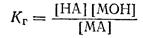
Величина Кг називається константою гідролізу у солі. ЇЇ значення характеризує здатність солі гідролізуватися; чим більше Кг, тим більшою мірою відбувається гідроліз.
1) сіль утворена сильною основою та слабкою кислотою
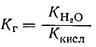
2) сіль утворена слабкою основою та сильною кислотою
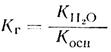
3) сіль утворена слабкою основою та слабкою кислотою
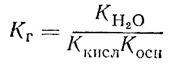
Контрольні запитання:
- Що називається йонним добутком води?
- Що називається гідролізом солей? Типи гідролізу солей.
- Визначте рН середовища розчинів солей: AlCl3, Ca(NO3)2, Na2SO3. Скласти відповідні рівняння гідролізу.
- Чому дорівнює концентрація гідроксид-йонів в розчині, рН якого дорівнює 10,8?
- Обчислити ступінь гідролізу ацетату калію в 0,1М розчині і рН розчину.
Література:
- Глинка Н.Л. Общая химия: Учебное пособие для вузов. – Л.: Химия, 1979. – Гл. VІІІ, §§ 90-92, с. 251-263.
- Хомченко Г.П. Химия. – М.: Высшая школа, 1981. – Ч. І, Гл. 5, §§ 45-46, с. 53-56.
