Vii. електролітична дисоціація
1. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) NaHCO3 i NaOH; б) K2SiO3 i HCl.
2. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) K2S i HCl; б) FeSO4 i (NH4)2S.
3. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Mg2+ + CO 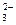 = б) H+ + OH
= б) H+ + OH 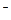 =
=
4. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) BaCl2 i Na2SO4; б) CrCl3 i KOH.
5. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) KHS i H2SO4; б) CaCl2 i AgNO3.
6. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) BaCO3 і HNO3; б) FeCl3 і KOH.
7. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Cu2+ + S2- = б) SiO 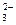 + 2H+ =
+ 2H+ =
8. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) Ca(OH)2 і HCl; б) CdSO4 і Na2S.
9. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) H3PO4 і Na2CO3; б) Na2SiO3 і CaCl2.
10. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) AgNO3 і K2CrO4; б) Pb(NO3)2 і KJ.
11. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Ca2+ + CO32- = б) Pb2+ + 2J 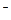 =
=
12. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) Cu(OH)2 і HNO3; б) Zn(OH)NO3 і HNO3.
13. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) Na3PO4 і CaCl2; б) K2CO3 і BaCl2.
14. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Fe3+ + 3ОH- = б) Cd2+ + 2OH 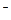 =
=
15. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) CaS і HCl; б) Cr(OH)3 і NaOH;.
16. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Zn2+ + S2- = б) Ag+ + Cl 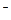 =
=
17. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) між сульфідом натрію і соляною кислотою;
б) між сульфатом заліза (ІІІ) і гідроксидом натрію.
18. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) (NH4)2SO4 і Ba(OH)2; б) KOH і CoCl2
19. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) AlCl3 і AgNO3; б) NaHCO3 і HCl
20. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) Ba(NO3)2 і H2SO4; б) Fe2(SO4)3 і K3PO4
21. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) 2H+ + SiO32- = б) PO43-+ Al3+ =
22. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Pb2+ + 2Cl 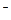 = б) Ag+ + J
= б) Ag+ + J 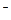 =
=
23. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Cu2+ + S2- = б) Ca(OH)+ + OH- =
24. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Ca2+ + CO 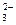 = б) 2H+ + CO
= б) 2H+ + CO 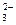 =
=
25. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Ni2+ + S2- = б) SO 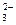 + Pb2+ =
+ Pb2+ =
26. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) NiSO4 і K2S; б) Na2SO3 і H2SO4(р).
27. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) K2CO3 i MgCl2; б) Cu(OH)2 і H2SO4.
28. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) HCl i NaOH; б) Pb(NO3)2 i Na2S
29. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) СO 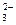 + 2H+ = б) Pb2+ + 2Cl
+ 2H+ = б) Pb2+ + 2Cl 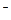 =
=
30. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) BaCl2 і CuSO4; б) Na2CO3 і CaCl2.
31. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) HCl i Fe(OH)2Cl; б) AgNO3 i Na2S
32. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Al3+ + 3OH 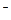 = б) Ag+ + CN
= б) Ag+ + CN 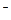 =
=
33. Скласти рівняння реакцій, що відбуваються в розчинах, в молекулярному та іонному виді між:
а) BaCl2 i Na2CO3; б) FeCl3 i Na2S
34. Дописати рівняння реакцій в іонному виді і скласти до них рівняння в молекулярному виді:
а) Ca2+ + 2F 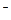 = б) Zn2+ + 2OH
= б) Zn2+ + 2OH 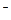 =
=
VIII. ГІДРОЛІЗ СОЛЕЙ
1. Написати рівняння реакції гідролізу в молекулярному та іонному виді для солей AgNO3 і MgCl2 Визначити, яке середовище утворюється в розчинах цих солей, та вказати значення рН.
2. Написати рівняння реакції гідролізу в молекулярному та іонному виді для солей Na2SiO3 і CrCl3. Визначити, яке середовище утворюється в розчинах цих солей, та вказати значення рН.
3. Написати рівняння реакції гідролізу в молекулярному та іонному виді для солей: FeCl3 і K2SiO3. Визначити, яке середовище утворюється в розчинах цих солей, та вказати значення рН.
4. Скласти рівняння гідролізу Na2S за ступенями. Яке значення рН має розчин цієї солі?
5. Яку реакцію повинні мати розчини таких солей: CuSO4, Na2CO3, K2SO4? Написати, де можливо, рівняння реакцій гідролізу в молекулярному та іонному виді.
6. Яка з солей (NH4)2SiO3 або NH4Cl більше підлягає гідролізу? Чому? Написати рівняння реакцій гідролізу цих солей в молекулярному та іонному виді. Визначити яким буде середовище розчинів.
7. Яке забарвлення має лакмус при розчиненні солей AlCl3, K2CO3, NaCl? Пояснити чому. Написати рівняння відповідних реакцій в молекулярному та іонному виді.
8. Дати визначення поняття гідролізу солей. В яких випадках виникають кислі солі? Відповідь підтвердити рівняннями відповідних реакцій в молекулярному та іонному виді.
9. Які з наведених солей підлягають гідролізу: NiCl2, FeSO4, КNO3. Написати, де можливо, рівняння реакцій гідролізу в молекулярному та іонному виді. Визначити, яке середовище утворюється в розчинах цих солей, та вказати значення рН.
10. Скласти рівняння гідролізу Fe(OH)Cl2 по ступеням. Яке значення рН має розчин цієї солі?
11. Навести приклади реакцій гідролізу солей в молекулярному та іонному виді з утворенням розчину, який має: а) рН>7, б) рН<7, в) рН=7.
12. Написати два рівняння реакцій гідролізу солей, в молекулярному та іонному виді, з утворенням основної солі.
13. Які з солей NaCl, Na2S, CoCl2 підлягають гідролізу? Скласти рівняння гідролізу відповідних солей в молекулярному та іонному виді. Яке значення рН мають розчини цих солей?
14. Скласти рівняння гідролізу KH2PO4 по ступеням. Яке значення рН має розчин цієї солі?
15. Написати рівняння гідролізу солей ZnSO4 та FeCl3 в молекулярному та іонному виді. Яке значення рН мають розчини цих солей?
16. Скласти рівняння гідролізу солей K2S та CuSO4 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
17. Які з солей K2SO3, K2SO4, FeCl3 підлягають гідролізу? Скласти рівняння гідролізу відповідних солей в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
18. Скласти рівняння гідролізу Na2SiO3 по ступеням. Яке значення pH має розчин цієї солі?
19. Які з солей KNO3, CrCl3, NaНCО3 підлягають гідролізу? Скласти рівняння гідролізу відповідних солей в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
20. Яка з солей FeCl2 чи FeCl3 більшою мірою підлягає гідролізу? Відповідь мотивувати. Скласти рівняння гідролізу наведених солей в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
21. Скласти рівняння гідролізу Al(NO3)3 по ступеням. Яке значення pH має розчин цієї солі?
22. Скласти рівняння гідролізу солей CuSO3 та K2CO3 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
23. Скласти рівняння гідролізу солей: FeCl3 та K2S в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
24. Скласти рівняння гідролізу солей: ZnCl2 та Na2CO3 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
25. Скласти рівняння гідролізу К3РО4 по ступеням. Яке значення pH має розчин цієї солі?
26. Скласти рівняння гідролізу AlCl3 по ступеням. Яке значення pH має розчин цієї солі?
27. Скласти рівняння гідролізу солей Cr2(SO4)3 та Na2SO3 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
28. Скласти рівняння гідролізу солей MgCl2 та Bi(NO3)3 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
29. Скласти рівняння гідролізу солей NaNO2 та Cu(NO3)2 в молекулярному та іонному виді. Яке значення pH мають розчини цих солей?
30. Скласти рівняння гідролізу Cr(OH)(NO3)2 по ступеням. Яке значення pH має розчин цієї солі?
31. Скласти рівняння гідролізу Na2HPO4 по ступеням. Яке значення pH має розчин цієї солі?
32. Скласти рівняння гідролізу SnCl2 по ступеням. Яке значення pH має розчин цієї солі?
33. Скласти рівняння гідролізу Cr(OH)Cl2 по ступеням. Яке значення pH має розчин цієї солі?
34. Скласти рівняння гідролізу Cr(OH)(NO3)2 по ступеням. Яке значення pH має розчин цієї солі?
