Определение средних содержаний элементов в руде методом среднего арифметического
Лабораторная работа №6
Определение атомных и весовых количеств элементов. Перевод атомных количеств в весовые проценты. Расчет средних содержаний.
Задание 1. Определение содержания элементов в пробах.
Даны количественные содержания основных оксидов по результатам силикатного анализа кварцевых порфиров месторождения «Молодежного», Оренбургская область (таблица 2). Необходимо определить, сколько каждого элемента (в весовых процентах) находится в отдельных пробах.
Пересчитать весовые проценты оксидов SiO2, Al2O3, Fe2O3, FeO, TiO2, MnO, MgO, CaO, Na2O, K2O, P2O5, SO3 на весовые проценты элементов, с составлением таблицы, используя нижеприведенный порядок расчетов.
Взять данные по атомной массе элементов из периодической таблицы Д.И.Менделева или из таблицы 1.
Таблица 1. Атомные массы элементов и их оксидов, расчетные коэффициенты элементов (К)
| Элементы | О | Si | Al | Fe | Ti | Mn | Mg | Ca | Na | K | P |
| Атомные массы | |||||||||||
| Оксиды | SiO2 | Al2O3 | FeO | Fe2O3 | TiO2 | MnO | MgO | CaO | Na2O | K2O | P2O5 |
| Молекулярные массы | |||||||||||
| Элементы | О | Si | Al | Fe | Ti | Mn | Mg | Ca | Na | K | P |
| Расчетный коэффициент К элементов |
Рассчитать молекулярную массу каждого оксида. Результаты записать в таблицу 1.
По соотношениям молекулярного веса оксида и атомной массы элемента (металла), входящего в его состав, рассчитываем концентрацию элемента в оксидах во всех пробах в весовых процентах, исходя из пропорции:
Приводим пример расчета для оксида кремния SiO2 в пробе 15.
Атомная масса О = 16;
Атомная масса Si = 28;
Рассчитываем молекулярную массу оксида кремния (в у.е.): SiO2 = 28 + 16×2 = 60;
содержание SiO2 в вес.% по пробе 15 из таблицы 2 = 70.4%.
Составляем пропорцию:
60 SiO2 – 70,4% SiO2
28 Si – Х% Si,
где Х – искомая величина, т.е., содержание Si в SiO2 в вес.% в исследуемом образце кварцевых порфиров месторождения «Молодежного».
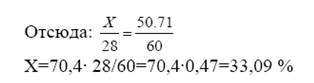
В приведенном расчете множитель 28/60 представляет собой частное от деления атомного веса определяемого элемента (в данном случае Si) на молекулярный вес оксида SiO2. Этот множитель остается постоянным применительно к любому значению содержания SiO2 в весовых %.
Вышеприведенная схема определения весовых количеств элемента с использованием атомных количеств применима к расчету содержаний любого элемента в весовых процентах по процентному содержанию его оксида. Поэтому нет необходимости в каждом конкретном случае составлять вышеприведенную пропорцию и решать ее. Следует принять отношение атомного веса элемента к его молекулярному весу за своего рода константу, расчетный коэффициент К, для использования при определении процентного
содержания элементов по содержанию их оксидов в весовых процентах.
Определяем расчетный коэффициент К для каждого элемента по формуле, включающий в числители атомный вес элемента А, в знаменателе - молекулярный вес оксида:
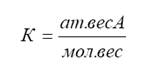
Результаты расчетов коэффициентов К для каждого элемента вносим в таблицу 1, составляемую по нижеприведенной форме.
Таблица 2. Данные химического анализа кварцевых порфиритов
месторождения «Молодежное»
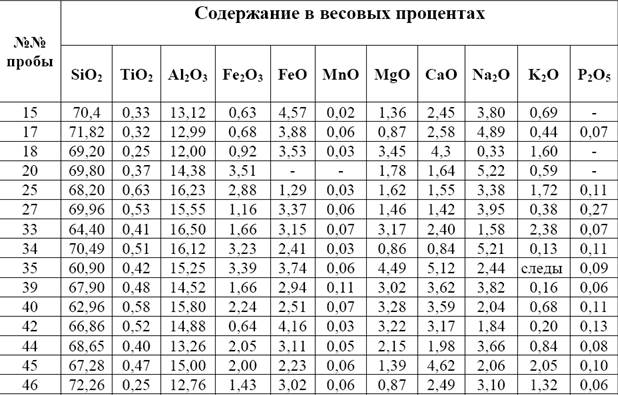
Используя данные таблицы 2 производим расчеты по определению содержания элементов в весовых процентах в каждой пробе (15-46). Для этого содержание оксида в весовых процентах (таблица 2) умножаем на расчетный коэффициент. Полученные данные заносим в таблицу 3.
Например К для SiO2 равен: 28/60 = 0,74.
Тогда содержание Si в SiO2 в вес.% в исследуемом образце кварцевых порфиров месторождения «Молодежного» равно: 70,4 · 0,74 = 33,09 (вес.%)
Таблица 3. Содержание элементов в кварцевых порфиритах месторождения «Молодежное»
 Элементы Номера проб Элементы Номера проб | О | Si | Al | Fe | Ti | Mn | Mg | Ca | Na | K | P |
| … |
Задание 2
Определение средних содержаний элементов в руде методом среднего арифметического.
Среднее арифметическое содержание рассчитываем по формуле, и результаты вычислений заносим в таблицу 4:
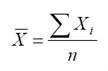
где Хi - содержание элемента в конкретной пробе, n – количество проб.
Таблица 4. Среднее содержание элементов в оксидах кварцевых порфиритов месторождения «Молодежное»
| Среднее содержание элементов в кварцевых порфиритах (в вес %) | ||||||||||
| Si | Ti | Al | Fe3+ | Fe2+ | Mn | Mg | Ca | Na | K | P |
| Кларки металлов в земной коре (вписать из таблицы) | ||||||||||
Записать следующие выводы:
1. Какой элемент/ы (металл/ы) преобладает в руде данного месторождения?
2. Какой металл/ы находится в дефиците, является редким?
3. По каким металлам данное месторождение может считаться богатым? (Для ответа на этот вопрос сравните среднее содержание редкого элемента с его кларком в земной коре).
4. Есть ли смысл добывать редкий металл в данном месторождении? (для ответа на этот вопрос сравните среднее содержание редкого элемента с его кларком в земной коре).
