Теория химического строения А. М. Бутлерова
ДОМАШНЕЕ ЗАДАНИЕ ПО ОРГАНИЧЕСКОЙ ХИМИИ
(по номеру в журнале группы)
ВАРИАНТ № 1
1. Теория химического строения органических веществ А.М. Бутлерова.
2. Карбоновые кислоты и их производные. Строение, номенклатура, изомерия.
3. Напишите уравнения реакций взаимодействия брома и водорода с бензолом, толуолом и стиролом. Покажите различие этих реакций.
4. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
O
¤¤
а) С2 Н4 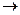 C2H5 Br
C2H5 Br 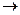 C2 H5 OH
C2 H5 OH 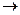 CH3 COOH
CH3 COOH 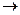 CH3 – C – O – C2 H5;
CH3 – C – O – C2 H5;
О
//
CH3– С
\
О О О
¤¤ ¤¤ \
б) С2 Н4 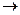 CH3 – С
CH3 – С 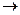 CH3 – C
CH3 – C 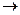 Са
Са
\ \ /
Н ОН О
/
CH3 – С
\\
О
5. Сколько г анилина можно получить из 61,5 г нитробензола при 90 %-ном выходе?
ВАРИАНТ № 2
1. Электронное строение атома углерода. Три типа гибридизации орбиталей атома углерода.
2. Получение, физические и химические свойства одноосновных карбоновых кислот.
3. Продукт полного гидролиза крахмала восстанавливает серебро из аммиачного раствора оксида серебра, а с уксусной кислотой образует сложный эфир. Какое вещество образовалось в результате полного гидролиза крахмала? Составьте соответствующие уравнения.
4. Исходным сырьем для получения хлоропренового каучука является ацетилен. Реакция идет по схеме: ацетилен → винилацетилен → хлоропрен → полимер хлоропрена. Напишите уравнение реакции получения хлоропренового каучука
5. Сколько звеньев С6Н10О5 в хлопковом волокне, если его молекулярная масса 1620000? Опишите химические свойства целлюлозы.
ВАРИАНТ № 3
1. Явление изомерии в органической химии. Типы изомерии.
2. Представители гидроксикислот в пищевой промышленности.
3. Один из способов получения спиртов заключается в том, что галогенопроизводные предельных углеводородов нагревают с растворами едких щелочей. Составьте уравнение реакции образования спирта:
а) из иодистого метила;
б) из иодистого пропила.
4. Приведите промышленные способы получения этиленгликоля. Какое применение находит он и его эфиры в промышленности? Напишите уравнения реакций.
5. В производстве кондитерских изделий применяют инвертный сахар (смесь равных количеств глюкозы и фруктозы). Сколько нужно взять сахарозы для получения из нее гидролизом 720 г инвертного сахара?
ВАРИАНТ № 4
1. Классификация реакций в органической химии.
2. Простые эфиры. Строение, свойства, получение.
3. Какие вещества получаются при полном гидрировании ароматических углеводородов:
а) бензола;
б) толуола;
в) стирола;
г) 1-метил-4-изопропилбензола?
Назовите образующиеся углеводороды.
4. Реакция серебряного зеркала является характерной для альдегидов. Почему муравьиная кислота даёт эту реакцию?
5. 5 т свекольной стружки, содержащей 12% сахара, поместили в диффузоры и пропустили через них 1000 л горячей воды. Определите концентрацию сахара в растворе, вытекающем из последнего диффузора, если степень экстракции сахара и свеклы 90%.
ВАРИАНТ № 5
1. Классификация органических соединений. Функциональные группы. Бифункциональные соединения.
2. Сложные эфиры. Строение, свойства, получение
3. Установите молекулярную формулу предельного углеводорода, если плотность его паров по воздуху равна 1,52.
4. Сколько кг натриевого мыла и глицерина можно получить из 1780 кг жира
С3Н5 (— О—С—С17Н35)3, если омылению подвергнулось 80 % жира?
║
О
5. Напишите уравнения реакций брожения глюкозы.
ВАРИАНТ № 6
1. Гомологический ряд предельных углеводородов. Изомерия. Номенклатура.
2. Высшие жирные кислоты. Состав и строение жиров.
3. Напишите структурные формулы изомеров состава С4Н9Cl. Назовите их по систематической номенклатуре. Какие типы связей существуют в этих соединениях?
4. Заполните схему превращений:
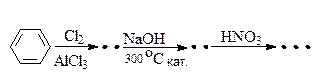
5. При гидрировании 20 л бутадиена образовалось 14 л бутана. Рассчитайте выход продукта реакции (%)
ВАРИАНТ №7
1. Способы получения алканов. Физические и химические свойства. Применение.
2. Синтез жиров. Твердые и жидкие жиры. Гидрогенизация жиров. Биологическая роль жиров.
3. Напишите и объясните реакции получения спиртов путём гидратации этиленовых углеводородов:
а) этилена;
б) пропилена;
в) бутилена;
г) изобутилена.
Назовите образующиеся спирты.
4. Напишите структурные формулы изомеров состава С6Н12, назовите их, укажите первичные, вторичные, третичные атомы углерода. Какой тип связи существует в этих соединениях? Объясните понятие "sp3-гибридизация".
5.Через бромную воду массой 120 г пропустили ацетилен объемом 4л до полного обесцвечивания раствора. Определите массовую долю (%) брома в бромной воде
ВАРИАНТ № 8
1. Циклоалканы. Получение, особенности химических свойств.
2. Омыление жиров. Мыла и синтетические моющие средства. Моющая способность в жесткой воде.
3. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения: а) С2 Н6 → С2 Н2 → С6 Н6 → С6 Н12; б) СаС2 → С2 Н2 → С6 Н6→ С6 Н5 NO2.
4. Какие превращения претерпевает изопропиловый спирт, если его: а) нагревать с галогеноводородными кислотами; б) нагревать с изопропиловым спиртом в присутствии серной кислоты; в) смешать с небольшим количеством металлического натрия? Напишите указанные реакции и назовите получившиеся соединения.
5. Сколько граммов уксусного альдегида (условия нормальные)можно получить путём окисления 200 мл 95,6%-ного спирта с плотностью 0,80 г/мл ?
ВАРИАНТ № 9
1. Гомологический ряд этиленовых углеводородов. Изомерия. Номенклатура.
2. Нитросоединения. Получение. Тринитротолуол. Особенность строения нитрогруппы.
3. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
С12 Н22 О11 → С6 Н12 О6 → С2 Н5 ОН → С2 Н4 → С2 Н5 Cl
4. Бутилкаучук является сополимером изобутилена и бутадиена. Резина, получаемая из бутилкаучука, обладает устойчивостью к старению и химическим воздействиям. Составьте примерную схему реакции сополимеризации, при которой получается этот вид каучука.
5. Щелочной гидролиз жиров. Какая масса глицерина образуется при щелочном гидролизе 331,5г триолеата глицерина?
ВАРИАНТ № 10
1. Химическая связь в органических соединениях. Механизм образования кратной связи.
2. Амины. Получение, строение и свойства.
3. В двух пробирках находятся уксусная и муравьиная кислоты. Какие характерные реакции дают возможность распознать их?
4. Установите структуру углеводорода С5Н10, если он обесцвечивает бромную воду и окисляется в уксусную и пропионовую кислоты. Напишите все реакции.
5. Хозяйственное мыло на заводах получают омылением твёрдых жиров раствором едкого натра. Сколько 60%-ного хозяйственного мыла получит фабрика из 10 т жира, содержащего 40% глицерида стеариновой кислоты, 40% глицерида пальмитиновой кислоты и 20% воды и примесей?
ВАРИАНТ № 11
1. Физические и химические свойства алкенов. Способы получения. Применение.
2. Анилин. Физические и химические свойства. Синтез анилина по Зинину.
3. При нагревании бензола с хлоропроизводными предельных углеводородов в присутствии хлорида алюминия получаются гомологи бензола. Составьте уравнение реакции образования метилбензола (толуола) и этилбензола.
4. Имеется два вещества состава С2Н6О. Одно из них реагирует с металлическим натрием с выделением водорода, другое не реагирует с металлическим натрием, но при нагревании с концентрированной серной кислотой образует две молекулы спирта. Напишите структурные формулы этих соединений.
5. Сколько кг 80%-ной уксусной кислоты можно получить при окислении 11 кг уксусного альдегида?
ВАРИАНТ №12
1. Галогенпроизводные углеводородов. Строение, свойства, получение.
2. Анилинокрасочная промышленность. Сырье, основные продукты.
3. Действием аммиака на галогенозамещённые кислоты можно получить следующие аминокислоты: аминоуксусную, α-, β-диаминомасляную, ε-аминокапроновую. Составьте уравнения соответствующих реакций.
4. Состав хлоропрена выражается формулой СН2 = С – СН = СН2
|
Cl
Составьте уравнения реакции полимеризации хлоропрена.
5. Гидролиз целлюлозы и крахмала выражают суммарно одним уравнением. Напишите это уравнение и рассчитайте, сколько глюкозы можно получить из 1 т древесины, содержащей 45% целлюлозы, если выход глюкозы составляет 80% теоретически возможного.
ВАРИАНТ № 13
1. Химические свойства алкадиенов. Способы получения. Номенклатура. Основные представители. Бутадиен.
2. Аминокислоты. Строение. Номенклатура.
3. Углеводород С8Н18 можно получить по реакциям Вюрца без побочных продуктов. При его бромировании и нитровании получаются третичные продукты замещения, а при хлорировании - три изомерных хлоралкана. Установите строение С8Н18, назовите углеводород и напишите все реакции.
4. Сколько безводной уксусной кислоты можно получить из 100 т технического карбида кальция, содержащего 4% примесей?
5. В двух пробирках находятся растворы глицерина и этилового спирта. При помощи какой реакции можно их отличить?
ВАРИАНТ № 14
1. Синтетический и натуральный каучук. Сравнение строения и свойств. Резины.
2.Получение и химические свойства α. –аминокислот. Биологическая роль α. –аминокислот.
3.Напишите уравнения реакций получения ароматических углеводородов ряда бензола путём каталитического дегидрирования алициклических углеводородов:
а) циклогексана;
б) метилциклогексана;
в) 1,2-диметилциклогексана.
Назовите полученные соединения.
4. Определите процентное содержание элементов в следующих кислотах:
а) муравьиной;
б) щавелевой;
в) бензойной.
5. Рассчитайте процентную концентрацию раствора спирта, которая получается в результате спиртового брожения 10 кг раствора, содержащего 1 кг глюкозы. Сколько углекислого газа при этом выделится?
ВАРИАНТ №15
1. Химические свойства алкинов. Номенклатура. Особенности строения.
2.Образование пептидной связи. Пептиды. Полипептиды.
3. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
а) СН3 – СН2 – СН = СН2 → СН3 – СН2 – СН2 – СН2Cl → СН3 – СН2 – СН2
О О
// //
б) С → СН4 → СН3Cl → СН3ОН → Н – С → Н – С
\ \
Н ОН
4. Приведите способы получения фенола. Какие из них могут быть использованы в промышленности и почему?
5. Строение и сравнение свойств глюкозы и фруктозы. Приведите уравнение реакции, с помощью которой можно различить глюкозу и фруктозу?
ВАРИАНТ № 16
1. Ацетилен. Свойства и получение.
2. Белки. Строение. Структурная организация. Биологическая роль белков.
3. Дегидратация спиртов в присутствии серной кислоты ведёт к образованию простых эфиров. Напишите уравнения реакций дегидратации для следующих спиртов: а) пропилового и изопропилового, б) двух молекул 2-метилбутанола-2,
в) двух молекул пентанола. Назовите полученные соединения.
4. Сколько г оксида серебра можно восстановить при помощи 200 мл 36 %-ного раствора муравьиного альдегида плотностью 1,11г/мл?
5. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
С2Н6 → С2Н5Cl → СН3 – СН2ОН → СН3 – СООН → СН2 – СООН →
׀
Cl
О
 → СН2 – СООН → H2N – СН2 – С – NH – СН2 – С ⁄⁄
→ СН2 – СООН → H2N – СН2 – С – NH – СН2 – С ⁄⁄
׀ ║ ОН
NH2 О
ВАРИАНТ № 17
1. Арены. Бензол и его гомологический ряд. Строение молекулы бензола. Ароматичность.
2. Моносахариды. Классификация.
3. Определите строение соединения С5Н11Br, при реакции которого с водным раствором NaOH получается первичный спирт, а при нагревании со спиртовым раствором NaOH и последующем действии бромоводорода получается 2-бром-2-метилбутан. Назовите С5Н11Br.
4. Какой объем углекислого газа (н.у.) выделится при брожении глюкозы, если при этом получено 11,5г этанола?
5. Как происходит полимеризация бутадиена? Напишите уравнения реакций.
ВАРИАНТ № 18
1. Получение и применение бензола.
2. Углеводы. Строение. Классификация. Нахождение в природе. Биологическая роль.
3. Напишите уравнения реакций получения диэтилового эфира методом дегидратации соответствующего спирта в присутствии серной кислоты.
4.Мочевину (карбамид) Н2N – С – NH2 получают нагреванием смеси аммиака с
║
О
углекислым газом либо фосгена СOCl2 с аммиаком. Составьте уравнения соответствующих реакций.
5.Сколько литров формальдегида, взятого при нормальных условиях, нужно растворить в воде, чтобы получить 2 л 36%-ного формалина плотностью 1,11г/мл?
ВАРИАНТ № 19
1. Физические и химические свойства бензола. Правила замещения в бензольном ядре.
2. Строение, химические свойства глюкозы и фруктозы.
3. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
О
 а) С → СН4 → СН3Cl → СН3ОН → НС ⁄⁄
а) С → СН4 → СН3Cl → СН3ОН → НС ⁄⁄
Н
О
 б) С → СаС2 → Н – С ≡ С – Н → СН3 – С ⁄⁄
б) С → СаС2 → Н – С ≡ С – Н → СН3 – С ⁄⁄
Н
4. Выведите формулы всех изомерных спиртов С4Н10О и назовите их по радикальной и систематической номенклатурах.
5. На предприятиях химической промышленности уксусный ангидрид получают каталитической дегидратацией уксусной кислоты при температуре 600˚ С. Сколько т уксусного ангидрид получат таким методом из 15 т 80 %-ной уксусной кислоты, если выход уксусного ангидрида составляет 90 % теоретически возможного?
ВАРИАНТ № 20
1. Многоядерные ароматические углеводороды. Строение. Основные представители.
2. Дисахариды. Строение. Химические свойства. Восстанавливающие и невосстанавливающие дисахариды. Основные представители.
3. Назовите по систематической номенклатуре углеводороды:
Н
׀
а) СН3 – С ≡ СН б) СН3 – С – С ≡ СН в) СН3 – С ≡ С – СН3
׀
СН3
4. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
а) С → СаС2 → С2Н2 → С2Н4 → С2Н5ОН
5. Как из целлюлозы получают этиловый спирт? Напишите уравнение реакции и рассчитайте, сколько глюкозы получится из 1 т древесных опилок, содержащих 57% целлюлозы. Каков теоретический выход спирта?
ВАРИАНТ № 21
1. Природные источники углеводородов.
2. Полисахариды. Крахмал. Строение. Нахождение в природе. Продукты гидролиза крахмала. Иодкрахмальная проба. Применение крахмала.
3. Какие реакции свидетельствуют о том, что глюкоза является альдегидоспиртом?
4. Исходным сырьем для получения хлоропренового каучука является ацетилен. Реакция идет по схеме: ацетилен → винилацетилен → хлоропрен → полимер хлоропрена. Напишите уравнение реакции получения хлоропренового каучука.
5. С какими из указанных веществ будет реагировать этиловый спирт: с водой, натрием, раствором щелочи, соляной кислотой; кислородом, уксусной кислотой? Напишите уравнения возможных реакций.
ВАРИАНТ № 22
1. Природный и попутный газы. Их состав. Способы переработки. Применение.
2. Полисахариды. Целлюлоза. Строение. Нахождение в природе. Химические свойства. Образование сложных эфиров целлюлозы. Направления использования.
3. Напишите структурные формулы изомеров состава С4Н9Cl. Назовите их по систематической номенклатуре. Какие типы связей существуют в этих соединениях?
4. Приведите уравнения реакций гидрирования, бромирования, гидробромирования и гидратации стирола. Объясните механизм присоединения брома к винильной группе стирола.
5. Омыление жиров. Рассчитайте массы гидроксида калия и тристеарата глицерина, которые потребуются для получения стеарата калия массой 805 кг. Массовая доля выхода продукта составляет 80%.
ВАРИАНТ № 23
1. Нефть, ее состав. Первичная переработка нефти. Продукты первичной переработки нефти, их применение.
2. Пятичленные гетероциклические соединения. Фуран. Тиофен. Пиррол. Химические свойства. Получение. Применение.
3. Напишите структурные формулы следующих карбоновых кислот:
а) 2-метилбутановой;
б) 3-метилпентановой;
в) 2-метилпентановой;
г) 2,2-диметилпентановой;
д) 2,2,3-триметилбутановой;
4. Из каких 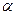 -аминокислот образованы следующие дипептиды:
-аминокислот образованы следующие дипептиды:
О Н О
// | //
NН2 – СН – С – NН – СН2СООН NН2 – С – С – NН – СН – СООН
| | |
СН3 СН3 СН3 – СН – СН3
Н О Н
| // |
NН2 – С – С – NН – СН2 – С – СООН
| |
СН3 СН3
5. За год цех выработал 13,76 т яблочный эссенции (изовалериановоизоамилового эфира), на что израсходовал 10,2 т изовалериановой кислоты и 8,8 т изоамилового спирта. Рассчитайте фактический расход сырья на 1 т эфира и выход его в процентах от теоретического.
ВАРИАНТ № 24
1. Каменный и бурый уголь. Способы переработки. Продукты переработки, их применение.
2. Шестичленные гетероциклические соединения. Пиридин. Химические свойства. Получение. Применение.
3. Назовите по систематической номенклатуре следующие ароматические углеводороды:
а) С6Н5 – СН3 д) С6Н5 – СН (СН3)2
б) С6Н5 – СН = СН2 е) С6Н5 – NO2
в) С6Н4 – (СН3)2 ж) С6Н4 – (С3Н7)2
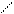 С2Н5
С2Н5
 г) С6Н4 з) С6Н4 – (Cl)2
г) С6Н4 з) С6Н4 – (Cl)2
СН3
4. Напишите уравнения реакций получения: а) муравьиного альдегида (фомальдегида) из спирта и метана; б) уксусного альдегида (ацетальдегида) из спирта и ацетилена.
5. Кусок мыла состава С17Н35 – С – ОNа массой 102 г опустили в стакан с избытком
║
О
серной кислоты. Содержимое размешали. Сколько г высокомолекулярной жирной кислоты всплыло на поверхность реакционной массы? Напишите уравнение реакции.
ВАРИАНТ № 25
1. Алифатические одноатомные спирты. Классификация. Номенклатура. Изомерия.
2. Химическая переработка древесины.
3. Напишите уравнение реакции получения изопрена из изопентана. Как называется эта реакция?
4. К синтетическим волокнам относится найлон. Он представляет собой продукт поликонденсации двухоснóвной (адипиновой) кислоты НООС – (СН2)4 – СООН и гексаметилендиамина Н2N – (CH2)6 – NH2. Составьте уравнение реакции образования найлона.
В чем преимущества синтетических волокон перед натуральными?
5. При окислении 10 мл метилового спирта (плотность 0,80г/мл) получено 120 г 3 %-ного раствора формальдегида. Каков его выход в процентах от теоретически возможного?
ВАРИАНТ № 26
1. Химические свойства и способы получения одноатомных предельных спиртов.
2. Нуклеиновые кислоты. Состав и строение. Биологическая роль.
3. Как получить бензол: а) из циклогексана; б) из бензойной кислоты; в) из фенола? Напишите уравнения реакций. Укажите промышленные способы получения бензола и толуола.
4. Назовите следующие вещества: С2Н5 – ОН, СН3 – О – СН3, СН3 – ОН,
С2Н5 – О – С2Н5, СН3 – О – С2Н5. К какому классу относится каждое из этих соединений? Напишите уравнения реакций их получения.
5. Сколько ацетилена было взято для получения 1 т уксусной кислоты, если производственные потери ацетилена 10 %, а окислилось альдегида 95 %?
ВАРИАНТ № 27
1. Многоатомные спирты. Этиленгликоль и глицерин. Получение и химические свойства.
2. Строение полимеров. Агрегатное и фазовое состояния.
3. Напишите структурные формулы следующих углеводородов: а) бутина- 2, б) 3-метиламина-1, в) 3,4-диметилпентина-1,
г) 2,5-диметилегксина-3,
д)3,3-диметилбутина-1.
4. Определите строение углеводорода С6Н14, при бромировании которого получается третичное бромпроизводное. Углеводород можно получить по реакции Вюрца без побочных продуктов. Напишите уравнения реакций и назовите углеводород.
5. Для получения уксусноэтилового эфира было взято 30 г безводной уксусной кислоты. Рассчитайте теоретический выход эфира, приняв практический выход равным 85 %.
ВАРИАНТ № 28
1. Фенолы. Изомерия и номенклатура. Химические свойства. Качественная реакция на фенол.
2. Методы синтеза высокомолекулярных соединений. Реакции полимеризации и поликонденсации.
3. Напишите структурные формулы спиртов с общей формулой С6Н14О, имеющих нормальный углеродный скелет (три изомера). Назовите их по систематической номенклатуре.
4. Составьте уравнения реакций, при помощи которых можно осуществить следующие превращения:
а) С2Н4 → С2Н5Br → С2Н5ОН → С2Н5 – О – СН3
б) СН4 → СН3Cl → СН3ОН → СН3 – О – СН3
5. Массовая доля крахмала в картофеле составляет 20%. Рассчитайте массу глюкозы, которая может быть получена из картофеля массой 405 кг. Выход продукта равен 70%.
ВАРИАНТ № 29
1. Строение, изомерия и номенклатура альдегидов и кетонов.
2. Механические и термомеханические свойства полимеров.
3. Напишите структурные формулы изомерных ацетиленовых углеводородов состава С7Н12, главная цепь которых состоит из пяти углеродных атомов, и назовите их по систематической номенклатуре.
4. Какие вещества и в каком количестве получаются из 1 кг этилового спирта:
а)при сжигании;
б) при нагревании.
5. Как получают и где используют ацетат целлюлозы? Составьте схемы реакций. Чем различаются моно-, ди- и триацетаты целлюлозы? Какие волокна называют искусственными, а какие – синтетическими?
ВАРИАНТ № 30
1. Способы получения и химические свойства альдегидов и кетонов. Реакция «серебряного зеркала».
2. Натуральные и синтетические волокна. Получение. Физические и химические свойства. Применение.
3. Напишите структурные формулы следующих соединений:
а) 2-метил-3-этилпентана
б) 2,2-диметил-3-этилпентана
в) 2,2,3-триэтилбутана
г) 2,3-диметилбутана
д) 2,5-диметил-3,3-диэтилгексана
е) 2,2,3,4-тетраметилгексана
ж) 2-метил-4-пропилгептана
з) 3-этил-4-пропилгексана
и) 2-метил-3-этил-5-пропилоктана
к) 2-метил-3-3-диэтилпентана.
4. Что с химической точки зрения представляет нитроглицерин? Напишите уравнение реакции его получения и укажите области его применения.
5. При сжигании 2,1 г углеводорода образовался углекислый газ массой 6,6 г и вода массой 2,7 г . Плотность паров этого углеводорода по водороду равна 28. Определите формулу вещества.
ВАРИАНТ № 31
1. Явление изомерии в органической химии. Типы изомерии.
2. Получение и химические свойства α. –аминокислот. Биологическая роль α. –аминокислот.
3. Напишите уравнения реакций образования сложных эфиров:
а) из уксусной кислоты и этилового спирта
б) из пропионовой кислоты и пропилового спирта
в) из масляной кислоты и этилового спирта
Как называется реакция образования сложного эфира?
4. Имеются два вещества состава С4Н8О2. Одно из них реагирует с карбонатом натрия с выделением углекислого газа, другое не реагирует с карбонатом натрия, но при нагревании с раствором щелочи образует спирт и соль. Напишите структурные формулы этих соединений.
5. Общая формула полисахарида (С6Н10О5)n. Рассчитайте, чему равно n в формулах молекул клетчатки льняного волокна (молекулярная масса 5 850 000) и клетчатки хлопкового волокна (молекулярная масса 1 750 000).
ВАРИАНТ № 32
1. Физические и химические свойства алкенов. Способы получения. Применение.
2. Синтез жиров. Твердые и жидкие жиры. Гидрогенизация жиров. Биологическая роль жиров.
3. Напишите структурные формулы спиртов с общей формулой С6Н14О, имеющих нормальный углеродный скелет (три изомера). Назовите их по систематической номенклатуре.
4. Какой мономер лежит в основе молекулы натурального каучука? Приведите формулу натурального каучука из трёх мономерных звеньев.
5. Вычислите объем воздуха, измеренный при н.у., который потребуется для полного сгорания бензола массой 5,3 г. Объемная доля кислорода в воздухе составляет 21%.
ВАРИАНТ № 33
1. Классификация органических соединений. Функциональные группы. Бифункциональные соединения.
2. Амины. Получение, строение и свойства.
3. В двух пробирках находятся растворы спирта и альдегида. Какая реакция поможет отличить альдегид от спирта? Как провести эту реакцию в лаборатории?
4. Из бензола любым способом синтезируйте фенол. Приведите реакции получения из фенола фенол-формальдегидных смол. Укажите условия проведения реакции.
5. Опишите при помощи уравнений процесс получения капрона. Перечислите свойства капрона. К каким смолам можно отнести капрон: к термопластическим или термореактивным? Как это можно доказать?
ВАРИАНТ № 34
1. Арены. Бензол и его гомологический ряд. Строение молекулы бензола. Ароматичность.
2. Углеводы. Строение. Классификация. Нахождение в природе. Биологическая роль.
3. Приведите все известные вам способы получения анилина; укажите, какие из них имеют промышленное значение.
4. Напишите формулу ε-аминокапроновой кислоты и схему реакции превращения ее в капролактам.
5. При полном гидролизе сахарозы образовалось 270 г смеси глюкозы и фруктозы. Определите массы сахарозы и воды, которые вступили в реакцию.
ВАРИАНТ № 35
1. Химические свойства алкинов. Номенклатура. Особенности строения.
2. Полисахариды. Крахмал. Строение. Нахождение в природе. Продукты гидролиза крахмала. Иодкрахмальная проба. Применение крахмала.
3. Напишите уравнения реакций, которые надо провести для осуществления следующих превращений:
циклогексан→бензол→этилбензол
4. Вычислите массу простого эфира, полученного из 25 г метанола по реакции межмолекулярной дегидратации, если реакция протекает с 80% выходом.
5. Составьте уравнения реакций получения мононитроклетчатки, динитроклетчатки и тринитроклетчатки. К какому классу соединений они относятся? Где применяются продукты нитрования целлюлозы
литература:
1. АРТЕМЕНКО А.И. Органическая химия, М., Высшая школа, 2009, 560с.
2. ЩЕРБИНА А.Э., МАТУСЕВИЧ Л.Г., СЕНЬКО И.В. Органическая химия. Задачи и упражнения. Учебное пособие. Минск, Новое знание, 2007, 297с.
3. РЕУТОВ О.А., КУРЦ А.Л., БУТИН К.П. Органическая химия. В 4 частях. Учебник. М., Бином. Лаборатория знаний, 2007.
ОРГАНИЧЕСКАЯ ХИМИЯ
Основные понятия органической химии
Углерод выделяется среди всех элементов тем, что его атомы могут связываться друг с другом в длинные цепи или циклы. Именно это свойство позволяет углероду образовывать миллионы соединений, изучению которых посвящена целая область — органическая химия.
Несколько причин обусловили проявление углеродом выше отмеченных свойств. Доказано, что энергия связи (прочность связи) С—С сопоставима с прочностью связей С—О. Углерод обладает возможностью проявлять не одну, а целых три разновидности гибридизации орбиталей: в случае sр3-гибридизации образуются четыре гибридных орбитали, имеющие тетраэдрическую ориентацию; с их помощью образуются простые ковалентные связи; в случае sp2-гибридизации образуются три гибридные орбитали, ориентированные в одной плоскости, и с их помощью образуются двойные кратные связи; наконец, с помощью двух sp-гибридизованных орбиталей, имеющих линейную ориентацию, между атомами углерода возникают тройные кратные связи. Сейчас хорошо известно, что атомы углерода способны образовывать простые, двойные и тройные связи не только друг с другом, но также и с другими элементами.
Теория химического строения А. М. Бутлерова.
Современная теория строения молекул объясняет и огромное число органических соединений, и зависимость свойств этих соединений от их химического строения. Она же полностью подтверждает основные принципы теории химического строения, разработанные выдающимся русским ученым А. М. Бутлеровым.
Основные положения этой теории (иногда ее называют структурной):
1) атомы в молекулах соединены между собой в определенном порядке химическими связями согласно их валентности;
2) свойства вещества определяются не только качественным составом, но и его строением, взаимным влиянием атомов, как связанных между собой химическими связями, так и непосредственно не связанных;
3) строение молекул может быть установлено на основе изучения их химических свойств.
Важным следствием теории строения был вывод о том, что каждое органическое соединение должно иметь одну химическую формулу, отражающую ее строение. Такой вывод теоретически обосновывал хорошо известное уже тогда явление изомерии,— существование веществ с одинаковым молекулярным составом, но обладающих различными свойствами.
Структурные формулы.
Существование изомеров потребовало использования не только простых молекулярных формул, но и структурных формул, отражающих порядок связи атомов в молекуле каждого изомера. В структурных формулах ковалентная связь обозначается черточкой. Как и в структурных формулах неорганических веществ, каждая черточка означает общую электронную пару, связывающую атомы в молекуле.
Структурная формула — изображение химических связей между атомами в молекуле с учетом их валентности.
