Классификация электролитов по степени диссоциации
Сильные α > 0,3; слабые α < 0,03 (при концентрации около 0,1 М)
Количественно процесс диссоциации электролита описывают константой диссоциации (КдисилирКдис).
Для слабых электролитов в справочных таблицах обычно приводят константы диссоциации или их отрицательные десятичные логарифмы.
| HA↔H+ + A– | Ка = Ккисл = [H+]•[A–]/[HA] | |
| pКа = -lg(Ка) |
Например, для уксусной кислоты (СН3СООН) Ка = 1,8•10-5; рКа = 4,8
Закон разбавления (Оствальда)
Допустим, концентрация электролита, распадающегося на 2 иона, равна С, а степень его диссоциации в данном растворе составляет a, тогда уравнение для константы диссоциации процессапримет вид:
Кдис= 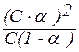 ,
,
где С·a – концентрация каждого из ионов, а С(1 – a) – концентрация недиссоциированных молекул.
Это уравнение представляет собой закон разбавления Оствальда. Оно позволяет определять степень диссоциации при разных концентрациях электролита, если определена его константа диссоциации; также константу диссоциации электролита, если известна его степень диссоциации при какой-либо концентрации. Для растворов, в которых диссоциация электролита очень мала, уравнение закона Оствальда можно упростить. В данном случае a<<1, и, следовательно, этой величиной можно пренебречь в знаменателе правой части уравнения. Тогда это уравнение примет следующий вид:
Кдис @ a2·С или a = 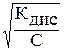
Таким образом, степень диссоциации возрастает при разбавлении раствора.
Величина Кдис электролита зависит от следующих факторов:
1.Природы электролита и растворителя;
2.Температуры;
но не зависит от концентрации растворённого вещества.
Кдис характеризует способность электролита распадаться на ионы. Чем меньше Кдис электролита, тем слабее электролит. Значения Кдис различных электролитов приводятся в справочниках при Т=298К (см. табл. 15).
Таблица 15
Значения Кдис различных электролитов
| Электролит | Константа диссоциации Ка (при 25°С) |
| HNO2 | Ка=4·10-4 |
| H2O2 | Ка, 1=10-12; Ка, 2=10-25 |
| H2SiO3 | Ка, 1=10-10; Ка, 2=10-22 |
| H2SO3 | Ка, 1=2·10-2; Ка, 2=10-14 |
| H2S | Ка, 1=6·10-8; Ка, 2=10-14 |
| CH3COOH | Ка =1,74·10-5 |
| HCOOH | Ка =1,8·10-4 |
| H2CO3 | Ка, 1=4,5·10-7; Ка, 2 =4,7·10-11 |
| NH4OH | Ка =1,8·10-5 |
| HF | Ка =7·10-4 |
Самым слабым электролитом из приведённых в таблице 15, является H2O2, а самым сильным – НF.
Все электролиты можно разделить на две группы: слабые и сильные.
Сильные электролиты в водных растворах диссоциированны практически полностью. Понятие степени диссоциации к ним практически не применимо.
Слабые электролиты диссоциируют в водных растворах лишь частично, и в растворе имеет место динамическое равновесие между недиссоциированными молекулами и ионами.
