ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ. 3.1. Плотность раствора серной кислоты, в 1 л которого содеожится 577 г Н2SO4,равна 1,335 г/мл
3.1. Плотность раствора серной кислоты, в 1 л которого содеожится 577 г Н2SO4,равна 1,335 г/мл. Вычислить процентную концентрацию раствора, а также его нормальность, молярность, моляльность и мольные доли Н2SО4 и Н2O. Ответ: 43,22%; 11,76н.; 5,88М; 7,76 моль/кг; 0,123; 0,877.
3.2. Определите нормальность, моляльность,
процентную концентрацию и титр 0,8М Fe2(SO4)3, если
плотность раствора равна 1 г/мл. Ответ: 4,8н.; 1,18
моль/кг; 32%; 0,3199 г/мл.
3.3. Вычислить процентную концентрацию и моляльность 8н. HNO3, плотность которой равна 1,246 г/мл. Каковы мольные доли HNO3 и Н2О в этом растворе? Ответ: 40,5%;10,8 моль/кг; 0,162; 0,838.
3.4. Вычислите грамм-эквивалент двухосновной кислоты, 37%-ный раствор которой 12,5н. и имеет плотность 1,664 г/мл. Какая это кислота? Чему равны молярная, моляльная концентрации и титр раствора этой кислоты? Ответ: 49,2 г; 6,25М; 5,94 моль/кг; 0,6156 г/мл.
3.5. B 1кг воды растворено 666 г КОН, плотность раствора равна 1,395 г/мл. Найти: массовую долю; молярность; моляльность раствора; мольные доли щелочи и воды. Ответ: 40%; 9,95 моль/л; 11,9 моль/кг; 0,176 и 0,824;
3,6. Плотность 15%-ного (по массе) раствора H2SO4 равна 1,105 г/мл. Вычислить: нормальность, молярность, моляльность раствора. Ответ: 3,38н.; 1,69 моль/л; 1,80 моль/кг.
3.7. Плотность 9%-ного (по массе) раствора сахарозы C12H22O11 равна 1,035 г/мл. Вычислить концентрацию сахарозы в г/л; молярность; моляльность раствора. Ответ: 93,2 г/л; 0,27 моль/л; 0,29 моль/кг.
3.8. Найти массу воды, необходимую для приготовления 1,5 моляльного раствора хлорида натрия, если имеется 10 г NaCl. Ответ: 144г.
3.9. Титр раствора серной кислоты 0,0245 г/мл. Определить молярную концентрацию раствора. Ответ: 0,25М.
3.10. Имеется 0,25н. раствор гидроксида натрия. Определить его титр. Ответ: 0,01 г/мл.
3.11. Рассчитать титр 0,15н. раствора: а) азотной кислоты; б) фосфорной кислоты; в) соляной кислоты. Ответ: а) 0,0095 г/мл; б) 0,0049 г/мл; в) 0, 0055 г/мл
3.12. Вычислите молярность, нормальность и моляльность раствора 20%-ной Н2SO4 плотностью 1,14 г/см3.
Ответ: 2,3 моль /л; 4,6н.; 2,55 моль/кг.
3.13. Вычислить молярность и нормальность раствора КI, титр которого равен 0,0017 г/мл. Ответ: 0,01М; 0,01н.
3.14. До какого объема нужно довести раствор при растворении 8,1 г FеС13, чтобы получить 0,1н. раствор? Каков титр раствора? Ответ: 1,5 л; 0,0054 г/мл.
3.15.Чему равна моляльность раствора, приготовленного растворением 9 г глюкозы С6Н12О6 в 500 мл воды? Ответ: 0,1 моль /кг.
3.16. Сколько граммов сахарозы C12H22O11 необходимо взять для пригововления 200 г раствора, моляльность которого равна 0,05 моль/кг? Ответ: 3,36 г.
3.17. Вычислите моляльность и массовую долю раствора (плотность 1,107 г/мл), содержащего 50 г СuSO4 в 450 мл воды.
Ответ: 0,694 моль/кг; 10%.
3.18. Опишите, как приготовить 1 л 1%-ного, одномолярного и однoнормального раствора серной кислоты.
3.19. Чему равен титр растворов: а) 0,1н. НС1; б) 1н. КОН; в) 0,5н. HNO3? Выразить титры в г/мл и в мг/мл.
3.20. Вычислите титр растворов: а) 0,1н. Н2SO4; б) 0,02н. Н3РO4; в) 0,02н. NаОН; г) 0,004н. Са(ОН)2. Выразите титры в г/мл и в мг/мл.
3.21. Титр раствора, серной кислоты равен 0,0049 г/мл. Какова нормальность раствора?
3.22. Титр раствора NаОН равен 2 мг/мл. Какова нормальность раствора?
3.23. На нейтрализацию 20 мл 1н. раствора гидроксида натрия пошло 20 мл раствора серной кислоты. Чему равны нормальность и титр раствора кислоты?
3.24. На нейтрализацию 40 мл 0,1н. раствора азотной кислоты пошло 4 мл раствора гидроксида натрия. Чему равны нормальность и титр раствора щелочи?
3.25. На нейтрализацию 60 мл 0,25н. Н2SO4 пошло 180 мл раствора КОН. Чему равны нормальность и титр раствора КОН?
Ответ: 0,083л.; 4,66 мг/мл.
3.26. Вычислить нормальность, моляльность, мольную долю и титр 50%-ного раствора гидроксида натрия.
3.27. Вычислите титры (в мг/мл) растворов а) 30%-ного КОН; б) 10%-ного НС1; в) 4%-ного NаОН. Определите нормальность этих растворов.
3.28. Вычислите моляльность и мольную долю растворов, приведенных в задаче №3.27.
3.29. Смешали 2 л 10%-ного и 4 л 24%-ного раствора азотной кислоты. Чему равна процентная концентрация, моляльность и мольная доля полученного раствора?
3.30. Из 10 кг 20%- ного раствора NаС1 при охлаждении выделилось 400 г соли. Чему равна процентная концентрация, моляльность и мольные доли NаС1 и Н2О охлажденного раствора?
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. ЗАКОН ВАНТ- ГОФФА
Примеры решения задач
Пример 1.
Вычисление осмотического давления растворов.
Вычислите осмотическое давление раствора, содержащего в
1,4 л 63 г глюкозы С6Н12О6 при 0°С.
Решение:
Осмотическое давление раствора определяют согласно закону Вант-Гоффа:
Pocм = nRT/V,
где п — количество растворенного вещества, моль;
V – объем раствора, м3;
R — молярная газовая постоянная, равная 8,3144 Дж/(моль-К).
В 1,4 л раствора содержится 63 г глюкозы, молярная масса которой равна 180,16 г/моль. Следовательно, в 1,4л раствора содержится
n= 63/180,16=0,35моль глюкозы.
Осмотическое давление этого раствора глюкозы:
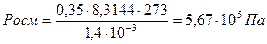
Пример 2.
Определение молекулярной массы неэлектролита по осмотическому давлению раствора.
Рассчитайте молекулярную массу неэлектролита, если в 5л раствора содержится 2,5 г неэлектролита. Осмотическое давление этого раствора равно 0,23∙105 Па при 20°С.
Решение:
Заменив п выражением m/M, где т — масса растворенного вещества, а М — его молярная масса, получим
Росм = mRT/(MV).
Отсюда молярная масса растворенного вещества равна
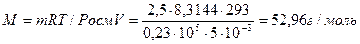
Следовательно, молекулярная масса неэлектролита равна 52,96-
Росм кПа: R=8,31 Дж/моль∙К;
Росм мм Hg ст.: R=62,32 л∙мм.рт.ст./град.∙моль;
Росм. атм.: R=0,082 л∙атм../град.∙моль;
