Флуоресцентні індикатори комплексонометрії
В комплексонометрії застосовують і флуоресцентні індикатори. Молекули цих сполук мають декілька атомів, які здатні бути лігандами, і тому такі речовини можуть утворювати комплекси з йонами металів. Зв’язування йона металу, як правило, супроводжується зміною флуоресценції комплексоутворюючої речовини, при цьому змінюється чи забарвлення, чи інтенсивність флуоресценції. Зміну флуоресценції, так як і зміну забарвлення, можна використати для визначення точки еквівалентності при комплексонометричному титруванні. Флуоресцентні індикатори ще називають металофлуорохромними. Їх зручно застосовувати при титруванні забарвлених розчинів.
Як приклади флуоресцентних індикаторів, що застосовуються в комплексонометрії, можна назвати 8-оксихінолін-5-сульфокислоту, 3-окси-2-нафтойну кислоту; кальцеїн, що є продуктом конденсації флуоресцеїну, формальдегіду і імінодиоцтової кислоти; похідні бензидину та інші.
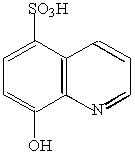 |
| 8-оксихінолін-5-сульфокислота |
Цей індикатор утворює при взаємодії з йонами металів розчинні комплекси, а не осади. Так, у розчині, що містить йони Zn2+ при рН ≈ 10 даний індикатор дає інтенсивну жовто-зелену флуоресценцію, яка зникає в кінцевій точці титрування розчину з йонами Zn2+ розчином ЕДТА.
Кислі розчини 3-окси-2-нафтойної кислоти

мають зелену флуоресценцію, яка у присутності йонів Al3+ переходить у синю. Цей ефект використовують для визначення кінцевої точки титрування йонів Al3+.
За участі індикатора 3-окси-2-нафтойної кислоти можливо роздільно визначати титруванням розчином ЕДТА йони Fe3+ і Al3+ при їх сумісній присутності. При цьому Fe3+ титрують при рН ≈ 2 до зникнення синього забарвлення комплексу Феруму з індикатором, а потім при рН=3 титрують Al3+ до переходу синьої флуоресценції розчину в зелену.
Кальцеїн застосовують переважно для титрування йонів Са2+ у сильнолужному розчині. Точку еквівалентності при цьому визначають за зміною забарвлення розчину від зелено-жовтого до коричневого. Одночасно із зміною забарвлення відбувається зміна флуоресценції, причому зміна флуоресценції відбувається більш інтенсивно, ніж зміна забарвлення. При утворенні комплексів Ca2+, Sr2+, Ba2+ з ЕДТА у присутності кальцеїну флуоресценція індикатора гаситься, що і використовується для визначення кінця титрування.
В інтервалі рН від 4,0 до 10,0 флуоресценція вільного кальцеїну гаситься йонами Cu2+, тому деякі йони металів можливо визначати зворотним титруванням надлишку ЕДТА стандартним розчином Cu2+-іонів, встановлюючи кінцеву точку титрування за гасінням флуоресценції кальцеїну. Таким способом визначають йони Cu2+, Co2+, Cr3+, Mo3+. Можливо також проводити пряме титрування Cu2+-іонів розчином ЕДТА чи поліаміну.
Серед інших флуоресцентних індикаторів слід назвати метилкальцеїн синій
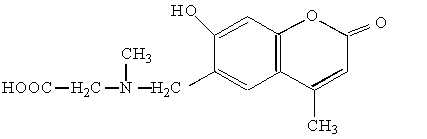
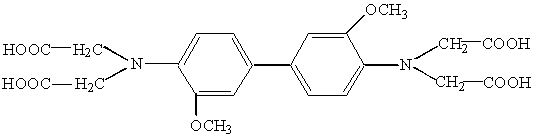
та похідні бензидину, наприклад, о-дианізидинкомплексон:
 .
.
Розчини о-дианізидинкомплексону при рН 4,0–10,0 мають синю флуоресценцію, яка гаситься при внесенні в розчин Cu2+-іонів. Тому за участі цього індикатора можна визначати ряд катіонів методом зворотного титрування надлишку ЕДТА розчином солі Купруму (ІІ).
