Взаимодействие галогенов с водой
Фтор в отличие от других галогенов воду окисляет:
2H2O + 2F2 = 4HF + O2.
Однако при насыщении льда фтором при -40С образуется соединение HFO
(Возможны также реакции: 2HFO = 2HF + O2; HFO + H2O= HF + H2O2,
а при избытке фтора : F2 +HFO = OF2 + HF.)
Можно отметить два типа взаимодействия молекул воды с молекулами галогенов.
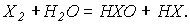
Константы этого равновесия для Х = Cl, Br, I малы , особенно для Х = Br, I , поэтому бром и иод при растворении в воде остаются преимущественно в молекулярной форме Br2 и I2.
Равновесие можно сместить вправо добавлением щелочных реагентов, например, Na2CO3:
Cl2 + Na2CO3 + H2O = NaHCO3 + NaCl + HClO ,
а также добавлением суспензий оксидов ртути (II) или висмута Bi2O3 для перевода в осадок хлорид-ионов:
Cl2 + 2HgO + H2O = HgO . HgСl2 + 2HClO,
2 Cl2 + Bi2O3 + H2O = 2BiOCl + 2HClO.
Приведенные реакции используют для получения HClO, HBrO, HIO.
Скорость реакции сильно зависит от температуры. Так, при действии хлора на эффективно охлаждаемый раствор щелочи образуются гипохлориты, например, жавелевая вода:
2NaOH + Cl2= NaClO + NaCl +H2O.
При взаимодействии же хлора с неохлаждаемым раствором щелочи происходит разогревание раствора и получаются хлораты, например, бертолетова соль KClO3:
6KOH + 3Cl2= KClO3 +5KCl + 3H2O.
Вопрос №10. Подгруппа кислорода, или халькогенов – 6-я группа периодической системы Д.И. Менделле-ва, включающая следующие элементы :
1) кислород – О;
2) сера – S;
3) селен – Se;
4) теллур – Te;
5) полоний – Po (радиоактивный элемент).
Номер группы указывает на максимальную валентность элементов, стоящих в этой группе. Общая электронная формула халькогенов: ns2np4– на внешнем валентном уровне у всех элементов имеется 6 электронов, которые редко отдают и чаще принимают 2 недостающих до завершения уровня электрона. Наличие одинакового валентного уровня обуславливает химическое сходство халькогенов. Характерные степени окисления: -1; -2; 0; +1; +2; +4; +6. Кислород проявляет только -1 – в пероксидах; -2 – в оксидах; 0 – в свободном состоянии; +1 и +2 – во фторидах – О2F2, ОF2 т. к. у него нет d-под-уровня и электроны разъединяться не могут, и валентность всегда – 2; S – все, кроме +1 и -1. У серы появляется d-подуровень и электроны с 3р и с 3s в возбужденном состоянии могут разъединиться и уйти на d-подуровень. В невозбужденном состоянии валентность серы – 2 – в SО, 4 – в SО2, 6 – в SО3. Se +2; +4; +6, Te +4; +6, Po +2; -2. Валентности у селена, теллура и полония также 2, 4, 6. Значения степеней окисления отражены в электронном строении элементов: О – 2s22p4; S – 3s23p4; Se – 4s24p4; Te – 5s25p4; Po – 6s26p4. Сверху вниз, с нарастанием внешнего энергетического уровня закономерно изменяются физические и химические свойства халькогенов: радиус атома элементов увеличивается, энергия ионизации и сродства к электрону, а также электроотрицательность уменьшаются; уменьшаются неметаллические свойства, металлические увеличиваются (кислород, сера, селен, теллур – неметаллы), у полония имеется металлический блеск и электропроводимость. Водородные соединения халькогенов соответствуют формуле: H2R: H2О, H2S, H2Sе, H2Те – хальководороды. Водород в этих соединениях может быть замещен на ионы металлов. Степень окисления всех халькогенов в соединении с водородом -2 и валентность тоже 2. При растворении хальководородов в воде образуются соответствующие кислоты. Эти кислоты – восстановители. Сила этих кислот сверху вниз возрастает, т. к. уменьшается энергия связи и способствует активной диссоциации. Кислородные соединения халькогенов отвечают формуле: RО2 и RО3 – кислотные оксиды. При растворении этих оксидов в воде они образуют соответствующие кислоты: Н2RО3 и Н2RO4. В направлении сверху вниз сила этих кислот убывает. Н2RО3 – кислоты-восстановители, Н2RO4 – окислители.
