ЭДС гальванического элемента, состоящего из медного и цинкового электродов, погруженных в 0,01 М растворы их сульфатов
(Е0Сu2+/Cu=0,34B, Е0Zn2+/Zn=-0,76B) равна___В.
1) 1,10
8) Для вычисления потенциала серебряного электрода в разбавленном растворе серебра с концентрацией CAg+ моль/л используется формула…
1) 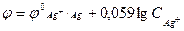
9) Для защиты медных изделий от коррозии в качестве катодного покрытия можно использовать…
1) Ag
10) При частичном восстановлении Сr2O3 образуется…
1) СrO
11) Если при электролизе водного раствора соли значение рН в катодном пространстве возросло, то электролизу подвергался раствор…
1) KCl
12) Эквивалент перманганата калия, если ион MnO4- восстанавливается до Mn+2,равен___ моль
1) 1/5
13) При электролизе раствора, содержащего одинаковые концентрации солей, на катоде в первую очередь будет выделятся…
1) железо
14) В реакции 3Ca + 2P®Ca3P2 атомы фосфора выступают в качестве…
3)окислителей
15) Сумма коэффициентов в уравнении реакции, соответствующая схеме 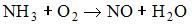 , составляет …
, составляет …
2)19
16) В гальваническом элементе, состоящем из никелевого 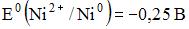 и железного
и железного 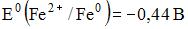 электродов, погруженных в 1 М растворы их солей, на аноде протекает процесс …
электродов, погруженных в 1 М растворы их солей, на аноде протекает процесс …
3) Fe 0 - 2e = Fe2+
17) Уравнение, которое описывает процесс электролиза расплава хлорида натрия в инертной атмосфере, имеет вид …
2) 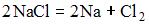
18) Сумма коэффициентов в суммарном уравнении процесса электролиза водного раствора AgNO3 равна…
2) 15
При электролизе раствора хлорида меди (II) на катоде выделилось 2,7 г меди. Объем газа (н.у.), выделившегося на аноде равен _______ л.
1) 4,48
20) При окислении в нейтральной среде KMnO4 восстанавливается с образованием…
1) MnO2
21) Уравнение процесса, протекающего на катоде при электролизе водного раствора КОН, имеет вид…
3) 2 Н2О + 2 ē ® Н2 + 2 ОН-
22) Сумма коэффициентов в левой части уравнения реакции KMnO4 + Na2SO3 + H2SO4®… составляет…
4) 10
23) При прохождении через раствор нитрата серебра количества электричества величиной 48250Кл на катоде образуется ___граммов чистого серебра (F=96500Кл/моль).
2) 54
24) Коэффициент перед молекулой восстановителя в уравнении реакции KMnO4 + Na2SO3 + H2SO4 = MnSO4 + Na2SO4 + K2SO4 + H2O равен.
1) 5
25) Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора хлорида натрия, имеет вид…
1) 2 Н2О - 4ē = О2 + 4 Н+
26) При зарядке свинцового аккумулятора на аноде протекает процесс…
2) PbO2 + 4H+ + SO42- + 2ē ® PbSO4 + 2H2O
27) Окисление азота происходит в процессе, схема которого…
2) NH4+ ® N2
28) Н2S обычно проявляет в окислительно-восстановительных реакциях свойства…
1) Только окислителя
2) Только восстановителя
3) И окислителя, и восстановителя
4) Ни окислителя, ни восстановителя
29) Если гальванический элемент составлен из двух серебряных электродов, один из которых стандартный, то для достижения наибольшего ЭДС другой электрод следует погрузить в раствор AgNO3 c концентрацией
4)0,1 М
30) Металлом, который нельзя получить электролизом водного раствора его соли, является…
2)Na
31) ЭДС гальванического элемента состоящего из железного и серебрянного электродов, погруженных в 0,1 М растворы их нитратов Е0(Fe+2/ Fe)= -0,44 В, Е0(Ag+/ Ag)= 0,80 В, равна_______В.
1) 1,21
2) 1,24
3) – 1,21
4) – 1,24
32) Чтобы получить анодное защитное покрытие, на железо следует нанести слой…
1) Хром
2) Олово
3) Никель
4) Свинец
33) Для получения 54 г серебра электролизом водного раствора нитрата серебра (выход по току 100%), необходимо чтобы в растворе содержалось___граммов чистой соли
2) 85
34) При электролизе водного раствора КСl на инертном аноде выделяется…
3)О2
В реакции
K2Cr2O7 +6KI +7H2SO4=Cr2(SO4)3 + 4K2SO4 +3I2 +7H2O
восстанавливается ион…
1) Н+
2) Сr2O72-
3) I-
4) SO42-
36) При электролизе водного раствора СuCl2 с графитовым анодом на …
1) катоде выделяется водород
2) аноде выделяется кислород
3) аноде выделяется хлор
4) катоде выделяется хлор
37) Oкислительно-восстановительная реакция в стандартных условиях возможна, если…
1) электроотрицательность окислителя выше электроотрицательсности восстановителя
2) стандартный потенциал Е0 восстановителя имеет отрицательное значение
3) значение разности потенциалов полуреакций окисления и восстановления положительно
4) стандартный потенциал Е0 окислителя имеет положительное значение
38) Согласно схеме гальванического элемента Fe|Fe2+||Ni2+|Ni ,…
1) электроны движутся от железного электрода к никелевому
2) никель окисляется
3) никелевый электрод является анодом
4) в процессе работы элемента на электроде осаждается железо
39) В системе, состоящей из луженого (покрытого оловом) железа при нарушении целостности покрытия в морской воде самопроизвольно протекает…
1) восстановление олова
2) окисление олова
3) восстановление железа
4) окисление железа
40) При электролизе водного раствора хлорида натрия на катоде протекает реакция…
1) 2H2O –4e → O2+4H+
2) 2H2O +2e → H2+2OH-
3) Na+ +e→Na
4) 2H++2e→H2
При электролизе воды на аноде выделилось 11,2 л (н.у.) кислорода. Объем водорода, выделившегося на катоде равен ____ л (н.у.)
1)22.4
