Раздел 1. Общая фармацевтическая химия
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «СЕВЕРО-ОСЕТИНСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
(ГБОУ ВПО СОГМА Минздрава России)
___________________________________кафедра фармации ______ _____________________________
Эталоны тестовых заданий по фармацевтической химии для студентов фармацевтического факультета (3-5 курсы).
КУРС, 5 СЕМЕСТР
МОДУЛЬ 1
Раздел 1. Общая фармацевтическая химия.
Трео - и эритро- стереоизомерия связана с наличием в структуре молекулы лекарственного вещества:
| +двух соседних хиральных атомов углерода |
| хирального атома углерода |
| нескольких хиральных атомов углерода |
| вторичного спиртового гидроксила |
| циклогексенового радикала |
Согласно ГФ температура плавления лекарственного вещества соответствует:
| +интервалу температуры между началом и концом плавления |
| появлению первой капли расплавленного вещества |
| полному переходу вещества в расплавленное (жидкое) состояние |
| полному переходу в жидкое состояние и потемнению |
| резкому изменению состояния вещества (вспенивание, потемнение) |
Согласно требованиям ГФ, интервал между началом и концом плавления не должен превышать:
| 0,5оС |
| +2оС |
| 1,5оС |
| 1оС |
| 3оС |
Согласно ГФ под температурой разложения вещества подразумевают:
| полный переход вещества в жидкое состояние |
| интервал температуры между началом и концом плавления |
| расплавление и улетучивание вещества |
| появлением первой капли расплавленного вещества (жидкости) |
| +резкое изменение состояние вещества (вспенивание, потемнение) |
В фармакопейном анализе определение температуры плавления позволяет оценить испытуемое лекарственное вещество по показателю:
| сульфатная зола |
| растворимость |
| влажность |
| количественное содержание |
| +подлинность |
Получение завышенных результатов при определении температуры плавления как правило информирует о:
| завышенной влажности испытуемого вещества |
| степени чистоты испытуемого вещества |
| +несоответствии подлинности испытуемого вещества |
| заниженном количественном содержании испытуемого вещества |
| завышенном содержании испытуемого вещества |
Получение заниженных результатов при определении температуры плавления как правило информирует о:
| завышенном количественном содержании испытуемого вещества |
| завышенной влажности испытуемого вещества |
| заниженном количественном содержании испытуемого вещества |
| несоответствии растворимости испытуемого вещества |
| +завышенном содержании примесей в испытуемом веществе |
Условные термины обозначения растворимости веществ в ГФ подразумевают:
| массу растворенного вещества в моль в 1000 мл растворителя |
| +объем растворителя (мл), необходимый для растворения 1 г вещества |
| массу растворенного вещества (г) в 1 мл растворителя |
| массу растворенного вещества (г) в 100 г растворителя |
| массу растворенного вещества (г) в 100 мл растворителя |
При определении растворимости навеску испытуемого лекарственного вещества отвешивают с точностью до:
| 0,0005 г |
| 0,001 г |
| +0,01 г |
| 0,0002 г |
| 0,005 г |
Согласно ГФ плотностью называют:
| +массу единицы объема вещества |
| объем единицы массы вещества |
| массу 1000 объемов вещества |
| массу 100 объемов вещества |
| объем единицы массы вещества |
Определить плотность жидкости с точностью до 0,001 позволяет использование:
| химического стакана |
| +пикнометра |
| ареометра |
| мерной колбы |
| мерного цилиндра |
Плотность жидкости с точностью до 0,01 определяют с помощью:
| мерного цилиндра |
| +ареометра |
| химического стакана |
| пикнометра |
| мерной колбы |
При потенциометрическом определении рН в качестве индикаторного применяют электрод:
| хлорсеребряный |
| платиновый |
| каломельный |
| +стеклянный |
| ртутный |
При потенциометрическом определении рН в качестве электрода сравнения применяют электрод:
| ртутный |
| +хлорсеребряный |
| стеклянный |
| хингидронный |
| платиновый |
Испытание на примеси, которые в данной концентрации раствора лекарственного вещества «не должны обнаруживаться», проводят сравнением содержимого пробирки:
| с эталонным раствором на определяемую примесь |
| со смесью основных и вспомогательных реактивов, открывающих искомую примесь |
| +с раствором испытуемого лекарственного вещества и вспомогательных реактивов |
| с растворителем, использованным для растворения лекарственного вещества |
| с водой очищенной |
При определении прозрачности жидкости согласно ГФ сравнение проводят с:
| +водой очищенной |
| глицерином |
| эталонами цветности |
| эталонами мутности |
| спиртом этиловым |
Согласно ГФ степень мутности растворов определяют визуально путем сравнения с:
| раствором гидразина сульфата в воде |
| раствором гексаметилентетрамина в воде |
| растворителем, взятым для приготовления раствора |
| водой очищенной |
| +эталонными растворами |
Окраску растворов определяют визуально путем сравнения с:
| исходными растворами |
| водой очищенной |
| растворителем, использованным для приготовления раствора |
| +эталонами цветности |
| стандартными растворами |
Бесцветными считают растворы, которые по цвету не отличаются от:
| эталонных растворов |
| воды очищенной |
| исходных растворов окраски |
| стандартных растворов окраски |
| +растворителя, использованного для приготовления раствора |
Бюкс с навеской вещества при определении потери в массе при высушивании помещают:
| в муфельную печь с открытой крышкой |
| не имеет значения |
| в муфельную печь с закрытой крышкой |
| +в сушильный шкаф с открытой крышкой |
| в сушильный шкаф с закрытой крышкой |
В лекарственных веществах с помощью титрования реактивом К. Фишера может быть определена вода:
| +как гигроскопическая, так и кристаллизационная |
| только кристаллизационная |
| только гигроскопическая |
| не реагирующая с компонентами реактива К. Фишера |
| реагирующая с любым компонентом реактива К. Фишера |
Содержание золы, нерастворимой в хлороводородной кислоте, в основном показывает содержание в лекарственном растительном сырье:
| органических примесей |
| общее количество неорганических веществ |
| солей тяжелых металлов |
| +солей или оксидов кремния (силикатов) |
| солей железа |
Содержание сульфатной золы показывает загрязненность органических лекарственных веществ:
| солями или оксидами кремния (силикатами) |
| солями меди, железа |
| промежуточными продуктами синтеза органического вещества |
| +солями тяжелых металлов |
| продуктами разложения органического вещества |
Содержание общей золы в основном показывает содержание в лекарственном растительном сырье:
| силикатов |
| органических примесей |
| избыточной влажности |
| +минеральных веществ |
| частей других растений |
Примесь хлорид-ионов в лекарственных веществах согласно ГФ обнаруживают:
| раствором нитрата серебра в присутствии раствора аммиака |
| реактивом Несслера |
| раствором нитрата серебра |
| раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
| +раствором нитрата серебра в присутствии азотной кислоты |
Примесь сульфат-ионов в лекарственных веществах согласно ГФ обнаруживают:
| раствором нитрата серебра в присутствии азотной кислоты |
| раствором ферроцианида калия в присутствии хлороводородной кислоты |
| раствором хлорида бария в присутствии уксусной кислоты |
| раствором сульфосалициловой кислоты в присутствии раствора аммиака |
| +раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
Примесь солей аммония в лекарственных веществах согласно ГФ обнаруживают:
| раствором нитрата серебра |
| раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
| раствором ферроцианида калия в присутствии хлороводородной кислоты |
| +реактивом Несслера |
| раствором оксалата аммония в присутствии растворов хлорида аммония и аммиака |
Примесь солей кальция в лекарственных веществах согласно ГФ обнаруживают:
| раствором серебра нитрата в присутствии азотной кислоты |
| раствором сульфида натрия в присутствии разведенной уксусной кислоты |
| раствором кислоты сульфосалициловой |
| +раствором оксалата аммония в присутствии растворов хлорида аммония и аммиака |
| раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
Примесь солей тяжелых металлов в лекарственных веществах согласно ГФ обнаруживают:
| +раствором сульфида натрия в присутствии разведенной уксусной кислоты |
| раствором кислоты сульфосалициловой |
| раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
| раствором ферроцианида калия в присутствии хлороводородной кислоты |
| раствором оксалата аммония в присутствии растворов хлорида аммония и аммиака |
Примесь солей железа в лекарственных веществах согласно ГФ обнаруживают:
| раствором сульфида натрия в уксуснокислой среде |
| раствором оксалата аммония в присутствии растворов хлорида аммония и аммиака |
| +раствором сульфосалициловой кислоты в присутствии раствора аммиака |
| раствором хлорида бария в присутствии разведенной хлороводородной кислоты |
| раствором ферроцианида калия в присутствии хлороводородной кислоты |
Согласно требованиям ГФ, при испытаниях на чистоту и допустимые пределы примесей вода и все реактивы должны быть:
| свободны от кислорода воздуха |
| иметь нейтральную реакцию среды |
| +свободны от ионов, на содержание которых проводят испытания |
| бесцветны |
| свободны от углекислоты |
При определении примесей хлоридов, сульфатов, кальция, железа эталонным и безэталонным способами сравнение результатов реакции в обеих пробах проводят после добавления соответствующего реактива:
| сразу |
| через 5 минут |
| через 10 минут |
| через 1 минуту |
| +через промежуток времени, указанный в ОФС на искомую примесь |
Для идентификации лекарственных веществ, имеющих в структуре молекулы асимметрический атом углерода, используют показатель:
| показатель преломления |
| температуру плавления |
| плотность |
| удельный показатель поглощения |
| +удельное вращение |
Укажите функциональную группу в структуре молекулы лекарственного вещества, позволяющую использовать для его идентификации реакцию гидроксамовой пробы:
| третичная аминогруппа |
| спиртовый гидроксил |
| первичная алифатическая аминогруппа |
| фенольный гидроксил |
| +сложноэфирная |
Для идентификации лекарственных веществ, имеющих в структуре молекулы альдегидную группу, проводят реакции:
| с реактивом Несслера |
| образования оснований Шиффа с аминами |
| «медного зеркала» |
| «серебряного зеркала» |
| +все перечисленные |
Поляриметрия может быть использована для подтверждения подлинности лекарственных веществ, содержащих в структуре:
| +асимметрический атом углерода |
| атомы галогенов |
| спиртовый гидроксил |
| сложноэфирную группу |
| хромофорные группы |
Адсорбционные индикаторы применяют в методах количественного анализа:
| +аргентометрия |
| комплексонометрия |
| кислотно-основное титрование в водных средах |
| броматометрия (прямая и обратная) |
| кислотно-основное титрование в неводных средах |
Методом прямой комплексонометрии проводят количественное определение следующих лекарственных веществ, кроме:
| кальция хлорида |
| магния сульфата |
| серебра нитрата |
| +цинка оксида |
| висмута нитрата основного |
Укажите реакцию среды, необходимую для повышения воспроизводимости результатов при количественном определении лекарственных веществ производных первичных ароматических аминов методом нитритометрии:
| щелочная |
| нейтральная |
| +кислая |
| не имеет значения |
| сильно-щелочная |
Количественное определение методом нитритометрии обусловливает наличие в структуре лекарственного вещества:
| спиртового гидроксила |
| +первичной ароматической аминогруппы |
| карбоксильной группы |
| альдегидной группы |
| фенольного гидроксила |
В аргентометрии (метод Мора) в качестве индикатора используют:
| флюоресцеин |
| эриохром черный |
| избыток титранта |
| фенолфталеин |
| +хромат калия |
Реакция среды при количественном определении солей галогенводородных кислот по методу Мора должна быть:
| +близкая к нейтральной |
| уксуснокислая |
| щелочная |
| солянокислая |
| азотнокислая |
В методе прямой перманганатометрии в точке конца титрования появляется окрашивание, обусловленное избытком титранта:
| зеленое |
| бурое |
| +розовое |
| синее |
| желтое |
Метод УФ спектрофотометрии используют для идентификации и количественного определения лекарственных веществ, содержащих:
| неионогенные галогены |
| +хромофорные группы |
| асимметрические атомы углерода |
| спиртовой гидроксил |
| карбоксильную группу |
При нитритометрическом количественном определении лекарственных веществ в случае образования окрашенных солей диазония в качестве индикатора можно использовать:
| +иодкрахмальную бумагу |
| метиленовый синий |
| тропеолин 00 |
| метиловый оранжевый |
| нейтральный красный |
Минерализацию образца при анализе методом Кьельдаля осуществляют в присутствии:
| +кислоты серной концентрированной и смеси сульфатов калия и меди |
| кислоты хлороводородной |
| калия перманганата |
| кислоты фосфорной концентрированной |
| кислоты хлороводородной и меди сульфата |
При алкалиметрическом титровании с индикатором фенолфталеином окраска титруемого раствора меняется:
| от ярко-розовой до желтой |
| от бесцветной до желтой |
| +от бесцветной до ярко-розовой |
| от ярко-розовой до бесцветной |
| от бесцветной до голубой |
При меркуриметрическом титровании используют индикатор:
| +дифенилкарбазид |
| метиловый оранжевый |
| хромат калия |
| эозионат натрия |
| железоаммониевые квасцы |
Цериметрическое определение основано на реакциях:
| осаждения |
| гидролиза |
| +окисления-восстановления |
| комплексообразования |
| нейтрализации |
Индикатором в цериметрическом методе анализа служит:
| фенолфталеин |
| метиловый оранжевый |
| хромат калия |
| крахмал |
| +о-фенантролин |
Адсорбционные индикаторы применяются в методе количественного определения:
| нитритометрии |
| броматометрии (прямая и обратная) |
| меркуриметрии |
| +аргентометрии |
| комплексонометрии |
Аргентометрический метод используют для определения:
| веществ, содержащих третичную аминогруппу |
| веществ, содержащих первичную ароматическую аминогруппу |
| веществ, содержащих спиртовый гидроксил |
| +галогенидов щелочных металлов |
| фенолов |
Для определения точки эквивалентности методом кислотно-основного титрования в среде ледяной уксусной кислоты используют индикатор:
| фенолфталеин |
| метиловый оранжевый |
| тропеолин 00 |
| +кристаллический фиолетовый |
| бромтимоловый синий |
Метод рефрактометрии основан на измерении:
| угла вращения плоскости поляризованного луча света |
| поглощения излучения |
| адсорбции |
| +показателя преломления растворов |
| светопоглощения |
Метод рефрактометрии можно использовать для анализа лекарственных веществ в:
| +30% растворах |
| 0,001% растворах |
| 0,1% растворах |
| 0,05% растворах |
| 0,01% растворах |
Фактор преломления раствора вещества показывает увеличение показателя преломления при увеличении концентрации вещества на:
| 15% |
| 8% |
| 10% |
| +1% |
| 25% |
При поляриметрическом определении измеряют:
| степень поглощения УФ излучения |
| +угол вращения поляризованного луча света |
| показатель преломления |
| поглощение излучения в ИК области спектра |
| поглощение излучения в видимой области спектра |
Фотоколориметрическое определение окрашенных растворов проводят в области оптического спектра:
| 1000-2000 нм |
| 190-380 нм |
| 780-1000 нм |
| 2000-4000 нм |
| +380-780 нм |
Фотоколориметрический метод можно использовать для количественного определения окрашенного соединения:
 |
+ 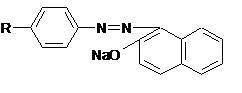 |
 |
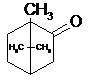 |
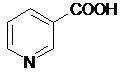 |
Спектрофотометрическое количественное определение основано на измерении:
| степени рассеяния света растворами веществ |
| +оптической плотности растворов лекарственных веществ |
| степени отражения |
| показателя преломления |
| угла вращения |
Количественное содержание вещества, определяемое спектрофотометрическим методом, рассчитывают с помощью:
| показателя преломления |
| +удельного показателя поглощения |
| рН среды |
| измерения силы тока |
| угла вращения |
Величина оптической плотности прямо пропорциональна:
| величине атмосферного давления |
| температуре окружающей среды |
| +концентрации исследуемого раствора |
| длине волны |
| молярной массе растворенного вещества |
Флуориметрия - метод фотометрического анализа, основанный на измерении:
| угла вращения |
| показателя преломления |
| +интенсивности флюоресценции |
| светорассеяния взвешенными частицами испытуемых веществ |
| оптической плотности |
Метод тонкослойной хроматографии используется со следующими целями, кроме:
| количественного анализа |
| +установления структуры |
| разделения веществ смеси |
| идентификации веществ |
| обнаружения примесей |
Количественное содержание компонента смеси при использовании метода ГЖХ рассчитывают по:
| показателю светопоглощения |
| значению Rf |
| значению Rs |
| времени удерживания |
| +площади пика |
Высокоэффективная жидкостная хроматография является вариантом:
| +колоночной жидкостной хроматографии |
| колоночной газовой хроматографии |
| тонкослойной хроматографии |
| радиальной хроматографии |
| бумажной хроматографии |
На измерении поглощения электромагнитного излучения основан метод:
| флуориметрии |
| +УФ спектрофотометрии |
| поляриметрии |
| хроматографии |
| рефрактометрии |
Отличие УФ спектрофотометрии от фотоколориметрии заключается в:
| зависимости светопоглощения от толщины слоя раствора |
| зависимости светопоглощения от концентрации вещества |
| +используемой области оптического спектра |
| зависимости светопоглощения от величины коэффициента светопоглощения |
| способах расчета концентрации вещества |
Фотоколориметрический метод основан на измерении интенсивности окраски следующих продуктов реакции, кроме:
| ауринового красителя |
| азокрасителя |
| гидроксамата железа |
| индофенолового красителя |
| +осадка с реактивом Драгендорфа |
Формула для расчета концентрации раствора применяется при использовании метода:
| +рефрактометрии |
| тонкослойной хроматографии |
| полярографии |
| спектрографии |
| поляриметрии |
Удельный показатель поглощения - это:
| оптическая плотность 1 М раствора |
| +оптическая плотность 1% раствора при толщине поглощающего слоя 1 см |
| показатель преломления раствора |
| величина удельного вращения |
| величина Rf |
Спектрофотометрический метод можно использовать для анализа лекарственных веществ, содержащих следующие хромофорные группы, кроме:
| -N=N- |
| -CH=N- |
| -CH=CH- |
| + -OH |
| -N=O |
При расчете величины удельного вращения поляриметрическим методом длина кюветы измеряется в:
| мкм |
| мм |
| м |
| см |
| +дм |
Расчеты содержания вещества в спектрофотометрическом методе анализа проводят следующими способами, кроме:
| по градуировочному графику |
| по уравнению градуировочного графика |
| по раствору стандартного образца |
| +по значению показателя преломления |
| по удельному показателю светопоглощения |
Величина Rf используется для:
| +подтверждения подлинности |
| определения примесей сульфатов |
| установления структуры |
| количественного определения |
| определения примесей хлоридов |
При изучении фармацевтической химии лекарственные вещества рассматриваются в соответствии с:
+химической классификацией;
фармакотерапевтической классификацией;
фармакологической классификацией;
анатомической классификацией.
Примесь хлорид-ионов в фармацевтических субстанциях обнаруживают с помощью:
+раствора серебра нитрата;
раствора бария хлорида;
раствора калия ферроцианида;
щелочного раствора калия тетрайодомеркурата(II) (реактив Несслера).
Примесь сульфат-ионов в фармацевтических субстанциях обнаруживают с помощью:
+раствора бария хлорида;
раствора серебра нитрата;
раствора натрия сульфида;
щелочного раствора калия тетрайодомеркурата(II) (реактив Несслера).
Примесь ионов аммония в фармацевтических субстанциях обнаруживают с помощью:
+щелочного раствора калия тетрайодомеркурата(II) (реактив Несслера);
раствора аммония оксалата;
раствора серебра нитрата;
раствора калия ферроцианида.
Примесь солей кальция в фармацевтических субстанциях обнаруживают с помощью:
+раствора аммония оксалата;
раствора бария хлорида;
щелочного раствора калия тетрайодомеркурата(II) (реактив Несслера);
раствора серебра нитрата.
Примесь солей цинка в фармацевтических субстанциях обнаруживают с помощью:
+раствора калия ферроцианида;
раствора бария хлорида;
раствора серебра нитрата;
раствора аммония оксалата.
Примесь солей железа в фармацевтических субстанциях обнаруживают с помощью:
+раствора сульфосалициловой кислоты;
раствора бария хлорида;
раствора аммония оксалата;
раствора серебра нитрата.
Примесь тяжелых металлов в фармацевтических субстанциях обнаруживают с помощью:
+раствора натрия сульфида;
раствора аммония оксалата;
раствора сульфосалициловой кислоты;
раствора серебра нитрата.
Примесь мышьяка в фармацевтических субстанциях обнаруживают по окрашиванию в желто-бурый цвет:
+бумаги, пропитанной раствором ртути(II) хлорида;
куркумовой бумаги;
йодкрахмальной бумаги;
синей лакмусовой бумаги.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре кетонную группу, можно использовать реакцию:
+образования гидразонов;
образования азокрасителя;
образования "серебрянного зеркала";
образования йодоформа.
С помощью реакции образования "серебрянного зеркала" можно подтвердить подлинность лекарственных веществ содержащих в химической структуре:
+гидроксиацетильную (α-кетольную) группу;
карбоксильную группу;
кетонную группу;
сложноэфирную группу.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре сложноэфирную группу, можно использовать:
+гидроксамовую пробу;
реакцию образования "серебрянного зеркала";
нингидриновую пробу;
реакцию образования азокрасителя.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре простую эфирную группу, можно использовать реакцию:
+образования оксониевых солей;
образования оснований Шиффа;
с реактивом Фелинга;
образования гидразонов.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре карбоксильную группу, можно использовать реакцию:
+этерификации;
образования "серебрянного зеркала";
образования азокрасителя;
гидролиза.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре сложноэфирную группу, можно использовать реакцию:
+гидролиза;
этерификации;
с нингидрином;
с реактивом Фелинга.
С помощью реакции образования "серебрянного зеркала" можно подтвердить подлинность лекарственных веществ содержащих в химической структуре:
+гидразидную группу;
карбоксильную группу;
кетонную группу;
простую эфирную группу.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре первичную ароматическую аминогруппу, используют реакцию:
+образования азокрасителя;
этерификации;
гидролиза;
образования "серебрянного зеркала".
При выполнении реакции образования азокрасителя используют реактивы:
+натрия нитрит, хлористоводородную кислоту, щелочной раствор β-нафтола;
натрия нитрат, хлористоводородную кислоту, щелочной раствор β-нафтола;
серебра нитрат, раствор формальдегида, раствор аммиака;
n-диметиламинобензальдегид в среде хлористоводородной кислоты.
Для подтверждения подлинности лекарственных веществ, содержащих в химической структуре третичную аминогруппу (третичный атом азота), используют реакцию:
+с реактивом Драгендорфа;
с реактивом Фелинга;
с диазореактивом;
образования "серебрянного зеркала".
Для количественного определения всех перечисленных лекарственных веществ (натрия бромид, кальция хлорид, прокаина гидрохлорид) может быть использован метод:
+аргентометрии;
комплексонометрии;
ацидиметрии;
алкалиметрии.
К методам окислительно-восстановительного титрования относится:
+йодометрия;
алкалиметрия;
ацидиметрия;
комплексонометрия.
МОДУЛЬ 2
