Растворы, механические смеси и химические соединения
Однородность растворов делает их очень сходными с химическими соединениями.
Химическое соединение — сложное вещество, состоящее из химически связанных атомов двух или нескольких элементов.
Раствор это не одно химическое соединение, а как минимум два смешанных соединения. В отличие от простого смешивания веществ, при растворении происходит взаимодействие между частицами, образующими раствор.
Выделение теплоты при растворении некоторых веществ тоже указывает на химическое взаимодействие между растворителем и растворяемым веществом.
Отличие растворов от химических соединений состоит в том, что состав раствора может изменяться в широких пределах. Кроме того, в свойствах раствора можно обнаружить многие свойства его отдельных компонентов, чего не наблюдается в случае химического соединения.
Непостоянство состава растворов приближает их к механическим смесям.
Механическая смесь — физико-химическая система, в состав которой входят два или несколько химических соединений (компонентов). В смеси исходные вещества включены неизменными. При смешивании не возникает никакое новое вещество.
От механических смесей растворы резко отличаются своею однородностью. Таким образом, растворы занимают промежуточное положение между механическими смесями и химическими соединениями.
Процесс растворения
Растворение кристалла в жидкости протекает следующим образом.
Когда вносят кристалл в жидкость, в которой он может растворяться, от поверхности его отрываются отдельные молекулы. Последние благодаря диффузии равномерно распределяются по всему объёму растворителя.
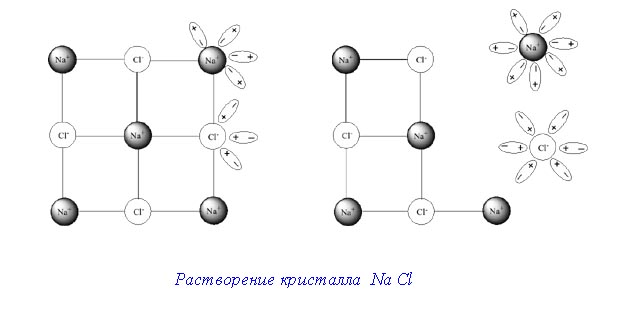
Отделение молекул от поверхности твёрдого тела вызывается, с одной стороны, их собственным колебательным движением, а сдругой – притяжением со стороны молекул растворителя.
Этот процесс должен был бы продолжаться до полного до полного растворения любого количества кристаллов, если бы не происходил обратный процесс – кристаллизация. Перешедшие в раствор молекулы, ударяясь о поверхность ещё не растворившегося вещества, снова притягиваются к нему и входят в состав его кристаллов.
Понятно, что выделение молекул из раствора будет идти тем быстрее, чем большеконцентрация раствора. А так как последняя по мере растворения вещества увеличивается, то, наконец наступает такой момент, когда скорость растворения становится равной скорости кристаллизации. Тогда устанавливаетсядинамическое равновесие, при котором в единицу времени растворяется и кристаллизуется одинаковое число молекул.

Раствор, находящийся в равновесии с растворяющимся веществом, называетсянасыщенным раствором.
Концентрация растворов
Насыщенными растворами приходится пользоваться сравнительно редко. В большинстве случаев употребляются растворы ненасыщенные, т.е. с меньшей концентрацией растворённого вещества, чем в насыщенном растворе.
Концентрацией раствора называется количество растворённого вещества, содержащееся в определённом количестве раствора или растворителя.
Растворы с большой концентрацией растворённого вещества называютсяконцентрированными, с малой – разбавленными.
Концентрацию раствора можно выражать по разному:
1. В процентах растворённого вещества по отношению ко всему количеству раствора.
2. Числом грам-молекул растворённого вещества, содержащегося в 1 литре раствора.
3. Числом грамм-молекул растворённого вещества, содержащегося в 1000 г растворителя
и т.д.
Растворимость
Растворимостью называется способность вещества растворяться в том или ином растворителе.
Мерой растворимости вещества при данных условиях служит концентрация его насыщенного раствора.
Растворимость различных веществ колеблется в широких пределах.
· Если в 100 граммах воды растворяется более 10 г вещества, то такое вещество
принято называть хорошо растворимым.
· Если растворяется менее 1 г вещества – малорастворимым.
· Если в раствор переходит менее 0,01 г вещества, то такое вещество называют
практически нерастворимым.
Принципы, позволяющие предсказать растворимость вещества, пока не известны. Однако, обычно вещества, состоящие из полярных молекул, и вещества с ионным типам связи лучше растворяются в полярных растворителях (вода, спиры, жидкий амиак), а неполярные вещества – в неполярных растворителях (бензол, сероуглерод).
Растворение большинства твёрдых тел сопровождается поглощением теплоты. Это объясняется затратой значительного количества энергии на разрушение кристаллической решётки твёрдого тела, что обычно не полностью компенсируется энергией, выделяющейся при образовании гидратов (сольватов).
Как правило, повышение температуры должно приводить к увеличению растворимости твёрдых тел.
Гидраты и сольваты.
При растворении многих веществ их молекулы или ионы связываются с молекулами растворителя, образуя соединения, называемые сольватами (от латинского solvere – растворять). Этот процесс называется сольватацией.
В частном случае, когда растворителем является вода, эти соединения называютсягидратами, а самый процесс их образования – гидратацией.
В зависимости от природы растворённого вещества, сольваты могут образовываться разными путями.
1. При растворении веществ с ионной структурой молекулы растворителя удерживаются около иона силами электростатического притяжения. В этом случае говорят о ион-дипольном взаимодействии.
2. Может иметь место донорно-акцепторное взаимодействие. Здесь ионы растворённого вещества обычно выступают в качестве акцепторов, а молекулы растворителя – в качестве доноров электронных пар. В таком взаимодействии могут участвовать растворители, молекулы которых обладают неподеленными электронными парами (например, вода, аммиак).
3. При растворении веществ с молекулярной структурой сольваты образуются вследствие диполь-дипольного взаимодействия. Диполи растворённого вщества могут быть при этом постоянными (у веществ с полярными молекулами) или наведёнными (у веществ с неполярными молекулами).
Кристаллогидраты
Вещества, в кристаллы которых входят молекулы воды, называютсякристаллогидратами, а содержащаяся в них вода – кристаллизационной.
Состав кристаллогидратов принято изображать формулами, показывающими, какое количество кристаллизационной воды содержит кристаллогидрат.
Примеры:
· кристаллогидрат сульфата меди (медный купорос), содержащий одну грамм-
молекулу CuSO4 и пять грамм-молекул воды, изображается формулой
CuSO4 · 5 H2O;
· кристаллогидрат сульфата натрия (глауберова соль) изображается формулой
Na2SO4 · 10H2O.
· Алюмокалиевые квасцы могут изображаться формулой:
K2SO4 · Al2(SO4)3 · 24H2O или после сокращения на два: KAl(SO4)2 · 12H2O
Свойства гидратов
Гидраты, как правило, нестойкие соединения, во многих случаях разлагающиеся уже при выпаривании растворов.
Но иногда гидраты настолько прочны, что при выделении растворённого вещества из раствора вода входит в состав его кристаллов.
Прочность связи между веществом и кристаллизационной водой в кристаллогидратах различна. Многие из них теряют кристаллизационную воду уже при комнатной температуре.
Так, прозрачные кристаллы «бельевой» соды (Na2СO3 · 10H2O), если оставить их лежать на воздухе, очень легко «выветриваются», т.е., теряя воду, становятся тусклыми и постепенно рассыпаются в порошок. Для обезвоживания других кристаллогидратов требуется довольно сильное нагревание.
