С одним и двумя гетероатомами. 1. Напишите структурные формулы и назовите соединения, образующиеся из бензола, если в его молекуле заменить: а) одну метиновую группировку −СН= на атом
1. Напишите структурные формулы и назовите соединения, образующиеся из бензола, если в его молекуле заменить: а) одну метиновую группировку −СН= на атом азота; б) две метиновых группировки −СН=, стоящие в положениях 1 и 3, на два атома азота; в) группировку −СН=СН− на атом серы;
г) группировку −СН=СН−СН= на два атома азота.
2. Какие виды таутомерии возможны для азотистых гетероциклических соединений, содержащих в кольце оксигруппировки?
3. Приведите формулы и назовите гетероциклические соединения, отличающиеся по размеру цикла, количеству и характеру гетероатомов.
4. Напишите структурные формулы следующих соединений:
а) 2,4-диметилтиофена; б) 2,3-диметил-4-этилпиррола; в) тетрагидрофурана; г) скатола; д) пирролина; е) фурфурола; ж) пирослизевой кислоты.
5. Приведите общую схему и укажите условия получения производных фурана, пиррола и тиофена из 1,4-дикарбонильных соединений алифатического ряда.
6. Напишите схему взаимного превращения фурана, пиррола и тиофена по Ю. К. Юрьеву и укажите условия реакций.
7. В каком валентном состоянии находятся все атомы в молекулах фурана, пиррола и тиофена? Объясните, как формируется s-скелет и p-электронный секстет в этих соединениях. Покажите направление электронных смещений в молекуле пиррола.
8. Какие факторы оказывают влияние на величину и направленность дипольных моментов? Объясните разницу этих значений для фурана, пиррола, тиофена (0,7D,1,8D,1,9D соответственно) и для полностью восстановленных их аналогов (1,7D, 1,6D и 0,5D соответственно).
9. Назовите следующие соединения:
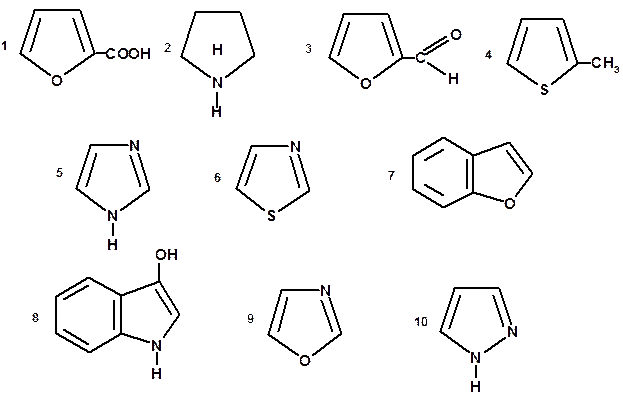
10. Приведите предельные структуры и мезоформулу пиррола. Какие химические свойства следует ожидать для этого соединения? Какова будет ориентация в реакциях замещения? Сравните реакционную способность пиррола и бензола.
11. Пятичленные гетероциклические соединения c одним гетероатомом относятся к электроноизбыточным системам. Чем это объясняется и как это сказывается на условиях протекания SN- и SE-реакций (сравните с бензолом)?
12. Из пиррола получите пирролидин, объясните разницу в их основных свойствах.
13. Расположите в ряд по степени уменьшения реакционной способности в реакциях электрофильного замещения следующие соединения: фуран, пиррол, тиофен, бензол, нитробензол, фенол.
14. Как будут влиять электронодонорные и электроноакцепторные заместители на реакционную способность пятичленных гетероциклов с электрофильными реагентами? Сравните реакционную способность пирослизевой кислоты, фурана и 2-этилфурана.
15. Напишите уравнения реакций пиррола с пиридинсульфотриоксидом, ацетилнитратом и уксусным ангидридом (в присутствии кислоты Льюиса).
16. Очистку бензола от серусодержащих примесей (тиофена) производят при помощи 90%-й серной кислоты. Поясните причину использования данного реагента.
17. В чем причина ацидофобности и как она изменяется в ряду пятичленных гетероциклических соединений с одним гетероатомом?
18. Куда присоединяется протон при взаимодействии пиррола с соляной кислотой? Напишите уравнение реакции. Чем объясняется легкость полимеризации фурана и пиррола при взаимодействии с кислотами?
19. Какое сульфирующее средство (дымящую серную кислоту, 85%-ю серную кислоту или комплекс пиридина с серным ангидридом) необходимо использовать для моносульфирования: пиррола, тиофена, бензола, фурана?
20. Для какого пятичленного гетероцикла (фурана, пиррола или тиофена) наиболее выражены свойства диенового углеводорода с сопряженными двойными связями? Поясните ответ.
21. Напишите структурные формулы промежуточных и конечных продуктов в следующих схемах:

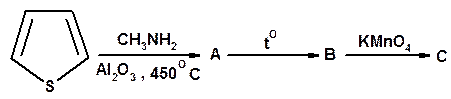
22. Приведите структурные формулы следующих соединений:
а) β-метилиндола (скатола); б) β-индолилуксусной кислоты (гетероауксина); в) 3-оксииндола (индоксила); г) триптофана.
23. Осуществите цепи превращений и назовите промежуточные и конечные продукты реакций:

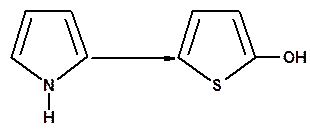
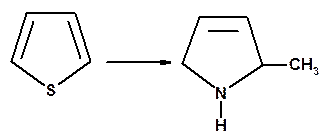
24. Напишите структурные формулы следующих азолов: а) тиазола; б) пиразола; в) оксазола; г) имидазола.
25. Имидазол значительно более сильное основание, чем пиррол и пиридин. Чем это можно объяснить?
26. Схематично изобразите для молекулы имидазола расположение в пространстве орбиталей обоих атомов азота. Наличие в цикле второго гетероатома с «внешней» неподеленной парой электронов придает имидазолу ряд специфических свойств. Каковы они? Приведите примеры.
27. Составьте схему образования водородных связей между молекулами пиразола (димер) и имидазола (олигомер).
