Реактор идеального смешения непрерывного действия
· реактор идеального смешения непрерывного действия с политермическим тепловым режимом (РИС-Н-П)
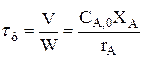 ; (3.15)
; (3.15)
При изменении объема реакционной среды:
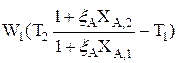 =
= 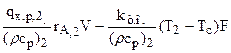 ; (3.16)
; (3.16)
· реактор идеального смешения непрерывного действия с изотермическим тепловым режимом (РИС-Н-И)
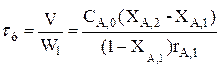 , (3.17)
, (3.17)
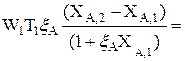
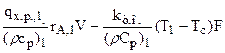 (3.18)
(3.18)
· реактор идеального смешения непрерывного действия с адиабатическим тепловым режимом (РИС-Н-А)
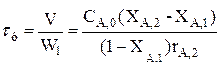 ; (3.19)
; (3.19)
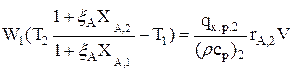 (3.20)
(3.20)
Реактор идеального смешения периодического действия
· реактор идеального смешения периодического действия с политермическим тепловым режимом (РИС-П-П)
tд=tу=t, (3.21)
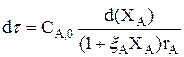 (3.22)
(3.22)
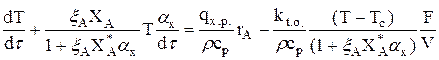 (3.20)
(3.20)
· реактор идеального смешения периодического действия с изотермическим тепловым режимом (РИС-П-И)
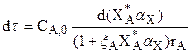 ; (3.21)
; (3.21)
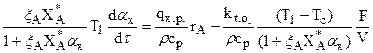 (3.22)
(3.22)
· реактор идеального смешения периодического действия с адиабатическим тепловым режимом (РИС-П-А)
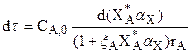 ; (3.23)
; (3.23)
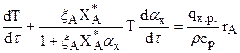 (3.24)
(3.24)
Реактор идеального вытеснения
· реактор идеального вытеснения с политермическим тепловым режимом:
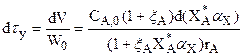 (3.25)
(3.25)
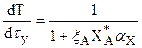
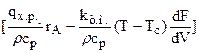 ; (3.26)
; (3.26)
· реактор идеального вытеснения с изотермическим тепловым режимом:
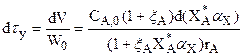 (3.27)
(3.27)
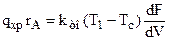 (3.28)
(3.28)
· реактор идеального вытеснения с адиабатическим тепловым режимом:
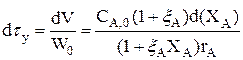 (3.29)
(3.29)
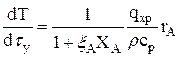 (3.30)
(3.30)
Приведенные модели описывают стационарные режимы работы РИС-Н и РИВ и нестационарные режимы РИС-П.
При выборе изотермического режима следует учитывать, что для его реализации в РИС-П и РИВ необходимо организовать переменный во времени (для РИС-П) и в пространстве (для РИВ) теплообмен с внешней средой.
Для РИС-П время пребывания не связано с объемом V и расходами W1 и W2 - здесь эти величины определяют время загрузки и выгрузки реакционной смеси:
tзагр.= V/W1 и tвыгр.= V/W2. (3.31)
Характеристическое уравнение РИС-П дает «чистое» время реакции, необходимое для достижения заданной степени превращения реагентов (ХА,2). При x=0:
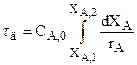 . (3.32)
. (3.32)
Чтобы определить объем такого реактора, кроме концентрации СА,0, ХА,1 и ХА,2 задают еще и количество продукта NR, которое требуется получить за один цикл:
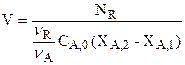 . (3.33)
. (3.33)
Производительность РИС-П, кмоль/ч:
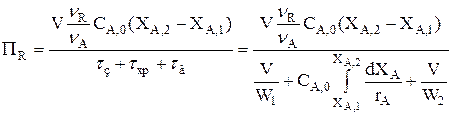 . (3.34)
. (3.34)
Примеры решения задач
Задача 1
Найти объем РИВ-И, необходимый для достижения степени превращения ХА,1 = 0,85 для реакции А® R с константой скорости k = 0,45 мин-1. Объемный расход потока на входе W0=32 л/мин при СА,0= 1 моль/л.
Решение
1.Характеристическое уравнение 
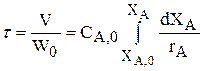
2.Кинетическое уравнение: rA=kCA,0(1-XA);
3. 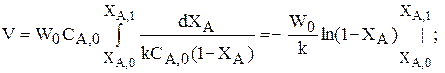
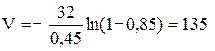 л.
л.
Задача 2
Найти объем РИС-Н, необходимый для достижения степени превращения ХА,1 = 0,85 для реакции А ® R с константой скорости k = 0,45 мин-1. Объемный расход потока на входе W0 = 32 л/мин при СA,0 = 1 моль/л.
Решение
1. Характеристическое уравнение 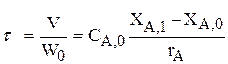
2. Кинетическое уравнение: rA=kCA,0(1-XA,1);
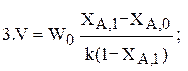
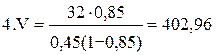 (л).
(л).
Задача 3
Найти объем двухступенчатого каскада К-РИС-И, необходимый для достижения в первой ступени ХА,1 = 0,55 и во второй ХА,2 = 0,85 для реакции А ® R с константами скоростей k1 = k2=0,45 мин-1 . Объемный расход потока на входе W0 = 32 л/мин при СА,0= 1 моль/л.
Решение
1. Модель 1-й ступени: t1 =CA,0(XA,1-XA,0)/rА,1;
2. модель 2-й ступени: t2 =CA,0(XA,2-XA,1)/r А,2.
3. Учитывая, что rA,1=k1CA,0(1-XA,1) и rA,2=k2CA,0(1-XA,2), запишем модель К-РИС:
t = t1+t2 = 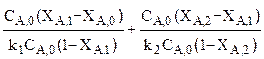
4. Выразим объем К- РИС этого уравнения при ХА,0=0:
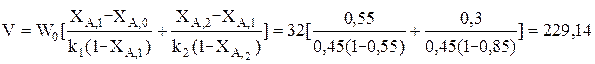 (л)
(л)
Задача 4
Определить конечную температуру Т2 и степень превращения ХА,2, которые могут быть достигнуты в РИС-Н-А для реакции А ® R+Q.
Условия проведения ХТП:
- объем реакционного пространства V=1 м3; V = 1 м3;
- расход реакционной смеси W0 = 0,25 м3/мин; W=WН=WК = 0,25 м3/мин;
- температура потока на входе Т1= 300 К; ТН = 300 оК;
- начальная концентрация компонента А СА,0=2 кмоль/м3; САН = 2 кмоль/м3;
- начальная степень превращения ХА,0=0; ХАН = 0;
- теплота химической реакции qxp=40000 кДж/кмоль; qХ.Р. = -40000 кДж/кмоль;
- удельная теплоемкость реакционной смеси ср=0,8 кДж/кг К; СР=СРК=СРН = 0,8 кДж/(кгЧоК);
- плотность реакционной смеси r=1110 кг/м3;
- константа скорости реакции при Т2 k=0,5 мин-1;
Решение
Используя приведенные выше соотношения, получим:
V/W0 = CA,0X A,1/[k CA,0(1- X A,1)]. Отсюда XA,1 = kV/(kV+W0) = 0,5Ч1/(0,5Ч1+0,25) = 0,667 и
Т2=T1-[qхрCA,0/rcp]Ч[kV/(kV+W0)] = 300 - [-40000Ч2/1110Ч0,8] Ч[0,5Ч1/(0,5Ч1+0,25)]=
= 360 K.
Задача 5
Найти ХА для реакции А ® R в РИС-Н-И, если объем реактора V = 2 м3, расход реакционной смеси W = 0,5 м3/мин, ХА,0 = 0 и константа скорости k = 0,5 мин-1.
Решение
 Получим выражение для степени превращения:
Получим выражение для степени превращения:
X A,1 = (W0XA,0+kV)/(kV+W0). При XA,0=0 это выражение преобразуется в
X A,1 = kV/(kV+W0) = 0,5Ч2/(0,5+ 0,5Ч2) = 0,667.
Задача 6
Найти ХА для реакции А ® R в РИВ-И, если объем реактора V = 2 м3, расход реакционной смеси W0 = 0,5 м3/мин, ХА,0 =0 и константа скорости k=0,5 мин-1.
Решение
V/W0 = 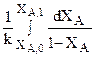 = -k-1ln(1-XA,k)+ k-1ln(1-XA,0), откуда
= -k-1ln(1-XA,k)+ k-1ln(1-XA,0), откуда
XA,1=1-(1- XA,0)exp(-kV/W0). При ХА,0=0 XA,1=1- exp(-kV/W0) = 1-exp(-0,5Ч2/0,5) = 0,8647.
Задача 7
Найти объем двухступенчатого каскада реакторов К-РИВ-И, необходимый для достижения в первой ступени ХА,1 = 0,55 и во второй ХА,2 = 0,85, для реакции А® R с константами скоростей k1 = k2=0,45 мин-1 . Объемный расход потока на входе W0 = 32 л/мин при СА,0= 1 моль/л.
Решение
1. Модель первой ступени: 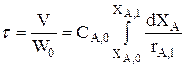 ;
;
2. Модель второй ступени: 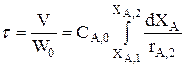 .
.
3. Учитывая, что rA,1=k1CA,0(1-XA,1) и rA,2=k2CA,0(1-XA,2), запишем модель К-РИВ:
t = t1+t2 = 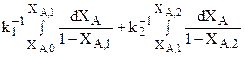
После интегрирования получим:
t= k1-1[ln(1-XA,0)/ln(1-XA,1)] + k2-1[ln(1-XA,1)/ln(1-XA,2)].
При k1 = k2 =k и подстановке численных значений получим выражение вида:
V=W0Чt = W0 k-1 Чln[(1-XA,0)Ч (1-XA,1) /(1-XA,1)Ч(1-XA,2)] =
= 32Ч0,45-1 Ч ln[(1-0)Ч(1-0,55) /(1-0,55)Ч(1-0,85)] =134,90 л.
При этом V1=56,78 и V2=78,12 л.
Задача 8
Определить объём V реактора РИС-Н –И для реакции 2A Ы R . Расход реакционной смеси W0 =2,832 м3/ ч, концентрация вещества А - СА,0 = 24 кмоль/м3.. Константа скорости прямой реакции k1=0,625 м3/(кмоль×ч), константа равновесия КС=16 м3/кмоль×ч. Заданная степень превращения ХА= aх×ХА* при aх=0,8..
Решение
1. Из характеристического уравнения РИС-Н V=W0×CA,0XA/rA. Конечная концентрация вещества А:
СА = СА,0 (1-aXХ*А)/(1+xaXХ*А), где x - коэффициент изменения объема:
2. x= 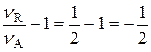 .
.
3. Конечная концентрация продукта R:
CR = CR,0+ 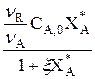 =
= 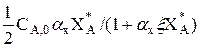 .
.
4. Kc = (2-X*A)ЧX*A/4CA,0(1- X*A)2, откуда
X*A= 1- 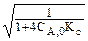 = 1-
= 1- 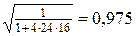
5. Запишем уравнение для скорости химической реакции:
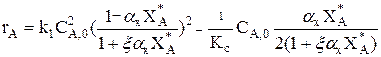
После преобразований и подстановки численных значений получим:
rA= 2,79 кмоль/м3 и V = 2,832Ч24Ч0,8Ч0,975=19,0 м3.
