Степень электролитической диссоциации. Ее определение по изотоническому коэффициенту и электропроводности раствора.
Отношение числа диссоциированных молекул к общему числу растворенных молекул называется степенью диссоциации(α). Степень диссоциации выражают в долях единицы или в процентах. В зависимости от степени диссоциации веществ в 0,1 н растворе при 298К электролиты иногда условно подразделяют на сильныеα>0,3;средние 0,3<α>0.03 и слабые α<0,03. Степень диссоциации зависит от химической природы вещества, температуры, концентрации и увеличивается с понижением концентрации и увеличением температуры раствора. Большинство солей, многие кислоты (HCl,HNO3, H2SO4), гидроксиды щелочных и щелочноземельных металлов (NaOH, KOH, Ca(OH)2) относятся к сильным электролитам. Примерами электролитов средней силы являются H3PO4, H2SO3, H2C2O4. К слабым электролитам относятся большинство органических кислот и оснований, H2СO3, H2SiO3, H2S, HCN, Mg(CN)2 и др.
Определение степени диссоциациииз измерений электропроводности и по изотоническому коэффициенту.
1) Эквивалентная электропроводность прямо пропорциональна числу ионов в растворе и, следовательно, степени диссоциации α
λ=Кα, (7.20)
где К – коэффициент пропорциональности.
Степень диссоциации, также как и эквивалентная электропроводность, увеличивается при понижении концентрации. В очень разбавленном (бесконечно разбавленном) растворе электролит диссоциирует полностью, т.е. α=1, следовательно
λ ∞ =К, (7.21)
где λ ∞ - эквивалентная электропроводность бесконечно разбавленного раствора. Эту величину получают экстраполируя (продолжая) концентрационную зависимость λ=f(c) на нулевую концентрацию электролита (бесконечно разбавленный раствор).
Подставляя значение К из ф-лы (7.21) в (7.20) получим:
α =λ/λ∞ (7.22)
Следовательно, степень диссоциации равна отношению эквивалентной электропроводности при данной концентрации к эквивалентной электропроводности при бесконечном разбавлении.
2) Пусть раствор содержит N моль электролита, степень диссоциации которого равна α. Тогда число моль продиссоциированного электролита составит αN, а недиссоциированного – N(1-α). Если молекула диссоциирует на n ионов, то число моль ионов в растворе составит nαN и общее число частиц растворенного вещества в растворе N(1-α) + nαN. Изотонический коэффициент показывает, во сколько раз увеличивается число частиц растворенного вещества в результате диссоциации, т.е.
 откуда получим для степени диссоциации
откуда получим для степени диссоциации  (7.23)
(7.23)
Из (7.23) следует, что при полной диссоциации электролита (α=1) изотонический коэффициент равен числу ионов, на которое распадается электролит (i=n).
Сильные электролиты — химические соединения, молекулы которых в разбавленных растворах практически полностью диссоциированы на ионы. Степень диссоциации таких электролитов близка к 1. К сильным электролитам относятся многие неорганические соли, некоторые неорганические кислоты и основания в водных растворах, а также в растворителях, обладающих высокой диссоциирующей способностью (спирты, амиды и др.).
Классическая теория электролитической диссоциации применима лишь к разбавленным растворам слабых электролитов. Сильные электролиты в разбавленных растворахдиссоциированы практически полностью, поэтому представления о равновесии между ионами и недиссоциированными молекулами лишено смысла. Согласно представлениям, выдвинутым в 20—30-х гг. 20 в. В. К. Семенченко (СССР), Н. Бьеррумом (Дания), Р. М. Фуоссом (США) и др., в растворах сильных электролитов при средних и высоких концентрациях образуются ионные пары и более сложные агрегаты. Современные спектроскопические данные показывают, что ионная пара состоит из двух ионов противоположного знака, находящихся в контакте («контактная ионная пара») или разделённых одной или несколькими молекулами растворителя («разделённая ионная пара»). Ионные пары электрически нейтральны и не принимают участия в переносе электричества. В сравнительно разбавленных растворах сильных электролитов равновесие между отдельными сольватированными ионами и ионными парами может быть приближённо охарактеризовано, аналогично классической теории электролитической диссоциации, константой диссоциации (или обратной величиной — константой ассоциации). Это позволяет использовать вышеприведённое уравнение для расчёта соответствующей степени диссоциации, исходя из экспериментальных данных.
В простейших случаях (большие одноатомные однозарядные ионы) приближённые значения константы диссоциации в разбавленных растворах сильных электролитов можно вычислить теоретически, исходя из представлений о чисто электростатическом взаимодействии между ионами в непрерывной среде — растворителе.
Примеры сильных электролитов: некоторые кислоты (HClO4, HMnO4, H2SO4, HCl, HBr; HI), гидроксиды щелочных и щёлочноземельных металлов (NaOH, KOH, Ba(OH)2); большинствосолей.
Слабые электролиты — химические соединения, молекулы которых даже в сильно разбавленных растворах незначительно диссоциированны на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах.
Слабыми электролитами являются:
почти все органические кислоты и вода;
некоторые неорганические кислоты: HF, HClO, HClO2, HNO2, HCN, H2S, HBrO, H3PO4,H2CO3, H2SiO3, H2SO3 и др.;
некоторые малорастворимые гидроксиды металлов: Fe(OH)3, Zn(OH)2 и др.
Константа диссоциации — вид константы равновесия, которая показывает склонность большого объекта диссоциировать (разделяться) обратимым образом на маленькие объекты, как например когда комплекс распадается на составляющие молекулы, или когда соль разделяется в водном растворе на ионы. Константа диссоциации обычно обозначается 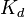 иобратна константе ассоциации. В случае с солями, константу диссоциации иногда называют константой ионизации.
иобратна константе ассоциации. В случае с солями, константу диссоциации иногда называют константой ионизации.
В общей реакции

где комплекс  разбивается на x единиц A и y единиц B, константа диссоциации определяется так:
разбивается на x единиц A и y единиц B, константа диссоциации определяется так:
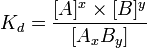
где [A], [B] и [AxBy] — концентрации A, B и комплекса AxBy соответственно.
Связь степени и коснстанты диссоциации. Исходя из определения степени диссоциации, для электролита КА в реакции диссоциации [A−] = [K+] = α·c, [KA] = c — α·c = c·(1 — α), где α — степени диссоциации электролита.
Тогда:
 , , | (2) |
Это выражение называют законом разбавления Оствальда. При очень малых α (α<<1) K=cα² и
 ,
,
таким образом, при увеличении концентрации электролита степень диссоциации уменьшается, при уменьшении — возрастает.
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов,молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых веществ — практически только от температуры.
Произведение растворимости. Материал из Википедии — свободной энциклопедии
Произведение растворимости (ПР, Ksp) — произведение концентраций ионов малорастворимого электролита в его насыщенном растворе при постоянной температуре и давлении. Произведение растворимости — величина постоянная.
При постоянной температуре в насыщенных водных растворах малорастворимых электролитов устанавливается равновесие между твердым веществом и ионами, образующими это вещество. Например, в случае для CaCO3 это равновесие можно записать в виде:

Константа этого равновесия рассчитывается по уравнению:

В приближении идеального раствора с учётом того, что активность чистого компонента равна единице, уравнение упрощается до выражения:

Константа равновесия такого процесса называется произведением растворимости.
В общем виде, произведение растворимости для вещества с формулой AmBn, которое диссоциирует на m катионов An+ и n анионов Bm-, рассчитывается по уравнению:

где [An+] и [Bm-] — равновесные молярные концентрации ионов, образующихся при электролитической диссоциации.
Из произведений растворимости можно рассчитать концентрации катионов и анионов в растворе малорастворимого электролита. Значения произведений растворимости приведены в справочниках.
Условия образования и растворения осадков.Зная концентрации ионов в растворе, можно прогнозировать направление гетерогенного процесса. Если произведение концентраций ионов, образующих малорастворимый сильный электролит, в степенях, равных стехиометрическим коэффициентам, будет больше  , то произойдет образование твердой фазы, т.е. осадка.
, то произойдет образование твердой фазы, т.е. осадка.
Таким образом, условием образования осадка является превышение произведения концентрации ионов малорастворимого сильного электролита над величиной  .
.
Последовательность осаждения двух и более малорастворимых сильных электролитов определяется не величиной Ks, а равновесными концентрациями ионов над осадком, которые вычисляют из Ks. В первую очередь образуется осадок того малорастворимого сильного электролита, для которого концентрация одноименного иона будет меньше.
В качестве примера рассмотрим последовательность осаждения фторида и оксалата кальция.
 (CaF2)= 4 ×10–11
(CaF2)= 4 ×10–11
 (CaC2O4)= 2×10–9
(CaC2O4)= 2×10–9
Если брать за основу  , то в первую очередь должен образоваться осадок CaF2, т.к.
, то в первую очередь должен образоваться осадок CaF2, т.к.
 (CaF2)<
(CaF2)<  (CaC2O4).
(CaC2O4).
Проверим это, рассчитав концентрацию ионов Са2+ в насыщенном растворе:
CaC2O4 ⇄ Са2+ 
CaF2 ⇄ Са2+ + 2F–.
При растворении каждого моля СаС2О4 в раствор переходит 1 моль ионов Са2+ и 1 моль ионов  :
:
 ( СаС2О4) = S2,
( СаС2О4) = S2,
где S – растворимость соли в моль/л:
aСа2+ = S =  = 4,5×10–5 моль/л
= 4,5×10–5 моль/л
При растворении моля CaF2 в раствор переходит 1 моль ионов Са2+ и 2 моль ионов F–:
 (CaF2)= aСа2+×a2F– = S×(2S)2 = 4S3
(CaF2)= aСа2+×a2F– = S×(2S)2 = 4S3
aСа2+ = S =  = 0,84×10–4моль/л
= 0,84×10–4моль/л
Для СаС2О4 в его насыщенном растворе активность ионов Са2+ меньше, чем для CaF2. Поэтому в первую очередь образуется осадок СаС2О4.
Процесс образования осадка можно расчленить на три основные стадии: 1) возникновение зародышей кристаллизации; 2) рост кристаллов из зародышей; 3) агрегация кристаллов с образованием поликристаллического осадка. Эти стадии протекают с разной скоростью. Это обстоятельство объясняет тот факт, почему при достижении условия:
am(An+) ×an(Bm–)> 
не всегда сразу же образуется осадок AmBn: последняя стадия может требовать для своего завершения нескольких часов, а то и суток.
Условием растворения осадка является неравенство:
am(An+) ×an(Bm–)<  ,
,
т.е. растворение осадка малорастворимого электролита происходит при условии, что произведение активностей его ионов меньше  .
.
Растворение осадка или сдвиг равновесия вправо может быть осуществлен с помощью любого метода уменьшения концентрации свободных ионов An+ или Bm–: 1) связыванием этих ионов в другой менее растворимый осадок, 2) связыванием ионов металла в комплекс, 3) связыванием аниона в малодиссоциированную кислоту, 4) окислением или восстановлением катиона или аниона.
Ио́нное произведе́ние воды́-произведение концентраций ионов водорода Н+ и ионов гидроксила OH− в воде или в водных растворах, константа автопротолиза воды.
Вывод значения ионного произведения воды. Вода, хотя и является слабым электролитом, в небольшой степени диссоциирует:

Равновесие этой реакции сильно смещено влево. Константу диссоциации воды можно вычислить по формуле:
 [H+] — концентрация ионов гидроксония (протонов);
[H+] — концентрация ионов гидроксония (протонов);
[OH−] — концентрация гидроксид-ионов;
[H2O] — концентрация воды (в молекулярной форме) в воде;
Концентрация воды в воде, учитывая её малую степень диссоциации, величина практически постоянная и составляет (1000 г/л)/(18 г/моль) = 55,56 моль/л.
При 25 °C константа диссоциации воды равна 1,8·10−16моль/л. Уравнение (1) можно переписать как:

Обозначим произведение K·[H2O] = Kв = 1,8·10−16 моль/л·55,56 моль/л = 10−14моль²/л² = [H+]·[OH−] (при 25 °C).
Константа Kв, равная произведению концентраций протонов и гидроксид-ионов, называется ионным произведением воды. Она является постоянной не только для чистой воды, но также и для разбавленных водных растворов веществ. C повышением температуры диссоциация воды увеличивается, следовательно, растёт и Kв, при понижении температуры — наоборот.
Водоро́дный показа́тель, pH (произносится «пэ аш», английское произношение англ. pH — piː'eɪtʃ «Пи эйч») — мера активности (в очень разбавленных растворах она эквивалентнаконцентрации) ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифмактивности водородных ионов, выраженной в молях на литр:

Вывод значения pH. В чистой воде при 25 °C концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH−]) одинаковы и составляют 10−7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H+] · [OH−] и составляет 10−14 моль²/л² (при 25 °C).
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается, а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH−] говорят, что раствор является кислым, а при [OH−] > [H+] — щелочным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентраций ионов водорода пользуются их десятичным логарифмом, взятым с обратным знаком, который собственно и является водородным показателем — pH.

pOH
Несколько меньшее распространение получила обратная pH величина — показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:

как в любом водном растворе при 22 °C  , очевидно, что при этой температуре:
, очевидно, что при этой температуре:

Гидролиз солей — разновидность реакций гидролиза, обусловленного протеканием реакций ионного обмена в растворах (преимущественно, водных) растворимых солей-электролитов. Движущей силой процесса является взаимодействие ионов с водой, приводящее к образованию слабого электролита в ионном или (реже) молекулярном виде («связывание ионов»).
Различают обратимый и необратимый гидролиз солей[1]:
1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону):


(раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону):


(раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
3. Гидролиз соли слабой кислоты и слабого основания:


(равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа).
Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален. См. также Электролитическая диссоциация.
Степень гидролиза. Под степенью гидролиза подразумевается отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр);
α = (cгидр/cобщ)·100 %
где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли.
Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Является количественной характеристикой гидролиза.
Константа гидролиза — константа равновесия гидролитической реакции. Так константа гидролиза соли равна отношению произведения равновесных концентраций продуктов реакции гидролиза к равновесной концентрации соли с учетом стехиометрических коэффициентов.
В качестве примера ниже приводится вывод уравнения константы гидролиза соли, образованной слабой кислотой и сильным основанием:


Уравнение константы равновесия для данной реакции имеет вид:
 или
или 
Так как концентрация молекул воды в растворе постоянна, то произведение двух постоянных  можно заменить одной новой — константой гидролиза:
можно заменить одной новой — константой гидролиза:

Численное значение константы гидролиза получим, используя ионное произведение воды  и константу диссоциации азотистой кислоты
и константу диссоциации азотистой кислоты  :
:


подставим в уравнение константы гидролиза равна:

В общем случае для соли, образованной слабой кислотой и сильным основанием:
 , где
, где  — константа диссоциации слабой кислоты, образующейся при гидролизе
— константа диссоциации слабой кислоты, образующейся при гидролизе
для соли, образованной сильной кислотой и слабым основанием:
 , где
, где  — константа диссоциации слабого основания, образующегося при гидролизе
— константа диссоциации слабого основания, образующегося при гидролизе
для соли, образованной слабой кислотой и слабым основанием:

