Химические свойства азотной кислоты
Главное, что мы должны отметить, – наличие высшей степени окисления атома азота ограничивает свойства азотной кислоты, с окислителями она не реагирует. Зато с восстановителями, в первую очередь с металлами, она реагирует нетрадиционно и разнообразно.
1. Реакции с металлами. С металлами азотная кислота реагирует как сильный окислитель даже в разбавленных растворах (в отличие от серной кислоты, проявляющей свои окислительные свойства только в концентрированном виде). Образуется обычно нитрат металла, но вместо водорода выделяются газообразные соединения азота: NО2, NО, N2O, N2 или аммиак, который в кислой среде сразу переходит в ион аммония. В принципе при реакции металла с азотной кислотой образуется весь этот «букет» газов, но в зависимости от металла и концентрации кислоты те или иные компоненты будут превалировать.
Так, в лабораторных условиях оксид азота(II) обычно получают при взаимодействии медных стружек с азотной кислотой плотностью 1,2 г/см3, т. е. при обработке меди разбавленной кислотой в газообразных продуктах реакции явно превалирует именно этот оксид:
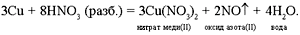
А вот при реакции азотной кислоты той же плотности (а следовательно, и концентрации) с железом содержание оксида азота(II) в смеси составляет только 40% – меньше половины, а остальные 60% равномерно распределены между нитратом аммония, азотом, оксидом азота(I) и оксидом азота(IV) (рис. 8).
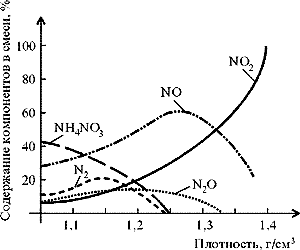 |
| Рис. 8. Зависимость содержания различных продуктов реакции железа с азотной кислотой от плотности азотной кислоты |
Следует отметить такой интересный и жизненно важный факт, что со 100%-й азотной кислотой ни железо, ни алюминий не реагируют (следовательно, ее можно хранить и перевозить в цистернах и других емкостях из этих металлов). Дело в том, что эти металлы покрыты прочными пленками оксидов, нерастворимых в чистой кислоте. Для проявления кислотных свойств нужно, чтобы кислота заметно диссоциировала, а для этого в свою очередь требуется вода.
2. Реакции с неметаллами.С кислородом и озоном азотная кислота не реагирует.
3. Реакция с водой не происходит.Вода лишь способствует диссоциации кислоты.
4. Реакции с кислотами.Азотная кислота не реагирует с другими кислотами по типу реакций обмена или соединения. Однако вполне способна реагировать как сильный окислитель. В смеси концентрированных азотной и соляной кислот протекают обратимые реакции, суть которых можно обобщить уравнением:
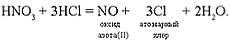
Образующийся атомарный хлор очень активен и легко отбирает электроны у атомов металлов, а имеющийся «под боком» хлорид-ион образует устойчивые комплексные ионы с получающимися ионами металлов. Все это позволяет перевести в раствор даже золото. По той причине, что золото – «царь металлов», смесь концентрированных азотной и соляной кислот называют царской водкой.
Концентрированная серная кислота как сильное водоотнимающее средство способствует реакции разложения азотной кислоты на оксид азота(IV) и кислород.
5. Реакции с основаниями и с основными оксидами. Азотная кислота – одна из сильных неорганических кислот и, естественно, со щелочами реагирует. Реагирует она также и с нерастворимыми гидроксидами, и с основными оксидами. Этим реакциям способствует еще и то обстоятельство, что все соли азотной кислоты имеют хорошую растворимость в воде, следовательно, продукты реакции не будут мешать ее протеканию.
