Способы устранения жесткости воды
Понятие жесткости
Жесткость воды принято связывать с катионами кальция (Са2+) и в меньшей степени магния (Mg2+). В действительности, все двухвалентные катионы в той или иной степени влияют на жесткость. Они взаимодействуют с анионами, образуя соединения (соли жесткости) способные выпадать в осадок. Одновалентные катионы (например, натрий Na+) таким свойством не обладают.
В данной таблице приведены основные катионы металлов, вызывающие жесткость, и главные анионы, с которыми они ассоциируются
| Катионы | Анионы |
| Кальций (Ca2+) | Гидрокарбонат (HCO3-) |
| Магний (Mg2+) | Сульфат (SO42-) |
| Стронций (Sr2+) | Хлорид (Cl-) |
| Железо (Fe2+) | Нитрат (NO3-) |
| Марганец (Mn2+) | Силикат (SiO32-) |
На практике стронций, железо и марганец оказывают на жесткость столь небольшое влияние, что ими, как правило, пренебрегают. Алюминий (Al3+) и трехвалентное железо (Fe3+) также влияют на жесткость, но при уровнях рН, встречающихся в природных водах, их растворимость и, соответственно, «вклад» в жесткость ничтожно малы. Аналогично, не учитывается и незначительное влияние бария (Ва2+).
Виды жесткости
Общая жесткость. Определяется суммарной концентрацией ионов кальция и магния. Представляет собой сумму карбонатной (временной) и некарбонатной (постоянной) жесткости.
Карбонатная жесткость. Обусловлена наличием в воде гидрокарбонатов и карбонатов (при рН>8.3) кальция и магния. Данный тип жесткости почти полностью устраняется при кипячении воды и поэтому называется временной жесткостью. При нагреве воды гидрокарбонаты распадаются с образованием угольной кислоты и выпадением в осадок карбоната кальция и гидроксида магния.
Некарбонатная жесткость. Обусловлена присутствием кальциевых и магниевых солей сильных кислот (серной, азотной, соляной) и при кипячении не устраняется (постоянная жесткость).
Единицы измерения
В мировой практике используется несколько единиц измерения жесткости, все они определенным образом соотносятся друг с другом. В России Госстандартом в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3).
Один моль на кубический метр соответствует массовой концентрации эквивалентов ионов кальция (1/2 Ca2+) 20.04 г/м3 и ионов магния (1/2Mg2+) 12.153 г/м3. Числовое значение жесткости, выраженное в молях на кубический метр равно числовому значению жесткости, выраженному в миллиграмм-эквивалентах на литр (или кубический дециметр), т.е. 1моль/м3=1ммоль/л=1мг-экв/л=1мг-экв/дм3.
Кроме этого в зарубежных странах широко используются такие единицы жесткости, как немецкий градус (do, dH), французский градус (fo), американский градус, ppm CaCO3.
Соотношение этих единиц жесткости представлено в следующей таблице:
| Единицы жесткости воды | ||||
| Моль/м3(мг-экв/л) | Немецкий градус, do | Французский градус, fo | Американский градус | ppm мг/дм3 СаСО3 |
| 1.000 | 2.804 | 5.005 | 50.050 | 50.050 |
Примечание:
Один немецкий градус соответствует 10 мг/дм3 СаО или 17.86 мг/дм3 СаСО3 в воде.
Один французский градус соответствует 10 мг/дм3 СаСО3 в воде.
Один американский градус соответствует 1 мг/дм3 СаСО3 в воде.
Происхождение жесткости
Ионы кальция (Ca2+) и магния (Mg2+), а также других щелочноземельных металлов, обуславливающих жесткость, присутствуют во всех минерализованных водах. Их источником являются природные залежи известняков, гипса и доломитов. Ионы кальция и магния поступают в воду в результате взаимодействия растворенного диоксида углерода с минералами и при других процессах растворения и химического выветривания горных пород. Источником этих ионов могут служить также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий.
Жесткость воды колеблется в широких пределах и существует множество типов классификаций воды по степени ее жесткости.
Обычно в маломинерализованных водах преобладает (до 70%-80%) жесткость, обусловленная ионами кальция (хотя в отдельных редких случаях магниевая жесткость может достигать 50—60%). С увеличением степени минерализации воды содержание ионов кальция (Са2+) быстро падает и редко превышает 1 г/л. Содержание же ионов магния (Mg2+) в высокоминерализованных водах может достигать нескольких граммов, а в соленых озерах — десятков граммов на один литр воды
В целом, жесткость поверхностных вод, как правило, меньше жесткости вод подземных. Жесткость поверхностных вод подвержена заметным сезонным колебаниям, достигая обычно наибольшего значения в конце зимы и наименьшего в период половодья, когда обильно разбавляется мягкой дождевой и талой водой. Морская и океанская вода имеют очень высокую жесткость (десятки и сотни мг-экв/дм3)
Влияние жесткости
С точки зрения применения воды для питьевых нужд, ее приемлемость по степени жесткости может существенно варьироваться в зависимости от местных условий. Порог вкуса для иона кальция лежит (в пересчете на мг-эквивалент) в диапазоне 2—6 мг-экв/л, в зависимости от соответствующего аниона, а порог вкуса для магния и того ниже. В некоторых случаях для потребителей приемлема вода с жесткостью выше 10 мг-экв/л. Высокая жесткость ухудшает органолептические свойства воды, придавая ей горьковатый вкус и оказывая отрицательное действие на органы пищеварения
Всемирная Организация Здравоохранения не предлагает какой-либо рекомендуемой величины жесткости по показаниям влияния на здоровье. В материалах ВОЗ говорится о том, что хотя ряд исследований и выявил статистически обратную зависимость между жесткостью питьевой воды и сердечно-сосудистыми заболеваниями, имеющиеся данные не достаточны для вывода о причинном характере этой связи. Аналогичным образом, однозначно не доказано, что мягкая вода оказывает отрицательный эффект на баланс минеральных веществ в организме человека
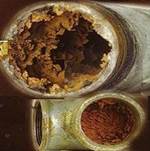 Вместе с тем, в зависимости от рН и щелочности, вода с жесткостью выше 4 мг-экв/л может вызвать в распределительной системе отложение шлаков и накипи (карбоната кальция), особенно при нагревании. Именно поэтому нормами Котлонадзора вводятся очень жесткие требования к величине жесткости воды, используемой для питания котлов (0.05—0.1 мг-экв/л).
Вместе с тем, в зависимости от рН и щелочности, вода с жесткостью выше 4 мг-экв/л может вызвать в распределительной системе отложение шлаков и накипи (карбоната кальция), особенно при нагревании. Именно поэтому нормами Котлонадзора вводятся очень жесткие требования к величине жесткости воды, используемой для питания котлов (0.05—0.1 мг-экв/л).
Кроме того, при взаимодействии солей жесткости с моющими веществами (мыло, стиральные порошки, шампуни) происходит образование «мыльных шлаков» в виде пены. Это приводит не только к значительному перерасходу моющих средств. Такая пена после высыхания остается в виде налета на сантехнике, белье, человеческой коже, на волосах (неприятное чувство «жестких» волос хорошо известное многим). Главным отрицательным воздействием этих шлаков на человека является то, что они разрушают естественную жировую пленку, которой всегда покрыта нормальная кожа и забивают ее поры. Признаком такого негативного воздействия является характерный «скрип» чисто вымытой кожи или волос. Оказывается, что вызывающее у некоторых раздражение чувство «мылкости» после пользования мягкой водой является признаком того, что защитная жировая пленка на коже цела и невредима. Именно она и скользит. В противном случае, приходится тратиться на лосьоны, умягчающие и увлажняющие кремы и прочие хитрости для восстановления той защиты кожи, которой нас и так снабдила матушка Природа.
Вместе с тем, необходимо упомянуть и о другой стороне медали. Мягкая вода с жесткостью менее 2 мг-экв/л имеет низкую буферную емкость (щелочность) и может, в зависимости от уровня рН и ряда других факторов, оказывать повышенное коррозионное воздействие на водопроводные трубы. Поэтому, в ряде применений (особенно в теплотехнике) иногда приходится проводить специальную обработку воды с целью достижения оптимального соотношения между жесткостью воды и ее коррозионной активностью.
Под жесткостью воды понимают свойство, обусловленное присутствием в воде растворенных солей, в основном кальция и магния. Жесткость воды подразделяется па карбонатную (присутствие в ней гидрокарбонатов магния и кальция) и некарбонатную (наличие солей сильных кислот - хлоридов или сульфатов кальция и магния). Сумма карбонатной и некарбонатной жесткости определяет общую жесткость.
Карбонатную жесткость называют временной, так как при длительном кипячении подобной воды гидрокарбонаты разлагаются с образованием осадка карбоната кальция и выделением углекислого газа:
Ca(HCO3)2 = СаСО3+СO2↑ + Н2O
Mg(НСО3)2 = Mg(ОН)2↓ + 2СO2↑
Жесткость воды, обусловленная наличием сульфатов магния и кальция, называется постоянной. Она может быть устранена лишь химическим путем:
CaSO4+Na2CO3=CaCO3↓+Na2SO4.
В настоящее время для устранения жесткости используют также ионообменные смолы.
Способы устранения жесткости воды
В природной воде растворены соли кальция и магния. Это гидрокарбонаты и сульфаты. Покажем два способа осаждения гидрокарбонатов для уменьшения жесткости воды. Первый способ – кипячение. При кипячении* растворимые гидрокарбонаты переходят в нерастворимые карбонаты, и жесткость воды уменьшается.
Сa(HCO3)2 = CaCO3 ↓ + H2O + CO2↑
Второй способ – добавление известковой воды. При добавлении известковой воды гидрокарбонаты переходят в карбонаты и вода становится более мягкой.
Сa(HCO3)2+ Ca(OH)2 = CaCO3 ↓ +2 H2O
Но жесткость воды зависит еще и от сульфатов кальция и магния. Сульфаты кальция и магния можно удалить с помощью карбоната натрия. При добавлении карбоната натрия сульфаты переходят в нерастворимые карбонаты кальция и магния.
CaSO4 + Na2CO3= CaCO3 ↓+ Na2SO4
УМЯГЧЕНИЕ ВОДЫ
Устранение из воды солей жесткости, т. е. умягчение её, необходимо производить для питания котельных установок, причем жесткость воды для котлов среднего и низкого давления должна быть не более 0,3 мг-экв/л. Умягчать воду требуется также для таких производств, как текстильное, бумажное, химическое, где вода должна иметь жесткость не более 0,7 -1,0 мг-экв/л. Умягчение воды для хозяйственно-питьевых целей также целесообразно, особенно в случае, если она превышает 7мг-экв/л. Применяют следующие основные методы умягчения воды:
· реагентный метод - путем введения реагентов, способствующих образованию малорастворимых соединений кальция и магния и выпадению их в осадок;
· катионовый метод, при котором умягчаемая вода фильтруется через вещества, обладающие способностью обменивать содержащиеся в них катионы (натрия или водорода) на катионы кальция и магния, растворенный в воде солей. А результате обмена задерживаются ионы кальция и магния и образуются натриевые соли, не придающие воде жесткость;
· термический метод, заключающийся в нагревании воды до температуры выше 100°, при этом почти полностью удаляются соли карбонатной жесткости.
Часто методы умягчения применяют комбинированно. Например, часть солей жесткости удаляют реагентным способом, а оставшуюся часть с помощью катионного обмена. Из реагентных методов содово-известковый способ умягчения является наиболее распространенным. Сущность его сводится к получению вместо растворенных в воде солей Са Mg нерастворимых солей СаСО3 и Mg(OH)2, выпадающих в осадок.
Оба реагента - соду Na2CO3 и известь Са(ОН)2 - вводят в умягчаемую воду одновременно или поочередно. Соли карбонатной, временной жесткости удаляют известью, не карбонатной, постоянной жесткости - содой. Химические реакции при удалении карбонатной жесткости протекают следующим образом:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3 + 2Н2О
Гидрат окиси магния Mg(OH)2 коагулирует и выпадает в осадок. Для устранения некарбонатной жесткости в умягчаемую воду вводят Na2CO3. Химические реакции при удалении некарбонатной жесткости следующие:
Na2CO3 + CaSO4 = CaCO3 + Na2SO4;
Na2CO3 + СаС12 = СаСО3 + 2NaCl.
В результате реакции получается углекислый кальций, который выпадает в осадок. Реагенты, применяемые при обработке воды, вводят в воду в следующих местах:
а) хлор (при предварительном хлорировании) - во всасывающие трубопроводы насосной станции первого подъема или в водоводы, подающие воду на станцию очистки;
б) коагулянт - в трубопровод перед смесителем или в смеситель;
в) известь для подщелачивания при коагулировании - одновременно с коагулянтом;
г) активированный уголь для удаления запахов и привкусов в воде до 5 мг/л - перед фильтрами. При больших дозах уголь следует вводить на насосной станции первого подъема или одновременно с коагулянтом в смеситель водоочистной станции, но не ранее чем через 10 мин после введения хлора;
д) хлор и аммиак для обеззараживания воды вводят до очистных сооружений и в фильтрованную воду. При наличии в воде фенолов аммиак следует вводить как при предварительном, так и при окончательном хлорировании.
К специальным видам очистки и обработки воды относятся опреснение, обессоливание, обезжелезивание, удаление из воды растворенных газов и стабилизация.
