Количественное определение. Весь процесс количественного определения алкалоидов в растительном сырье можно разделить на три основных этапа (стадии): 1) извлечение алкалоидов из
Весь процесс количественного определения алкалоидов в растительном сырье можно разделить на три основных этапа (стадии): 1) извлечение алкалоидов из растительного сырья; 2) очистка полученных "извлечений и, если требуется по методике, разделение смеси алкалоидов на индивидуальные соединения; 3) определение содержания алкалоидов.
Извлечение алкалоидов. При количественном определении алкалоиды из растительного сырья, так же как и при их выделении (получении), извлекают или в ви^е оснований, или солей.
1. Извлечение алкалоидов в виде основания. При извлечении алкалоидов в виде оснований соли алкалоидов, в виде которых они содержатся в растениях, переводят в основания. Это достигается обработкой сырья различными щелочами. При количественном определении алкалоидов в растительном сырье чаще всего используют растворы аммиака и едкого натра, а также карбонат натрия и гидроксид кальция. Выбор щелочи зависит от свойств и строения алкалоидов. Извлечение свободных оснований алкалоидов проводится органическими растворителями, не смешивающимися с водой, обычно хлороформом, этиловым эфиром или дихлорэтаном.
2. Извлечение алкалоидов в виде солей. Соли алкалоидов в большинстве своем хорошо растворяются в воде и спиртах (этиловый, метиловый). Обычно алкалоиды экстрагируют 1—2%-ной серной, соляной, винной, уксусной кислотой или подкисленным спиртом.
Очистка извлечения. Для очистки извлечений чаще всего проводится повторное переведение солей алкалоидов в водный раствор и свободных оснований в органический растворитель (см. с. 133). Кроме того, для очистки извлечений, а также для разделения алкалоидов широко используется хроматографический метод (ко- лоночная хроматография, хроматография в тонком слое сорбента и на бумаге).
Определение содержания алкалоидов. Количественное содержание алкалоидов можно определить: гравиметрическим, титрометрическим, колориметрическим, полярометриче- ским, полярографическим, спектрофотометр ическим.денситометриче- ским или другими методами.
Методика количественного определения алкалоидов в листьях красавки (Folium Belladonnae), траве красавки (Herba Belladonnas), корнях красавки (Radix Belladonnae), листьях белены (Folium Hyoscyami) и листьях дурмана (Folium Stramonii).
В листьях, траве и корнях красавки (Atropa bellodonna L.), листьях белены (Hyoscyamus niger L.) и дурмана обыкновенного (Datura stramonium L) сем. пасленовых (Solanaceae) содержатся алкалоиды производные тропана. В этих видах растительного сырья преобладает гиосциамин, переходящий под влиянием щелочей в оптически инактивный атропин. Кроме того, в значительно меньшем количестве содержится скополамин и другие близкие по
6 п/р Гринкевич н др.
строению алкалоиды!
| сн,он |
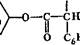 |
| N—СН |
| скополамип |
сн2он
V—CH^V-O—с—с н / 7 II 1 •
Гиосциамин
По данной методике определяется содержание суммы алкалоидов. Определение проводится титрометрическим методом (обратное титрование).
10 г измельченного сырья, проходящего сквозь сито с диаметром отверстий 1 мм, помещают в колбу вместимостью 250 мл, приливают 7 мл концентрированного раствора аммиака, 150 мл этилового эфира [3] и в течение I ч смесь часто и энергично взбалтывают, эфирное извлечение быстро фильтруют через вату в колбу вместимостью 200 мл, прикрывая воронку часовым стеклом. К фильтрату прибавляют 5 мл воды, энергично взбалтывают и оставляют в покое до просветления эфирного слоя, после чего отмеривают с помощью мерного цилиндра 90 мл эфирного извлечения в делительную воронку вместимостью 200 мл. Цилиндр дважды ополаскивают этиловым эфиром порциями по 10 мл, которые присоединяют к отмеренному эфирному извлечению.
Из эфирного извлечения алкалоиды извлекают последовательно 20, 15, 10 мл 1%-ной НС1 до полного их извлечения (проба с реактивом Майера или раствором кремневольфрамовой кислоты), каждый раз фильтруя через смоченный водой фильтр (диаметром 5 см) во вторую делительную воронку такой же вместимости. Фильтр дважды промывают 1%-ной НС1 по 5 мл, присоединяя промывную, жидкость к общему кислотному извлечению.
Кислотное извлечение подщелачивают 10%-ным раствором аммиака до щелочной реакции по фенолфталеину и алкалоиды извлекают последовательно 20, 15, 10 мл хлороформа, взбалтывая по 3 мин.
Каждую порцию хлороформного извлечения фильтруют через бумажный фильтр, на который предварительно помещают 4—5 р свежепрокаленного безводного сульфата натрия, смоченного хлороформом. Фильтрование проводят в колбу для отгонки вместимостью 100 мл. Фильтр промывают хлороформом дважды по 5 мл. Хлороформ отгоняют на водяной бане до 1—2 мл, остаток хлороформа в колбе удаляют продуванием воздуха до полного исчезновения запаха растворителя.
Сухой остаток растворяют в 15 мл 0;02 н. НС1 при подогревании на водяной бане'и оттитровывают избыток последней 0,02 н. NaOH до появления желтой окраски (индикатор — метиловый красный).
1 мл 0,02 н. НС1 соответствует 0,005780 г алкалоидов (считая на гиосциамин). Процентное содержание в пересчете на абсолютно сухое сырье х вычисляют по формуле
(15 — V) 0,005780- 100- 100 /л (100—да)
где V — объем 0,02 н. NaOH, пошедшего на титрование, мл; т — масса навески сырья, соответствующая объему эфирного извлечения, г; w — потеря в массе сырья при высушивании, %.
"Реактивы и оборудование: аммиак(конц., 10%-ный р-р); НС1 (1%-ная, 0,02 н.); NaOH (0,02 н.); хлороформ; эфир этиловый; Na2S04 (безводн.); реактив Майера; кремневольфрамовая кислота; фенолфталеин; метиловый красный;
Бумага лакмусовая синяя; бумага фильтровальная; вата гигроскопическая; колбы с притертой пробкой вместимостью 150 мл; колбы конические с нормальным шлифом вместимостью 100 мл; колбы конические вместимостью 100 мл; воронки делительные вместимостью 200 мл; цилиндры мерные на 10, 20 и 100 мл; воронки стеклянные для фильтрования диаметром 5 см; сггекла часовые; палочки стеклянные; бюксы с притертой крышкой; бюретки вместимостью 25 мл; капельницы стеклянные лабораторные; установка для отгонки хлороформа; шкаф сушильный лабораторный; весы ручные; весы лабораторные аналитические; эксикатор; штативы для делительных воронок; штативы лабораторные; бани водяные лабораторные; сито с диаметром отверстий 1 мм.
Методика количественного определения скополамина в семенах дурмана индейского (Semen Daturae innoxicte) (ФС 42-1005-75). Плоды и семена дурмана индейского (Datura innoxia Mill.) сем. пасленовых (Solanaceae) содержат тропановые алкалоиды (скопола- мин, гиосциамин, норгиосциамин и др.). Большее количество приходится на долю скополамина.
Определение содержания скополамина в растительном сырье проводится гравиметрическим методом.
10(5 г сырья, измельченного и просеянного сквозь сито с отверстиями диаметром 1 мм, взвешенного с погрешностью не более 0,01 г, помещают в колбу вместимостью 1 л, заливают 800 мл дихлорэтана и 50 мл раствора аммиака, встряхивают в течение 20 мин и оставляют до следующего дня. Затем содержимое колбы вновь взбалтывают в течение 20 мин и после отстаивания дихлорэтановое извлечение фильтруют, точно измеряют его объем, переносят в делительную воронку вместимостью 1 л, алкалоиды извлекают 10%-ной уксусной кислотой 6 раз по 20 мл до полного извлечения (проба с кремневольфрамовой кислотой).
| 6» |
Полученное уксуснокислое извлечение промывают 2—3 раза хлороформом порциями по* 20 мл, затем уксуснокислое извлечение подщелачивают карбонатом калия по фенолфталеиновой бумаге и алкалоиды извлекают этиловым эфиром 5—6 раз порциями по 30 мл (проба с кремневольфрамовой кислотой). Эфирные извлечения фильтруют через бумажный фильтр с 3—4 г безводного Na2S04 в предварительно взвешенную (с погрешностью не более 0,0001 г) круглодонную колбу вместимостью 200 мл, фильтр с Na2S04 промывают 30 мл сухого этилового эфира, который присоединяют к основному эфирному извлечению, эфир отгоняют досуха на водя
ной бане. Остаток растворяют в 15—20 мл хлороформа, приливают 20—25 мл 1%-ной пикриновой кислоты в хлороформе, 2—3 мл воды и 20 мл бензола. Содержимое колбы перемешивают стеклянной палочкой в течение 45 мин и оставляют на 24 ч.
Выпавший осадок пикрата скополамина отфильтровывают на предварительно взвешенном стеклянном фильтре № 3. Фильтр с осадком и колбу с пикратом скополамина, оставшимся на стенках, сушат в сушильном шкафу при 100—105 °С в течение 3 ч до постоянной массы и после охлаждения взвешивают. Масса пикрата скополамина, находящегося в колбе и собранного на стеклянном фильтре, составляет общее количество выделенного пикраТгГ скополамина. 1 г пикрата скополамина содержит 0,559 г скополамина-основания.
Процентное содержание скополамина-основания х на абсолютно сухое сырье вычисляют по формуле
_ 0,559а100 • 100* m (100 —йу) '
где т — масса навески сырья, соответствующая объему дихлорэта- нового извлечения, взятого для анализа, г; а — количество пикрата скополамина, г; w — потеря в массе сырья при высушивании, %; 0,559 — коэффициент пересчета пикрата скополамина на ско- пол амин-основание.
Реактивы и оборудование: аммиак 10%-ный; СН3СООН 10%-ная; K2C03; Na2S04; пикриновая кислота; кремневольфрамовая кислота; дихлорэтан; этиловый эфир; бензол; хлороформ; фенолфталеин
Бумага .фильтровальная; колбы с притертой пробкой вместимостью 1 л; колбы конические вместимостью 1 л; колбы круглодонные с нормальным шлифом вместимостью 200 мл; цилиндры мерные на 10, 100 и 1000 мл; фильтры стеклянные № 3, воронки делительные вместимостью 200 и 1000 мл, воронки стеклянные для фильтрования диаметром 7 см; бюксы с притертыми крышками; эксикатор; палочки стеклянные; сито с диаметром отверстий 1 мм; установка .для отгонки эфира; бани водяные лабораторные; весы ручные; весы лабораторные аналитические; штативы для делительных воронок; шкаф сушильный лабораторный.
Методика количественного определения алкалоидов в траве термопсиса (Herba Thermopsidis) (ГФ X, ст. 327). В траве термопсиса (Thermopsis lanceolata R. Br.) сем. бобовых — Fabaceae (Legumino- sae) содержатся алкалоиды — производные хинолизидина (термопсин, гомотермопсин, пахикарпин, анагирин, метилцитизин и др.):
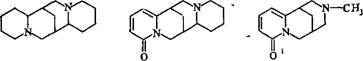 пахикарпин анагирин (термопсин) метилцитизив пахикарпин анагирин (термопсин) метилцитизив |
По данной методике определяется сумма алкалоидов титромет- рическим методом (прямое титрование).
Около 10 г (точная навеска) травы термопсиса, измельченной и просеянной сквозь сито с диаметром отверстий 1 мм, помещают в колбу вместимостью 400—500 мл, приливают 200 мл хлороформа, подщелачивают 10%-ным раствором аммиака до ясно щелочной реакции по фенолфталеину, взбалтывают на вибрационном аппарате в течение 1,5 ч-. Хлороформное извлечение процеживают через вату в мерный цилиндр. Точно отмеренный объем хлороформного извлечения, соответствующий определенной навеске сырья, переносят в колбу и хлороформ отгоняют до объема 5 мл. Остаток переносят в делительную воронку вместимостью 100 мл, колбу дважды промывают 5 мл хлороформа, который присоединяют к основному хлороформному раствору. Хлороформный раствор взбалтывают с 1 %-ной НС1 по 10 мл, затем по 5 мл до полного извлечения алкалоидов (проба с реактивом Майера или с раствором кремневольфрамовой кислоты). Объединенные солянокислые извлечения подщелачивают 10%-ным NaOH по фенолфталеину и трижды извлекают хлороформом порциями по 15, 10 и 5 мл. Хлороформные извлечения фильтруют через фильтр, в который помещают 2 г безводного Na2S04. Фильтр с Na2S04 трижды промывают хлороформом порциями по 10 мл, которые присоединяют к основному фильтрату. Хлороформ отгоняют на водяной бане до 2—3 мл и его остаток удаляют продуванием воздуха. Полученный в колбе остаток растворяют в 5 мл этилового спирта и прибавляют 15 мл воды, 2 капли раствора метилового красного и 1 каплю метиленового синего и титруют 0,1 н. НС1 до появления сине-фиолетового окрашивания.
1 мл 0,1 н. НС1 соответствует 0,0244 г алкалоидов термопсиса: _ 0,0244У-100-100-200 * V\tn (100 —ш)
где V — объем 0,1 н. НС1, израсходованный на титрование, мл; m — масса навески сырья, г; w — потеря в массе сырья при высушивании, %; V1 — объем хлороформного извлечения, взятого для анализа, мл.
Реактивы и оборудование: NH4OH 10%-ный; хлороформ; этиловый спирт (этанол); НС1, 0,1 н., 1%-ная; NaOH; фенолфталеин; Na2S04 (безводн.); этиленовый синий; метиловый красный; реактив Майера; креМне- вольфрамовая кислота.
Колбы с притертой пробкой вместимостью 500 мл; колбы конические с нормальным шлифом вместимостью 100 мл; колбы конические вместимостью 100 мл; воронки делительные вместимостью 100 мл; цилиндры мерные на 10, 25 и 200 мл; воронки стеклянные для фильтрования диаметром 5 см; бюретки вместимостью 25 мл; капельницы стеклянные лабораторные; установка для отгонки хлороформа; бюксы с притертой крышкой; штативы для делительных воронок; штативы лабораторные; шкаф сушильный лабораторный; эксикатор; весы аналитические лабораторные; весы ручные; сито с диаметром отверстий 1 мм.
Методика количественного определения цитизина в траве термопсиса очередноцветкового (Herba Thermopsidis alterniflorae ФС 42-1281-79). Трава термопсиса очередноцветкового (Thermopsis alterniflora Rgl. et Schmath.), сем. бобовых — Fabaceae (Legumino- sae) содержит алкалоиды производные хинолизидина; основным является цитизин:
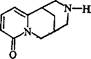 |
Трава термопсиса очередноцсеткового наряду с семенами термопсиса ланцетовидного служит промышленным источником получения цитизина. Определение содержания цитизина в траве термопсиса очередноцветкового проводят хроматоспектрофотометрическим методом.
Около 10 г (с погрешностью до 0,01 г) сырья, измельченного и просеянного сквозь сито с диаметром отверстий 1 мм, помещают в плоскодонную колбу вместимостью 250 мл, приливают 100 мл хлороформа, подщелачивают 5 мл концентрированного раствора NH4OH, закрывают пробкой и встряхивают на вибрационном аппарате в течение 2 ч или оставляют при комнатной температуре на 12—15 ч, после чего встряхивают полчаса.
Хлороформное извлечение фильтруют через вату в мерный цилиндр; 50 мл фильтрата переносят в коническую колбу вместимостью 100 мл и хлороформ отгоняют до объема 1—2 мл. Остатки хлороформа удаляют продуванием воздуха. К остатку пипеткой приливают 2 мл 0,1 н. раствора NaOH и растирают стеклянной палочкой до полного удаления комочков, затем прибавляют 8 мл воды и перемешивают. К содержимому приливают пипеткой 10 мл 0,2 н. НС1, перемешивают 5—6 мин и фильтруют через тройной бумажный складчатый фильтр диаметром 7 см.
По 0,04 мл фильтрата (70—90 мкг) наносят калиброванной микропипеткой на линию старта (на 4 средние полосы) хроматографической пластинки; первую полосу оставляют контрольной; на шестую полосу наносят в качестве «свидетеля» 0,04 мл (80 мг) 0,2%-ного спиртового раствора цитизина-основания.
Растворы наносят полосами длиной 1—1,2 см каждая. Во время нанесения проб пластинку подсушивают теплым воздухом. Пластинку с нанесенными пробами высушивают на воздухе в течение 5 мин, затем помещают в предварительно насыщенную (не менее 2 ч) вертикальную камеру со смесью растворителей: 95%-ный этиловый спирт — хлороформ — концентрированный раствор аммиака (40 : 80 : 0,05) и хроматографируют восходящим методом при комнатной температуре.
Через 1,5—2 ч, когда фронт растворителей пройдет около 16 см, пластинку вынимают из камеры, сушат на воздухе в течение 3 мин и просматривают в УФ свете при длине волны 360 нм. Отмечают участки с пятнами на уровне «свидетеля». Цитизин просматривается на синем фоне пластинки в виде фиолетовых пятен. Для проверки полосу со «свидетелем» и одну полосу с испытуемым раствором проявляют реактивом Драгендорфа.
Участки сорбента с пятнами, находящимися на уровне проявленного пятна цитизина (испытуемого раствора и пятна «свидетеля»), и такой же участок сорбента с контрольной полосы количественно переносят в колбы со шлифом, заливают 10 мл 95%-ного этилового спирта и встряхивают на вибрационном аппарате в течение 1 ч. Затем растворы переносят в пробирки для центрифугирования и центрифугируют 15 мин при скорости вращения 4000 об/мин или фильтруют через двойной бумажный складчатый фильтр.
Оптическую плотность полученного элюата измеряют на спектрофотометре СФ-4А или СФ-16 в кювете с толщиной слоя 10 мм при длине волны 311 нм, используя в качестве раствора сравнения элюат с контрольной полосы.
Процентное содержание цитизина х в пересчете на абсолютно сухое сырье вычисляют по формуле
_ 100-20-10D-1,11 • 100К D - 111 • 400/С * /л50 • V ■434 (100 — ш) ~~ mV-434 (100-И '
где 100 — объем хлороформа, взятого для извлечения суммы алкалоидов из сырья, мл; 50 — объем хлороформного извлечения, взятого для анализа, мл; 20 — объем солянокислого раствора суммы алкалоидов, мл; V — объем солянокислого раствора суммы алкалоидов, нанесенного на хроматограмму, мл; 10 — объем элюата, мл; 434 —удельный показатель поглощения цитизина Епри длине волны 311 нм, полученный на приборе, использованном при разработке метода; т — масса навески сырья, г; w — потеря в массе сырья при высушивании, %; D — оптическая плотность элюата при длине волны 311 нм; 1,11 — поправочный коэффициент на неполное элюирование цитизина с хроматограммы; К — инструментальная поправка на используемые кюветы и спектрофотометр.
Приготовление сорбента. 2 кг силикагеля марки КСК (ГОСТ 3966—76) измельчают на шаровой мельнице и переносят в бутыль вместимостью 10 л, заливают 6 л 2 н. НС1, перемешивают и оставляют на 15—20 ч, после чего НС1 сливают сифоном и силикагель промывают дистиллированной водой декантацией с отстаиванием в течение 7 ч до отрицательной реакции промывной воды на хлориды (проба с AgN03). Затем силикагель заливают таким же, количеством воды, тщательно перемешивают и через 20 мин быстро сливают суспензию в низкий кристаллизатор. Осевшие крупные частицы отбрасывают, суспензию после отстаивания переносят на воронку Бюхнера с тройным бумажным фильтром и промывают 3—4 раза 95%-ным этиловым спиртом. Силикагель сушат на воздухе в течение 4—5 ч, хранят в стеклянной банке с притертой пробкой.
Приготовление хроматографических пластинок. 0,3 г CaS04 тщательно растирают в фарфоровой ступке, прибавляют 2,7 г силикагеля КСК и перемешивают. Прибавляют 5 мл 0,1 н. NaOH, перемешивают пестиком 30—40 с, затем добавляют еще 5 мл NaOH, продолжая размешивать 30 — 40 с. Гомогенную массу, не содержащую пузырьков воздуха, наносят ровным слоем на пластинку размером 13 X 18 см и оставляют на 17—20 ч в строго горизонтальном положении на воздухе. Высушенную пластинку делят на 6 продольных полос шириной 2 см каждая (толщина разделительных линий 1—2 мм).
Приготовление 0,2%-ного спиртового раствора цитизина. 0,1 г (точная навеска) цитизина-осневания (ст. 199 ГФ X) помещают в мерную колбу вместимостью 50 мл, растворяют в 95%-ном этиловом спирте, доводят спиртом до метки и тщательно размешивают.
Определение инструментальной поправки «К» н а используемый спектрофотометр и кюветы. Инструментальная поправка устанавливается по дихромату калия на спектрофотометре и в кюветах, которые будут использованы при проведении анализа. Кюветы должны быть постоянными — одна для контроля, другая для используемого раствора.
10 мг (точная навеска) высушенного до постоянной массы при 105 °С дихромата калия растворяют в 100 мл 0,005 М H2S04. Полученный исходный раствор разбавляют 0,005 М H2S04 в соотношениях 1:1, 1:2; 1:3, 1.4; 1:5. Оптическую плотность полученных растворов определяют на спектрофотометре в кювете с толщиной слоя 10 мм при длине волны 311 нм. В качестве раствора сравнения используют 0,005 М H2S04. Удельный показатель поглощения (Е^) дихромата калия вычисляют по формуле
, % 10VnD
-iCM т »
где m — масса навески дихромата калия, мг; V— объем раствора, мл; п— число разведения, D— оптическая плотность дихромата калия
Инструментальная поправка К вычисляется по формуле К = 50,62/£1'с/^дК, где 50,62 — значение удельного показателя поглощения дихромата калия при длине волны 311 нм, полученное по прибору, на котором проводился анализ количественного определения дитизина при разработке метода (СФ-4А); ^'^мДК — удельный показатель поглощения дихромата калия при длине волны 311 нм по прибору, на котором проводят анализ количественного определения цитизина.
Содержание цитизина в пересчете на абсолютно сухое сырье должно быть не менее 0,6 %.
Реактивы и оборудование: хлороформ, аммиак (конц. р-р); NaOH (0,1 н.); НС1 (0,1 и.; 2 н.); этиловый спирт 95%-ный (этанол); реактив Драгендорфа; силикагель марки КСК; CaS04; HsS04, 0,005 М; вода дистиллированная; AgN03; цитизин; калия дихромат.
Бумага фильтровальная; колбы плоскодонные с притертой пробкой вместимостью 250 мл; колбы конические с нормальным шлифом вместимостью 100 мл; цилиндры мерные на 10 и 100 мл; установка для отгонки хлороформа; пипетки измерительные вместимостью 1 и 2 мл; бюксы о притертой крышкой; вибрационный аппарат; ступки фарфоровые с пестиком; палочки стеклянные; вата гигроскопическая; колба Бунзена; воронки Бюхнера; воронки стеклянные для фильтрования диаметром 5 и 10 см; пластинки стеклянные для ТСХ размером 13 X X 18 см; камера хроматографическая для ТСХ; весы лабораторные аналитические; весы ручные; сита с диаметром отверстий 1 мм; шкаф сушильный лабораторный; УФ лампа; центрифуга лабораторная; спектрофотометры СФ-4А, СФ-16; бани водяные лабораторные; штативы для делительных воронок.
Методика количественного определения платифиллина в траве крестовника плосколистного (Herba Senecionis platyphylloidis). Крестовник плосколистный (Senicio platyphylloides Somm. et. Lev) сем. астровых — Asteraceae (сложноцветных — Compositae) содержит алкалоиды — производные пирролизидина (платифиллин, сене- цифиллин). В растительном сырье они содержатся в основном в виде N-оксидов:
сн—сн8 сн3 сн3 сн—сн3 сн3 СН;,
0=с—G-CHr-<!:н—i—с=о о=с-с—снг—<h—с==о
d)HЬн
CHj—О ~ O—j---- 1---- г—снг—о
UJ
'NvI
О платифиллин
Платифиллин N-оксид
По данной методике проводится определение платифиллина в восстановленной форме хроматофотоэлектроколориметрическим методом.
Аналитическую пробу сырья измельчают до размера частиц 2 мм, берут навеску сырья массой 20 г (с погрешностью не более 0,01 г), помещают в колбу вместимостью 1 л, заливают 500 мл 5%-ной H2S04; сюда же добавляют 4 г цинковой пыли, смесь перемешивают, встряхивают, закрывают ватным тампоном, оставляют стоять в течение 6 ч при периодическом встряхивании и затем кислотное извлечение фильтруют через бумажный фильтр.
100 мл фильтрата помещают в делительную воронку, подщелачивают концентрированным раствором аммиака (по фенолфталеину) и алкалоиды исчерпывающе извлекают этиловым эфиром порциями 70, 30, 30 мл и т. д. (пробы на полноту извлечения с 1 %-ным раствором кремневольфрамовой кислоты). Эфирные извлечения объединяют, сушат безводным Na2S04, отфильтровывают и отгоняют досуха на водяной бане. Сухой остаток растворяют в 5 мл хлороформа. 0,05 мл полученного раствора наносят на линию старта стеклянной пластинки размером 6 X 18 см с закрепленным слоем силикагеля марки КСК. Пластинку с нанесенной пробой высушивают на воздухе в течение 5—10 мин, а затем помещают в хроматографическую камеру с метиловым спиртом и хроматогра- фируют восходящим способом. Когда фронт растворителя дойдет до конца пластинки, ее вынимают из камеры, сушат сначала на воздухе в течение 5 мин, затем в сушильном шкафу 30 мин при температуре 50 °С, охлаждают на воздухе и опрыскивают реактивом Драгендорфа. При этом на пластинке должно появиться пятно платифиллина (Rf около 0,36) и, выше — пятно сенецифиллина (Rf около 0,50). Проявленное пятно платифиллина обводят препаровальной иглой. Отмеченный участок счищают в делительную воронку вместимостью 50 мл, в которую затем прибавляют 15 мл 1 %-ной НС1 и встряхивают в течение 3 мин. При этом образовавшийся на адсорбенте комплекс алкалоида с реактивом Драгендорфа разрушается. Затем в воронку прибавляют 0,2 мл 1 %-ного раствора тропеолина 000— II и 10 мл хлороформа, вновь встряхивают в течение 3 мин и окрашенный хлороформный слой, содержащий соединение алкалоида с тропеолином, фильтруют через бумажный фильтр, предварительно смоченный хлороформом, в мерную колбу вместимостьнЛЮ мл. Экстракцию хлороформом повторяют еще два раза, объем раствора в колбе доводят до метки хлороформом, перемешивают и интенсивность окраски раствора определяют при помощи фотоэлектроколориметра ФЭК-56М со светофильтром № 5 (К ==- 490 нм) на фоне хлорофбрма в кювете с толщиной слоя 10 или 50 мм в зависимости от интенсивности окраски раствора. Количество платифиллина в пятне хроматограммы в мкг находят по калибровочному графику. Процентное содержание платифиллина в виде основания в абсолютно сухом сырье х вычисляют по формуле
~аУ100 • 5 • 100 Vim -1 ОООООО(ЮО-ш) '
где а—содержание алкалоидов в пятне хроматограммы, найденное по калибровочному графику, мг; V — объем хлороформного раствора, полученного при растворении сухого остатка, мл; Vx — объем хлороформного раствора, нанесенного на хроматограмму, мл; т — масса навески сырья, г; до — потеря массы сырья при высушивании, %.
Содержание платифиллина-основания должно быть не менее 0,3 %.
