Количественные характеристики процесса диссоциации.
1) Степень диссоциации (α % ) – это отношение числа молекул электролита, какие продиссоцировали (Nдис.), к общему числу растворенных молекул электролита (Nраств.).
α = Nдис. ∕ Nраств. ∙ 100, %
Сильные электролиты имеют степень диссоциации больше 50%.
Слабые электролиты имеют степень диссоциации меньше 50%.
Сильные электролиты диссоциируют | полностью, необратимо|необоротный|.
H2O
Ba(OH)2 → Ba2+ + 2OH-
Слабые электролиты диссоциируют | ступенчато, обратимо|обратимый|.
H2O
Fe(OH)2 ↔ FeOH+ + OH- I ступень
FeOH+ ↔ Fe2+ + OH- II ступень
2)Константа диссоциации ( Кдис.) – это отношение произведения концентрации ионов в растворе электролита к концентрации неразрушенных молекул.
H2O
NH4OH ↔ NH4+ + OH-
Кдис. = [NH4+] ∙ [OH-] ∕ [NH4OH]
Из выражения Кдис. понятно, что чем больше величина константы диссоциации, тем более диссоциированным является соединение.
НЕОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ КАК ЭЛЕКТРОЛИТЫ
ОСНОВАНИЯ|основание|
Основания– это электролиты, которые диссоциируют с отщеплением одной или нескольких анионов гидроксогрупп (ОН- ).
Основания|основание| – сильные электролиты ( сильные основания |основание|) – это основания|основание|, образованные металлами подгруппы лития и кальция
H2O
Sr(OH)2 → Sr2+ + 2OH-
Основания |основание| – слабые электролиты ( слабые основания|основание|) – это основания|основание|, образованные магнием и большинством d – металлов.
H2O
Ni(OH)2 ↔ NiOH+ + OH- I ступень
NiOH+ ↔ Ni2+ + OH- II ступень
КИСЛОТЫ
Кислоты– это электролиты, которые диссоциируют с отщеплением катионов Гидрогена ( Н+ ).
Сильные кислоты – это кислоты, которые имеют степень диссоциации больше 50%. Например: HNO3 , HCl, H2SO4 и тому подобное(смотри табл.«Степени диссоциации» ).
H2O
H2SO4 → 2H+ + SO42-
Слабые кислоты – это кислоты, которые имеют степень диссоциации меньше 50%. Например: H2CO3, H2S, HCN и тому подобное.
H2O
H2S ↔ H+ + HS- I ступень
HS- ↔ H+ + S2- II ступень
АМФОТЕРНЫЕ ГИДРОКСИДЫ
Амфотерные гидроксиды– это твердые, труднорастворимые электролиты, которые способны диссоциировать и как основания, и как кислоты. Все амфотерные гидроксиды – электролиты слабые.
Схема диссоциации по типу слабых основ|основания|аний
H2O
Zn(OH)2 ↔ ZnOH+ + OH-
ZnOH+ ↔ Zn2+ + OH-
Схема диссоциации по типу кислот
( происходят в щелочной среде).
H2O
Zn(OH)2 ≡ H2ZnO2 → 2H+ + ZnO22-
OH-
СОЛИ
Соли– это электролиты, которые диссоциируют на катионы металлов или основных остатков и анионы кислотных остатков. Все соли ведут себя в растворах как сильные электролиты.
H2O
Na2SO4 → 2Na+ + SO42-
средняя соль катионы металла анион кислотного остатка
H2O
CrOH(NO3)2 → CrOH2+ + 2NO3-
основная соль катион основного остатка анион кислотного остатка
H2O
Ca(HCO3)2 → Ca2+ + 2HCO3-
кислая соль катион металла анион кислотногоостатка
H2O
K3[ Fe(CN)6 ] → 3K+ + [ Fe(CN)6 ] 3-
комплексная соль катионы металла комплексный анион
Реакции в растворах электролитов происходят между ионами и потому называются ионнымиреакциями.
Ионные реакции записываются с помощью|посредством| трех уравнений:
а) молекулярного
б) полного ионно – молекулярного
в) сокращенного ионно – молекулярного.
а) СаСО3 + 2НСІ → СаСІ2 + Н2О + СО2
б) СаСО3 + 2Н+ + 2СІ- → Са2+ + 2СІ- + Н2О + СО2
в) СаСО3 + 2Н+ → Са2+ + Н2О + СО2
В ионных реакциях сильные растворимые электролиты записываются в виде ионов; вещества труднорастворимые|, газообразные и слабые электролиты, записываются в виде молекул. Ионные реакции происходят в том направлении, которое|какое| приводит к|до| связыванию ионов в вещества труднорастворимые|, газообразные, слабые электролиты. Если обозначенные вещества присутствуют и среди реагентов и среди продуктов, такие реакции являются обратимыми |обратимыми| (↔).
ВОДА
Общая масса воды на Земле составляет 1 • 10!* тонн. В том числе пресной воды 3%, что составляет 4 • 105 км3 , из которых 80% это вода ледников.
Тело человека вмещает ≈ 70% воды. Потеря 12% воды из тела человека приводит к|до| гибели.
Характер использования|употребления| водных ресурсов разделяется на:
а) многоразовое|многократное| ( океаны, моря, реки|речка|, озера) : транспорт, гидроэлектростанции, рыбная ловля , и тому подобное;
б) необратимое (2500 – 3000 км3 / год):
- домашнее хозяйство 10%
- промышленность 8 %
- сельское хозяйство 82%
Формы содержания |содержания| воды в веществах
1. Конституционная– входит в состав соединения. Выделяется после разложения вещества.
Са(ОН)2 → СаО + Н2О ↑ (пар)
2.Кристаллизационная– находится в пустотах кристаллических решеток веществ кристаллогидратов. Удаляется после нагревания выше 1000 С обратимо.
t0
СоСІ2 ∙ 6Н2О ↔ СоСІ2 + 6Н2О
Кристаллогидрат синий
розовый
3.Гигроскопическая– содержится поверхностью вещества. Химически не связанная. Удаляется обратимо при условиях уменьшения давления пара воды в воздухе даже при стандартных температурах.
Строение|стройка| молекулы воды
Тип химической связи в молекуле воды между атомами Оксигена и Гидрогена ковалентний полярный. По форме молекула воды представляет собой угол, в вершине которого находится атом Оксигена. При наличии личных двух пар спаренных электронов и смещенной от двух атомов Гидрогена электронной плотности, атом Оксигена имеет значительный отрицательный заряд. Атомы Гидрогена имеют положительные заряды. Таким образом, молекула воды представляет собой диполь.
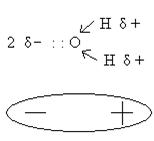
При большом количестве диполей они присоединяются друг к другу противоположно заряженными полюсами (межмолекулярная водородная связь), что вызывает специфические свойства воды, которые отличают ее от аналогов ( H2S , H2Se , H2Te, и тому подобное).
Физические свойства воды
| Вещество | Агрегатное состояние при стандартных условиях | Молекулярная масса | Температура плавления, 0 С | Температура кипения, 0 С |
| H2O | жидкость | |||
| H2S | газ | - 85,6 | - 60,3 | |
| H2Se | газ | - 65 | - 49 | |
| H2Te | газ | - 42 | - 2 | |
| H2Po | жидкость | - 36 | + 35 |
Плотность воды равняется 1 г / см3 при температуре 4 0 С . При температурах более высоких, а также и более низких плотность воды уменьшается. Плотность льда 0,9 г / см3 . Чистая вода практически не проводит электрический ток.
Вода как электролит
Вода– это амфотерний электролит ( амфолит). Диссоциация воды сопровождается образованием катионов Н+ и анионов ОН- .
Н2О ↔ Н+ + ОН-
Степень диссоциации воды равняется 2 • 10 - 9 %, то есть вода – электролит очень слабый.
Количественной характеристикой диссоциации слабых электролитов является константа равновесия процесса диссоциации, которая называется константой диссоциации
Кдис. = [ Н+]∙[ОН-] ∕ [Н2О] = const при T= const
Учитывая очень малую степень диссоциации воды, [Н2О] можно считать величиной постоянной.
Кдис. ∙ [Н2О] = К Н2О = [ Н+] ∙ [ОН-]
где К Н2О - ионное произведение води
К Н2О = Кдис. ∙ [Н2О] = 1,8 ∙ 10−16 ∙ 55,56 = 1 ∙ 10−14 ( моль ∕ л)2 = const
Таким образом, для воды и разбавленных водных растворов при постоянной температуре произведение концентрации ионов Гидрогена (Н+) и ионов ОН- - является величиной постоянной.
Для воды и нейтральных растворов
[ Н+] = [ОН-] = √ К Н2О = √ 10−14 = 10−7 моль ∕ л
Для растворов кислот, у каких ионов Н+ больше чем ОН-
[ Н+] > 10−7 ( 10−6 , 10−5 … 100 )
Для растворов щелочей, у каких ионов Н+ меньше чем ОН-
[ Н+] < 10−7 ( 10−8 , 10−9 … 10−14 )
Кислотность и основность | растворов можно определять с помощью|посредством| водородного показателя – рН| (пе| аш|), или с помощью|посредством| индикаторов.
рН = - lg [ Н+]
| Среда | Концентрация Н+, моль / л | рН |
| Нейтральная | [ Н+] = [ОН-] = 10−7 | |
| Кислая | [ Н+] > 10−7 ( 10−6 , 10−5 … 100 ) | < 7 |
| Щелочная | [ Н+] < 10−7 ( 10−8 , 10−9 … 10−14 ) | >7 |
Индикаторы– это вещества, которые изменяют свою окраску в зависимости от среды.
| Индикатор | Среда | ||
| кислая | нейтральная | щелочная | |
| метилоранж | красный | оранжевый | желтый |
| лакмус | красный | фиалковый | синий |
| фенолфталеин | бесцветный | бесцветный | розовый |
Значение рН| некоторых|некоих| веществ
| Кровь | 7,4 - 7,45 |
| Слюна | 6,35 – 6,85 |
| Желудочный сок | 0,9 – 1,1 |
| Слезы | 7,4 – 7,5 |
ЖЕСТКОСТЬ В О Д Ы
Вода, которую|какую| люди используют для питья и технологических потребностей, представляет собой очень разведенный раствор разнообразных|многообразных| солей. В результате|вследствие| диссоциации, соли находятся в воде в виде ионов: катионов металлов и анионов кислотных остатков.
Ионный состав воды предопределен химическим составом почвы|грунта|, сквозь которую|какой| проходит вода прежде чем|перед тем как| попадет в реки|речку| ( наземные или подземные), которые|какие| являются источником|истоком| водоснабжения населенных пунктов. При прохождении воды сквозь кальциевые и магниевые минералы, ионы этих металлов попадают в воду.
СаCO3 +H2O +CO2 → Ca(HCO3)2
известняк
Н2О
Ca(HCO3)2 → Ca2+ + 2HCO3-
Н2О
CaSO4 ∙ 2H2O → Ca2+ + SO42- + 2H2O
гипс
MgCO3 ∙ СаCO3 +2 H2O +2 CO2 → Mg2+ + 2HCO3- + Ca2+ + 2HCO3-
доломит
Н2О
KCl ∙ MgCl2 ∙ 6H2O → K+ + Mg2+ + 3Cl- + 6H2O
Вода, обогащенная ионами кальция и магния, называется жесткой.
Общая жесткость– это суммарное содержание солей кальция и магния в воде.
Карбонатная жесткость- это содержание в воде гидрогенкарбонатов кальция и магния.
Некарбонатная жесткость- это содержание в воде солей кальция и магния некарбонатной природы ( сульфатов, хлоридов, и тому подобное ).
Количественно жесткость воды измеряется числом миллимоль эвивалентов ионов Mg2+ та Ca2+ в литре воды ( Ж, мМЭ (Mg2+ + Ca2+) ∕ л )
В зависимости от содержания|содержания| ионов жесткости, воды бывают| :
мягкие Ж < 4 мМЭ / л
средней жесткости Ж от 4 до 8 мМЭ / л
жесткие Ж от 8 до 12 мМЭ / л
очень жесткие Ж > 12 мМЭ / л
Использования|употребления| в технологических процессах и быту|обиходе| жестких и очень жестких вод приводит к|до| повышению расходов электроэнергии, топлива, моющих средств. Поэтому жесткие воды нужно смягчать, то есть изымать из|с| них ионы кальция и магния.
Способы смягчения воды.
Кипячение.
t0
Ca(HCO3)2 → СаCO3 ↓ + H2O +CO2↑
накипь
Путем кипячения можно устранить лишь карбонатную жесткость . Поэтому она называется временной.
Соли, которые предопределяют некарбонатную жесткость, при кипячении в осадок не выпадают. Поэтому некарбонатная жесткость еще называется постоянной.
Реагентные способы
а) Известняковый ( для устранения карбонатной жесткости)
Ca(HCO3) + Ca(OH)2 à 2CaCO3↓ + 2H2O
гашеная известь
б) Содовый
Ca(Mg)Cl2 + Na2CO3 → Ca(Mg)CO3 ↓ + 2NaCl
сода кальцинированая
в) Фосфатный
3MgSO4 + 2Na3PO4 → Mg3(PO4)2 ↓ + 3 Na2SO4
фосфат натрия
Ионный обмен
Катионирование – воду пропускают через слой катионита – вещества, которое способно обменивать свои ионы Na+ или H+ на ионы Ca2+ и Mg2+ из воды.
ГИДРОЛИЗ СОЛЕЙ
Гидролиз– это есть процесс взаимодействия ионов соли с молекулами воды, в результате чего образуются слабые электролиты ( молекулы или ионы).
Образование в результате|вследствие| ионных реакций слабых электролитов возможно лишь|только| при условии наличия среди реагентов таких веществ, которые|какие| вмещают ионы, которые принадлежат слабым электролитам (слабым основаниям|основанию|, слабым кислотам ).
Соли– это продукт взаимодействия оснований с кислотами. В зависимости от природы оснований и кислот, которые образуют соли, последние можно разделить на такие типы :
1. Соль, которая образована сильным основанием|основанием| и сильной кислотой :
NaOH + HCl → H2O + NaCl
сильное сильная соль
основание|основание| кислота
2. Соль, которая образована слабым основанием|основанием| и сильной кислотой :
Mg(OH)2 + H2SO4 → 2H2O + MgSO4
слабое сильная соль
основа|основание|ние кислота
3. Соль, которая образована сильным основанием|основанием| и слабой кислотой :
2KOH + H2SO3 → 2H2O + K2SO3
сильное слабая соль
основание|основание| кислота
4. Соль, которая образована слабой основой|основанием| и слабой кислотой:
2NH4OH + H2CO3 → 2H2O + (NH4)2CO3
слабое слабая соль
основа|основание|ние кислота
Природа соли определяет характер взаимодействия ее ионов с молекулами воды, то есть вероятность гидролиза.
1. Соли, которые образованы сильными основаниями и сильными кислотами, гидролизу не подвергаются , потому что ионы таких солей образуют с молекулами воды сильные основания и сильные кислоты, которые полностью диссоциируют. Равновесие процесса смещено в сторону обратной реакции образования воды.
NaCl + H2O ↔ NaOH + HCl
Na+ + Cl- + H2O ← Na+ + OH- + H+ + Cl-
слабый электролит
Реакция среды таких растворов нейтральна. рН| = 7
2. Соли, которые образованы слабым основанием|основанием| и сильной кислотой гидролизуются по катиону :
2MgSO4 + 2H2O ↔ (MgOH)2SO4 + H2SO4
2Mg2+ + 2SO42- + 2HOH ↔ 2MgOH+ + SO42- + 2H+ + SO42-
Mg2+ + HOH → MgOH+ + H+
Среда таких растворов кислая. рН| < 7
3. Соли, которые образованы сильным основанием|основанием| и слабой кислотой гидролизуются по аниону :
K2SO3 + H2O ↔ KHSO3 + KOH
2K+ + SO32- + HOH ↔ K+ + HSO3- + K+ + OH-
SO32- + HOH → HSO3- + OH-
Среда таких растворов щелочная. рН| > 7
4. Соли, которые образованы слабым основанием|основанием| и слабой кислотой гидролизуются и по катиону и по аниону :
а) NH4CN + H2O → NH4OH + HCN
NH4+ + CN- + HOH → NH4OH + HCN
б) (NH4)2CO3 + H2O → NH4HCO3 + NH4OH
2NH4+ + CO32- + HOH → NH4+ + HCO3- + NH4OH
NH4+ + CO32- + HOH → HCO3- + NH4OH
в) Fe(CH3COO)2 + H2O → FeOHCH3COO + CH3COOH
Fe2+ + 2 CH3COO- + HOH → FeOH+ + CH3COO- + CH3COOH
Fe2+ + CH3COO- + HOH → FeOH+ + CH3COOH
г) Al2(CO3)3 + 6H2O → 2Al(OH)3 ↓ + 3 H2CO3
Реакции среды таких растворов определяются по сравнительным значениям степени диссоциации слабых оснований, кислот или ионов слабых электролитов (например HCO3- , FeOH+ и тому подобное).
Гидролиз солей, которые образованы многозарядными ионами, происходит ступенчато.Число ступеней| равняется заряду иона. Реально гидролиз происходит преимущественно по первой ступени|. Вторую и следующие ступени| следует учитывать лишь|только| при очень сильном разведении растворов.
Количественное оценивание глубины гидролиза делается по значению константы гидролиза.
Для условного обратимого|обратимого| процесса:
Me+nAm- + mn H2O ↔ mMe(OH)n+ nHmA
Me+A- + H2O ↔ MeOH + HA
где Ме+ - катион слабого основания
А- - анион слабой кислоты
Константа равновесия имеет вид :
[МеОН] · [НА]
Кравн. = -------------------- ( 1 )
[МеА] · [Н2О]
Концентрация воды в разведенных растворах величина постоянная. Поэтому произведение Кравн. · [Н2О] тоже является величиной постоянной и называется константой гидролиза.
Исходя из уравнения ( 1 ) :
[МеОН] · [НА]
Кгидр. = -------------------- ( 2 )
[МеА]
Из|с| выражения ( 2 ) делаем вывод : чем больше значение константы гидролиза соли, тем в большей мере соль подлежит гидролизу.
Процессы гидролиза солей следует учитывать в лабораторной, аналитической практике, в процессах химической технологии, в процессах затвердевания |затвергидравлических вяжущих веществ, и тому подобное.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
[ Co(NH3)4Cl2]NO3
Согласно теории Вернера (1891р|.) комплексные соединения состоят из внешней сферы и комплексного иона.
Внешняя сфера– это группа атомов вне квадратных скобок.
Комплексный ион– это группа атомов в квадратных скобок.
Комплексный ион состоит из центрального атома ( или иона) и лигандов. Центральный атом (ион) называется комплексообразователем. Роль комплексообразователя чаще выполняют атомы металлов ( в состоянии Ме0 или Меn+).
Лиганди– это молекулы, или ионы кислотных остатков, которые соединяются с комплексообразователем чаще с помощью донорно – акцепторной химической связи. Донорно – акцепторная связь – это связь, при реализации которой обобщенная электронная пара образуется путем размещения электронной пары одного атома (донора) на электронной орбитали второго атома (акцептора).
Схема образования комплексного иона [ Zn(NH3)4]2+
| ↑↓ | |||||||
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | |||
| ↑↓ | ↑↓ | ↑↓ | |||||
| ↑↓ | |||||||
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | |||
| ↑↓ | ↑↓ | ↑↓ | |||||
| ↑↓ |
Zn0
Zn2+
3
s p d f
H
. .
NH3 4 H : N : ↑↓
. .
H
[Zn(NH3)4]2+
| ↑↓ | ↑↓ | ↑↓ | |||||
| ↑↓ | |||||||
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | |||
| ↑↓ | ↑↓ | ↑↓ | |||||
| ↑↓ |
s p d f
Процесс соединения лиганд с комплексообразователем называется процессом координации. В приведенном примере акцептором электронных пар является ион Zn2+ Он называется комплексообразователем или центром координации, или центральным атомом.
Молекулы NH3 – лиганды, координированные центральным атомом. Донором электронных пар является Нитроген. Каждая координированная группа может занимать около центрального атома одно или несколько координационных мест ( по числу электронных пар). Число электронных пар, которые лиганд отдает для образования связи с комплексообразователем называется координационной емкостью лиганд или дентатностью лиганд. Монодентатные лиганды – предоставляют одну электронную пару ( однозарядные ионы кислотных остатков, молекулы аммиака, воды, гидроксогруппи и тому подобное ). Полидентатные (бидентатные, тридентатные и больше ) лиганды – многозарядные ионы кислотных остатков (C2O42- ; СО32- ; SO42- ; SO32- ; PO43- ) молекулы органических соединений.
Общее число электронных пар донора, которые атом комплексообразователь размещает на своих орбиталях ( координирует) называется координационным числом комплексообразователя.
Так, в соединении Na3[CoC2O4(NO2)4] координационное число кобальта (Со3+) равняется шести, потому что ион NO2- монодентатный, а ион C2O42- - бидентатный.
