Атомно-абсорбційний спектральний аналіз
Атомно-абсорбційний спектральний метод аналізу запропонував у 1955р. Уолш.
Суть цього методу полягає у наступному.
При поглинанні кванта світла hν вільний атом А переходить у збуджений стан А*:
A + hν = A*,
де h – постійна Планка;
ν – частота, яка визначається умовою частот Бора,

де  і
і  – енергія атома в збудженому і основному станах відповідно.
– енергія атома в збудженому і основному станах відповідно.
Найбільш вірогідною зміною енергетичного стану атома при збудженні є його перехід на рівень, найближчий до основного енергетичного стану, тобто резонансний перехід. Якщо на незбуджений атом направити випромінювання з частотою, що дорівнює частоті резонансного переходу, кванти світла будуть поглинатися атомами і інтенсивність випромінювання буде зменшуватися. Ці явища лежать в основі атомно-абсорбційної спектроскопії. Таким чином, якщо в емісійній спектроскопії концентрація речовини визначається за інтенсивністю випромінювання, яке прямо пропорційне числу збуджених атомів, то в атомно-абсорбційній спектроскопії аналітичний сигнал (зменшення інтенсивності випромінювання) пов’язаний з числом незбуджених атомів.
На основі розрахунків випливає, що число атомів у збудженому стані незначне у порівнянні з числом атомів на основному (нижньому) рівні і не перевищує 1-2% від загального числа атомів. У зв’язку з цим атомно-абсорбційний аналіз вигідно відрізняється від емісійного, оскільки за рівних умов величина аналітичного сигналу пов’язана з більшим числом атомів, ніж в емісійній спектроскопії, а це означає, що величина сигналу у меншій мірі залежить від випадкових коливань в режимі роботи вузлів атомно-абсорбційного спектрофотометра.
Як джерело випромінювання в атомно-абсорбційній спектроскопії використовують здебільшого лампу з катодом, який містить досліджуваний елемент. Катод такої лампи виготовляють у вигляді металічного стаканчика, в якому відбувається випаровування речовин і збудження атомів елементів внаслідок електричного розряду в атмосфері інертного газу під невеличким тиском. Катоди, виготовлені з елементів з відносно низькими температурами плавлення, легко руйнуються. Для визначення таких елементів використовують графітові катоди, просочені солями елементів, які визначаються. Анод у вигляді металічного стрижня розміщують поряд з катодом і обидва електроди вміщують у скляний балон зі скляним або кварцовим віконцем. Лампа живиться струмом від високоточного випрямляча-стабілізатора, який дає напругу 500-600В з коливаннями, які не перевищують сотих часток відсотка.
Пара матеріалу катода та інших речовин, що знаходяться на внутрішній поверхні катода, попадають у плазму внаслідок катодного розпилювання і випаровування у процесі розряду при напрузі 200-300В і силі струму 5-30мА. У спектрі свічення при температурі близько 800К у порожнинному катоді спостерігаються резонансні частоти цих елементів.
Зменшення інтенсивності резонансного випромінювання в умовах атомно-абсорбційної спектроскопії підпорядковується експоненціальному закону спаду інтенсивності в залежності від довжини шару і концентрації речовини, що аналогічний закону Бугера-Ламберта-Бера. Якщо І0 – інтенсивність падаючого монохроматичного світла, а І – інтенсивність цього світла після проходження крізь полум’я, то величину 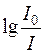 можна назвати оптичною густиною. Залежність оптичної густини від концентрації досліджуваної речовини виражається рівнянням:
можна назвати оптичною густиною. Залежність оптичної густини від концентрації досліджуваної речовини виражається рівнянням:

де k– коефіцієнт поглинання світла;
l – товщина світлопоглинаючого шару (полум’я)
c – концентрація.
Згідно рівняння, оптична густина прямо пропорційна концентрації речовини. Проте, у дійсності виявляється, що залежність оптичної густини від концентрації не завжди буває строго лінійною. Відхилення від лінійності викликано різними причинами, серед яких найбільш суттєвими є нестабільність роботи спектрофотометра, немонохроматичність ліній емісії, викликана зверхтонкою структурою, утворення у полум’ї різних сполук досліджуваного елемента з киснем чи супутніми елементами та ін. Тому у практиці аналізу здебільшого застосовують метод градуювального графіка або метод добавок.
У методі градуювального графіка вимірюють оптичну густину декількох стандартних розчинів і будують графік у координатах: оптична густина – концентрація. Потім у тих же умовах визначають оптичну густину досліджуваного розчину і за градуювальним графіком знаходять її концентрацію.
За методом добавок спочатку вимірюють оптичну густину DХ, потім у досліджуваний розчин вводять певний об’єм стандартного розчину і знову вимірюють оптичну густину D(Х+стандарт). Якщо c(Х) – концентрація досліджуваного розчину, а c(стандарт) – стандартного, то:
Dx = k·l·c(Х); D(Х+стандарт) = k·l·(c(Х)+c(стандарт)).
Враховуючи, що k і l однакові, маємо:
 .
.
Звідки:

Методи атомно-абсорбційної спектроскопії використовуються для аналізу практично будь-якого технічного чи природного об’єкту, особливо там, де необхідно визначити незначний вміст елементів. Методики атомно-абсорбційного визначення розроблені більш ніж для 70 елементів, зокрема Mg, Zn, Cu, Ca, Pb, Fe, Ag, Ni, Hg, Cd, Bi та ін. За цим методом аналізують метали, сплави, різні концентрати. Наприклад, у золоті визначають вміст срібла, свинцю, міді і цинку при їх наявності 10–4%. Ці методики застосовуються для визначення Zn, Fe, Mg, Cu та ін. елементів у ґрунтах, добривах, рослинах та інших об’єктах при вмісті елементів порядку
10–4-10–5%. Атомно-абсорбційний метод застосовується також у клітинних і біологічних аналізах на Плюмбум, Меркурій, Бісмут, Кадмій та інші елементи.
Атомно-абсорбційним методом не можна визначити елементи, резонансні лінії яких лежать у далекому ультрафіолеті (Карбон, Фосфор, галогени та ін.).
Суттєвим недоліком метода є неможливість одночасного визначення декількох елементів.
