Методы титриметрического анализа
Титриметрический анализ можно проводить двумя методами: методом отдельных навесок и методом пипетирования.
Метод отдельных навесок. На аналитических весах берут 5-6 навесок определяемого вещества А, каждую из которых растворяют в небольшом количестве дистиллированной воды, и полученные растворы титруют раствором титранта. Массу анализируемого вещества для каждой отдельной навески рассчитывают по формуле
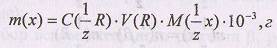
Из среднего арифметического всех найденных значений определяют содержание анализируемого вещества и рассчитывают погрешность.
Метод пипетирования (метод аликвот).Метод пипетирования заключается в том, что на титрование отбирают пипеткой только часть анализируемого раствора Va. Навеску анализируемого вещества растворяют в мерной колбе объемом VK. Массу навески рассчитывают таким образом,
чтобы она была в (VK / Va.) раз больше, чем масса определяемого вещества, необходимая на отдельное титрование.
Следовательно, при расчете массы по результатам титрования
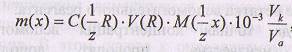
По сравнению с методом отдельных навесок в методе пипетирования существуют дополнительные случайные отклонения, возникающие в результате погрешностей измерения объемов пипетки и мерной колбы, в которой готовят стандартный раствор. Кроме того, ошибка при взвешивании определяемого вещества может привести к неверным результатам за счет систематической погрешности. Однако ввиду большей длительности и трудоемкости определения по методу отдельных навесок на практике чаще используют метод пипетирования.
В основе кислотно-основного титрования положена реакция взаимодействия ионов водорода или гидроксония с гидроксид-ионами:
Н+ + ОН- = Н2О, Н3О+ + ОН- = 2Н2О
При помощи этого метода определяют кислоты, основания, соли, способных гидролизоваться в водных растворах, а также их смеси, азот, серу в органических соединениях, некоторые органические соединения (формальдегид, спирты и др.).
В качестве титрантов в кислотно-основном титровании применяют в основном растворы сильных кислот (НС1, Н2SО4) и сильных оснований (КОН, NaOH).
В зависимости от природы титранта кислотно-основное титрование включает два основных метода: ацидиметрия и алкалиметрия. В ацидиметрии титрантом служит раствор кислоты, а применяют ее для определения различных оснований. В алкалиметрии титрант - раствор щелочи, а применяется для определения кислот,
Титранты кислотно-основного титрования относятся к титрантам второго типа - стандартизированные или с установленным титром. В качестве исходных веществ для установления титра рабочих растворов кислот используют тетраборат натрия (Na2B4O7*10H2O) или карбонат натрия безводный (Na2CO3), а для установления титра растворов щелочей – щавелевую (Н2С2О4*2Н2О) или янтарную (Н2С4Н4О4) кислоту.
Кислотно-основное титрование не сопровождается внешним эффектом, а лишь изменением рН. Реакция среды в точке эквивалентности определяется природой взаимодействующих кислот и оснований.
В кислотно-основном методе титрования различают три случая титрования:
1. Титрование сильной кислоты сильной щелочью и наоборот:
НСl + NaOH = NaCl + H2O; H+ + OH- = H2O
Точка эквивалентности находится в нейтральной среде (рН=7), т.к. образующаяся соль не подвергается гидролизу.
2. Титрование слабой кислоты сильной щелочью:
СН3СООН + NaOH = CH 3COONa + H2O
В ионном виде:
СН3COOH + OH- = CH3COO- + H2O
В точке эквивалентности образуется соль слабой кислоты и сильного основания, которая вступает в реакцию гидролиза:
СH3COONa + HOH ↔ CH3COOH + NaOH
В ионном виде:
СН3СОО- + НОН ↔ СН3СООН + ОН-
В растворе накапливаются ионы ОН- и точка эквивалентности будет находиться в щелочной среде (рН > 7 ), не совпадая с точкой нейтральности.
3. Титрование слабого основания сильной кислотой:
NH4OH + HCl = NH4Cl + H2O
В ионном виде:
NH4OH + H+ = NH4+ + H2O
Образующаяся соль слабого основания и сильной кислоты (NH4Cl) подвергается гидролизу, и в растворе накапливаются ионы Н+, что вызывает смещение точки эквивалентности в кислую среду. Следовательно, и в третьем случае точка эквивалентности не совпадает с точкой нейтральности.
Поскольку кислотно-основное титрование не сопровождается внешним эффектом, например, изменением окраски, для фиксирования точки эквивалентности применяют индикаторы
Согласно протолитической теории к кислотам относятся химические соединения, способные в растворах отдавать протоны, а к основаниям вещества, способные присоединять протоны. Для того чтобы кислота могла отдать протон, необходимо присутствие основания, принимающего этот протон. Отдавая протон, кислота образует сопряженное с ней основание, а основание, принимая протон, образует сопряженную с ним кислоту.
В водных растворах кислот имеет место следующее равновесие:
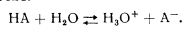
В воде, которая является кислотой и основанием одновременно и представляет собой слабый электролит устанавливается равновесие
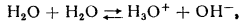
в сокращенном виде
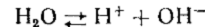 |
Константа равновесия этой реакции при температуре 25° С равна
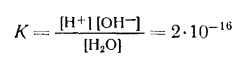 |
В водных растворах масса воды в большинстве случаев очень велика по сравнению с массой растворенного вещества, количество ее в 1 л раствора можно считать постоянным. Тогда выражение для константы равновесия запишется следующим образом:
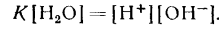
Из уравнения следует, что ионное произведение является величиной постоянной при постоянной температуре. Эту константу называют ионным произведением воды, которое при температуре 25° С равно

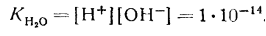
В чистой воде
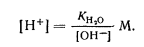 |
При избытке [ОН-]
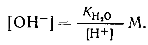 |
При избытке [Н + ]
Концентрацию водородных ионов обычно используют для характеристики среды. В большинстве расчетов, относящихся к кислотно-основному равновесию, концентрации (и другие величины) удобно выражать в виде отрицательных логарифмов этих величин, обозначаемых знаком „р". Тогда
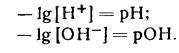 |
