Задача. Какую массу оксида кальция можно получить при термическом разложении 600 г известняка, содержащего 10% примесей?
Лабораторная работа №2.
«Ознакомление со свойствами смесей и дисперсных систем»
Цель: исследовать свойства дисперсных систем.
Реактивы и оборудование: сборник задач, Периодическая система химических элементов Д.И. Менделеева.
Теоретические основы
Дисперсные (раздробленные) системы являются гетерогенными, в отличие от истинных растворов (гомогенных). Они состоят из сплошной непрерывной фазы – дисперсионной среды и находящихся в этой среде раздробленных частиц того или иного размера и формы – дисперсной фазы.
Обязательным условием существования дисперсных систем является взаимная нерастворимость диспергированного вещества и дисперсионной среды.
Дисперсные системы классифицируют:
1. по степени дисперсности;
2. по агрегатному состоянию дисперсной фазы и дисперсионной среды;
3. по интенсивности взаимодействия между ними;
4. по отсутствию или образованию структур в дисперсных системах.
В зависимости от рамеров частиц дисперсной фазы дисперсные системы бывают в виде взвесей и коллоидов.
Взвеси (размер дисперсной фазы более 100нм) ─ эмульсии, суспензии, аэрозоли.
Коллоидные растворы (размер дисперсной фазы от 1 до 100нм) – гели, золи.
Агрегатное состояние дисперсных систем бывает разным и обозначается двумя буквами.
Например: аэрозоль обозначается Г-Ж.
Г – газообразная дисперсионная среда, Ж – жидкая дисперсная фаза.
Моль – единица измерения количества вещества.
n[моль]
1 моль любого вещества имеет массу, численно равную Mr, но имеющую единицу измерения г/моль. Эта масса называется молярной, обозначается М.
Mr = M [г/моль]
Количество вещества и масса связаны соотношением:
n = m/М
Количество вещества и число структурных единиц N связаны соотношением:
n = N/NA
Молярный объем газов (Vm)
V = m/p --- Vm=M/p
Vm = 22,4 л/моль
n =V/Vm
Типовой пример решения задачи
Задача. Какую массу оксида кальция можно получить при термическом разложении 600 г известняка, содержащего 10% примесей?
| Последовательность действий | Пример выполнения действий |
| 1.Запишите условие и требование задачи с помощью общепринятых обозначений | Дано: m(СаСО3)=600г W(примесей)=10% Найти: m(CаO)-? |
| 2.Составьте уравнение химической реакции | Решение: СаСО3 = СаО+СО2 |
| 3.В уравнении подчеркните формулы веществ, которые записаны в «Дано» и «Найти» | СаСО3 = СаО+СО2 |
| 4.Найдите массу чистого вещества (освободиться от примесей) | 600г - 100% Х г - 10% Х= 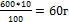 - масса примесей, Тогда масса чистого СаСО3 равна 600-60=540г - масса примесей, Тогда масса чистого СаСО3 равна 600-60=540г |
| 5.Под подчеркнутыми формулами подпишите по коэффициентам «моли» | СаСО3 = СаО+СО2 1 моль 1 моль |
| 6.Вычислите количество вещества n, которое записано в «Дано». Для расчета берите уже массу чистого вещества | 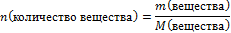 n(СаСО3) = n(СаСО3) = 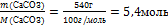 |
| 7.Подпишите найденное n под формулой этого вещества | СаСО3 = СаО+СО2 1 моль 1 моль 5,4 моль |
| 8.Под формулой вещества, массу которого надо найти, поставьте х моль | СаСО3 = СаО+СО2 1 моль 1 моль 5,4 моль х моль |
| 9.Из полученной пропорции выразите х | 1 моль 1 моль 5,4 моль х моль х = 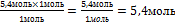 – это количество вещества n(СаО) – это количество вещества n(СаО) |
| 10.Зная n( CаО) найдите массу CаO | m=nM m(CаO)= n (CаO) 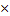 M (СаО) M (CаО) =40+16=56г/моль m(СаО)=5,4 M (СаО) M (CаО) =40+16=56г/моль m(СаО)=5,4 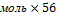 г/моль=302,4г г/моль=302,4г |
| 11.Запишите ответ | Ответ: m(СаО)=302,4г |
Ход работы:
Задание. Решите задачи.
