Фазовые диаграммы состояния двухкомпонентных систем
Диаграмма состояния - графическое изображение зависимости какого-либо свойства системы от ее состава. Диаграммы состояния строят по экспериментальным данным в координатах температура – состав. Они широко применяются при изучении различных минералов, силикатных систем, горных пород, металлических сплавов, водных растворов солей и др.
К основным типам диаграмм состояния двухкомпонентных конденсированных систем относятся:
· диаграмма с простой эвтектикой;
· диаграмма с образованием устойчивого химического соединения (конгруэнтно плавящегося);
· диаграмма с образованием неустойчивого химического соединения (инконгруэнтно плавящегося);
· диаграмма с неограниченной взаимной растворимостью компонентов в твердом состоянии;
· диаграмма с ограниченной растворимостью компонентов в твердом состоянии (I и II вида);
· диаграмма с ограниченной взаимной растворимостью компонентов в жидком состоянии.
Для таких систем при р = const, правило фаз Гиббса имеет вид:
С = 3 - Ф
2.3.1. Диаграмма состояния системы с эвтектикой
Является наиболее простой диаграммой состояния, в которой компоненты неограниченного смешиваются друг с другом в жидком состоянии. Однако совершенно не смешиваются в твердом состоянии, химически не взаимодействуют друг с другом и не образуют твердых растворов.
Диаграмма состояния системы с простой эвтектикой для компонентов А и В схематически представлена на рис.1.
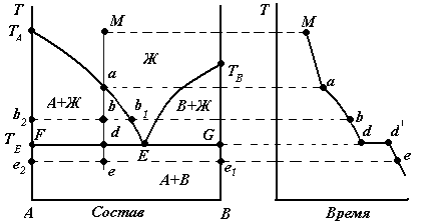
Рис.1. Диаграмма состояния с эвтектикой
ТАЕ – линия ликвидуса (каждая точка на линии показывает состав расплава, который находится в равновесии с кристаллами А);
ТВЕ – линия ликвидуса (в равновесии с кристаллами В);
FEG – линия солидуса (линия эвтектики);
Рассмотрим процесс охлаждения расплава, заданного точкой М.
| Точка | Что происходит | Ф | С | Что означает число степеней свободы |
| М | Охлаждение расплава | Можно менять температуру и состав расплава | ||
| а | Появляются первые кристаллы компонента А | Можно менять только температуру | ||
| b | Продолжают выпадать кристаллы компонента А, состав расплава b1, состав твердой фазы b2 | Можно менять или температуру или состав расплава | ||
| d | Одновременно кристаллизуются компоненты А и В, на кривой охлаждения участок d-d’ | Система инвариантна | ||
| e | Охлаждение механической смеси компонента А состава е2 и компонента В состава е1 | Можно менять только температуру |
Соотношение между количеством твердой и жидкой фаз определяется по правилу рычага. Например, смесь в точке b соответствует начальному составу 40% А и 60% В, то при температуре Та она представляет собой гетерогенную систему из кристаллов вещества А и жидкой фазы. Для определения состава этих фаз проводят горизонталь b2b1 через точку b до пересечения с границами области (длина рычага). Определить количество кристаллической фазы и жидкого расплава можно по соотношению:
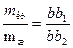
2.3.2. Фазовая диаграмма с конгруэнтно плавящимся химическим соединением
Если компоненты А и В образуют одно устойчивое химическое соединение состава АхВy, плавящееся без разложения, то на диаграмме состояния кривая ликвидуса образует максимум в точке Д (рис.2). В этой точке состав кристаллической фазы совпадает с составом жидкой фазы. В случае, если максимум на диаграмме имеет острую форму, химическое соединение АхВy устойчиво при плавлении; если максимум «пологий», то химическое соединение частично диссоциирует при плавлении.
Как видно из рис.2, фазовая диаграмма представляет собой как бы две диаграммы с простой эвтектикой: А-АВ и В-ВА. Можно разделить такую диаграмму на две части по вертикали, соответствующей химическому соединению, и рассматривать каждую часть диаграммы отдельно.
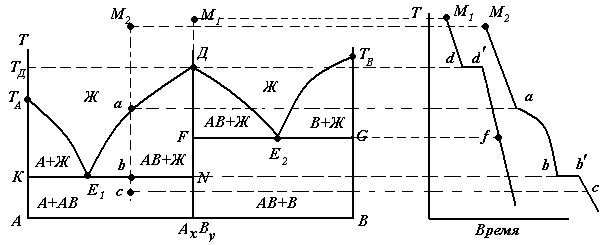
Рис.2. Диаграмма состояния системы с образованием химического соединения, плавящимся без разложения (конгруэнтно)
Состав химического соединения АхВy в точке Д можно определить, зная состав соединения в молекулярных или массовых процентах.
А).Состав компонентов А и В выражен в мольных процентах:
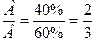 , состав химического соединения А2В3;
, состав химического соединения А2В3;
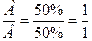 , состав химического соединения АВ .
, состав химического соединения АВ .
Б).Состав компонентов А и В выражен в массовых процентах:
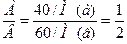 , состав химического соединения АВ2 .
, состав химического соединения АВ2 .
Рассмотрим процесс охлаждения расплава, заданного точками М1 и М2. Точка М1 отвечает составу конгруэнтно плавящегося химического соединения АхВy. Число независимых компонентов системы, образованных из одного химического соединения АхВy, равно единице и число степеней свободы в этом случае равно: С=К – Ф + 1 = 1 – Ф + 1 = 2 - Ф.
| Точка | Что происходит | Ф | С | Что означает число степеней свободы |
| М1 | Охлаждение расплава | Можно менять только температуру | ||
| Д | Появляются первые кристаллы компонента АхВy | Система инвариантна | ||
| F | Охлаждается твердая фаза химического соединения АхВy | Можно менять только температуру |
Рассмотрим процесс охлаждения расплава, заданного точкой М2.
| М2 | Охлаждение расплава | Можно менять температуру и состав расплава | ||
| а | Появляются первые кристаллы компонента АхВy | Можно менять только температуру | ||
| b | Кристаллизуются компонент А и химическое соединение АхВy | Система инвариантна | ||
| с | Охлаждение механической смеси А и АхВy | Можно менять только температуру |
2.3.3. Фазовая диаграмма с инконгруэнтно плавящимся химическим соединением
Диаграмма, когда компоненты А и В могут образовывать химическое соединение АхВy, плавящееся с разложением, т.е. инконгруэнтно, приведена на рис.3.
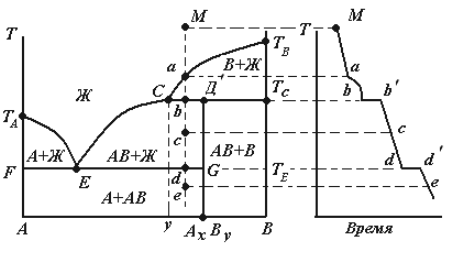
Рис.3. Диаграмма состояния системы с образованием химического соединения, плавящимся с разложением (инконгруэнтно)
Инконгруэнтно плавящееся химическое соединение АхВy устойчиво только ниже температуры Тc. При повышении температуры выше Тc химическое соединение распадается на две фазы: кристаллы компонента В и расплав состава y (точка С). На перитектической прямой СДТc в равновесии находятся три фазы:
- расплав состава точки С ( CL );
- кристаллы АхВy состава точки Д;
- кристаллы компонента В.
По правилу фаз Гиббса число степеней свободы в точке С равно нулю (С = 3 - Ф = 3 - 3 = 0), что указывает на постоянство температуры Тс и состава расплава. Чтобы состав расплава не менялся, одновременно с кристаллизацией АхВy ранее выпавшие кристаллы компонента В должны растворяться, поддерживая постоянным содержание компонента В в расплаве. При этом происходит перитектическое превращение: Lc + В  АхВy.
АхВy.
Точка С называется точкой перитектики, температура Тс - температурой перитектики. В точке перитектики, так же как и в точке эвтектики, в равновесии находятся расплав и две твердые фазы. Однако процессы при охлаждении существенно различаются: в точке эвтектики одновременно кристаллизуются две твердые фазы, а в точке перитектики – одна твердая фаза кристаллизуется, а другая растворяется. На кривой охлаждения при Тс наблюдается горизонтальный участок b-b’.
Рассмотрим процесс охлаждения расплава, заданного точкой М.
| Точка | Что происходит | Ф | С | Что означает число степеней свободы |
| М | Охлаждение расплава | Можно менять температуру и состав расплава | ||
| а | Появляются первые кристаллы компонента В | Можно менять или температуру или состав расплава | ||
| b | Начинается кристаллизация хим. соединения АхВy, ранее выпавшие кристаллы компонента В растворяются, на кривой охлаждения горизонтальный участок b-b’ | Система инвариантна | ||
| с | Продолжается кристаллизация АхВy из расплава | Можно менять или температуру или состав расплава | ||
| d | Кристаллизуются компонент А и химическое соединение АхВy, на кривой охлаждения горизонтальный участок d-d’ | Система инвариантна | ||
| е | Охлаждение механической смеси А и АхВy | Можно менять только температуру |
