Химическая связь и химические свойства элементов
В наиболее общем виде образование химической связи происходит путем спаривания двух электронов, принадлежащих различным атомам. При этом возникает общая электронная пара (молекулярная орбиталь - МО), которая связывает эти атомы. Если МО имеет симметричное распределение электронной плотности, возникающая связь называется КОВАЛЕНТНОЙ НЕПОЛЯРНОЙ (молекулы Н2, N2, О2, I2 и т.п.).
При смещении электронной плотности к ядру одного из атомов образуется КОВАЛЕНТНАЯ ПОЛЯРНАЯ связь (НСl, Н20, С02 и др.). При значительном смещении электронной плотности связь называют ИОННОЙ (NaCl, КВг, СаО и др.).
Способность атома смещать к себе электронную плотность МО оценивается величиной его электроотрицательности (ЭО)
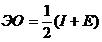 ,
,
где I - энергия ионизации атома, кДж/моль;
Е - сродство атома к электрону, кДж/моль.
ЧЕМ БОЛЬШЕ РАЗНОСТЬ ЭО АТОМОВ ВЗАИМОДЕЙСТВУЮЩИХ ЭЛЕМЕНТОВ, ТЕМ СИЛЬНЕЕ СМЕЩЕНИЕ ЭЛЕКТРОННОЙ ПЛОТНОСТИ К АТОМУ БОЛЕЕ ЭЛЕКТРООТРИЦАТЕЛЬНОГО ЭЛЕМЕНТА, ТЕМ ВЫШЕ ПОЛЯРНОСТЬ СВЯЗИ. С ДРУГОЙ СТОРОНЫ, ЧЕМ ВЫШЕ ПОЛЯРНОСТЬ СВЯЗИ, ТЕМ БОЛЕЕ СПОСОБНА ДАННАЯ ХИМИЧЕСКАЯ СВЯЗЬ К ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ В РАСТВОРАХ.
Для качественной оценки образующейся связи используют не абсолютные значения ЭО, а относительные (ОЭО). Если ЭО лития - 536 кДж/моль - принять за единицу, получают шкалу ОЭО элементов (приложение, табл. 1)
ПРИМЕР 6
Написать электронную формулу для атома элемента N 17 в нормальном и возбужденных состояниях. Указать возможные степени окисления, написать формулы оксидов и гидроксидов для низшей и высшей степеней окисления. По значениям ОЭО рассчитать полярность связей и определить возможный тип диссоциации (кислотный или основный) этих гидроксидов в водных растворах.
РЕШЕНИЕ
Элемент N 17 - это элемент третьего периода - хлор. Его электронная формула в нормальном состоянии
1s22s22p63s23p5.
Поглощая энергию извне, атом хлора может переходить в возбужденное состояние, при этом валентные электроны в пределах одного слоя распределяются по одному в АО (ячейках)

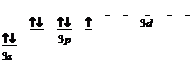
нормальное состояние

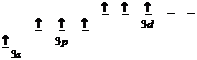
возбужденное состояние
Таким образом, в возбужденном состоянии атом хлора имеет семь не спаренных электронов на внешнем уровне и может иметь степени окисления: +1+2+3+4+5+6+7. Низший оксид: Cl2O, высший - Cl2O7. Их гидроксиды: HOCl, HClO4.
Все гидроксиды имеют одинаковый фрагмент молекулы Н-О-Э, в данном случае Н-1О-2Cl.
Используя значение ОЭО (см. приложение, табл.1), рассчитаем условия полярности связей 1 и 2
∆ОЭО(1)=ОЭО (О) – ОЭО (Н)= 3,5-2,1 = 1,4;
∆ОЭО(2)=ОЭО (О) – ОЭО (Cl)= 3,5-3,0 = 0,5.
Связь 1 более полярна (∆ОЭО(1) > ∆ОЭО(2)), следовательно, она с большей вероятностью будет разрываться в водных растворах и диссоциация гидроксидов будет происходить следующим образом: HСlO=H++ClО-; HClO4= H++ClO4-. Это кислоты.
Помимо значений ОЭО, тип электролитической диссоциации химической связи зависит от степени окисления элемента. Чем она выше, тем сильнее проявляются кислотные свойства гидроксида, поэтому HClO4 диссоциирует сильнее, чем HСlO.
