Физические и химические свойства металлов. Химическая связь в металлах
Металлы – особый класс веществ, обладающих комплексом свойств: высокой электропроводимостью и теплопроводностью, ковкостью и пластичностью, металлическим блеском и высокой отражательной способностью к свету [1,3-5,8,10,14].
Плотность большинства металлов значительна. Это говорит об очень плотной структуре металлических кристаллов. Высокие ковкость и пластичность указывают на отсутствие жесткости в металлических решетках, их плоскости довольно легко движутся относительно друг друга. Высокая электропроводимость и теплопроводность обеспечиваются большой подвижностью электронов в их пространственной структуре. Металлический блеск обусловлен отражением световых лучей от электронов.
К общим химическим свойствам можно отнести:
1) малую электроотрицательность как следствие низких энергий ионизации и малого сродства к электрону;
2) атомы металла – восстановители, отдавая электроны, образуют только положительные ионы;
3) в сложных ионах или полярных молекулах атомы металла всегда образуют положительные центры.
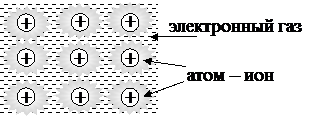 Химическая связь в металлах. Кристаллическая решетка металла есть система атомов, определенным образом расположенных в пространстве; состоит из большого числа атомов, представляющих собой сложные энергетические поля, действующие друг на друга (рис. 9.1).
Химическая связь в металлах. Кристаллическая решетка металла есть система атомов, определенным образом расположенных в пространстве; состоит из большого числа атомов, представляющих собой сложные энергетические поля, действующие друг на друга (рис. 9.1).
Рис. 9.1. Схема изображениякристаллической решетки металла
Вследствие малой плотности электронов на внешнем уровне (1-2), атомы металла легко сближаются и обобщают электроны. Валентные электроны с небольшой энергией ионизации свободно перемещаются по вакантным орбиталям всех соседних атомов, обеспечивая связь между ними, т.е. являются нелокализованными. Совокупность свободных электронов иногда называют «электронный газ». Таким образом, в узлах кристаллической решетки находятся положительные ионы металла, а валентные электроны передвигаются между ними в различных направлениях.
Типы кристаллических структур металлов,
Их характеристика
Тип кристаллической системы определяется природой частиц, видом химической связи и т.д. В каждой пространственной решетке можно выделить структурный элемент минимального размера, который называется элементарной ячейкой. Из более чем 80 элементов в таблице Д. И. Менделеева 53 металла кристаллизуются в виде одного из трех типов кристаллических решеток (рис. 9.2).
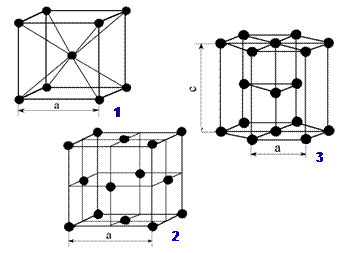
Рис. 9.2. кристаллические решетки, характерные для металлов:
1 – объемно-центрированная кубическая решетка; 2 – гранецентрированная кубическая решетка; 3 – гексагональная плотноупакованная решетка
На рис. 9.2 приведены примеры простых кристаллических решеток. В простой кубической решетке частицы располагаются в вершинах куба. В гранецентрированной решетке (ГЦК) частицы располагаются не только в вершинах куба, но и в центрах каждой его грани. В объемно-центрированной кубической (ОЦК) решетке дополнительная частица располагается в центре каждой элементарной кубической ячейки. Гексагональная плотноупакованная ячейка (ГПУ) состоит из отстоящих друг от друга параллельных центрированных гексагональных оснований. Три атома находятся на средней плоскости между основаниями. Частицы в кристаллах плотно упакованы, так что расстояние между их центрами приблизительно равно размеру частиц.
