Конформация кресла конформация ванны (лодки)
Наиболее выгодной является конформация «кресла», так как в ней полностью отсутствует угловое напряжение.
Каждый атом углерода в циклогексановом кольце может иметь два заместителя: в аксиальном (а) и экваториальном (е) положениях.
Аксиальные заместители (а) располагаются вверх и вниз параллельно оси симметрии.
Экваториальные заместители (е) расположены под углом 109º28´ к оси симметрии в направлении к периферии от молекулы.
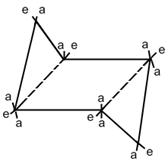
Наиболее энергетически выгодным является экваториальное расположение заместителей в циклогексановом кольце, так как при этом отсутствует торсионное напряжение.
При аксиальном расположении заместителей возникают 1,3 диаксиальные взаимодействия, что ведет к возникновению торсионного напряжения и образованию термодинамически менее устойчивых соединений.
1.8. Классификация реагентов и органических реакций.
Реакционная способность – способность вещества вступать в ту или иную химическую реакцию и реагировать с большей или меньшей скоростью.
Реакционный центр – атом или группа атомов в молекуле, непосредственно участвующие в химической реакции.
Субстрат – вещество, подвергающееся изменениям в результате химической реакции.
Реагент – партнер субстрата и более простое вещество.
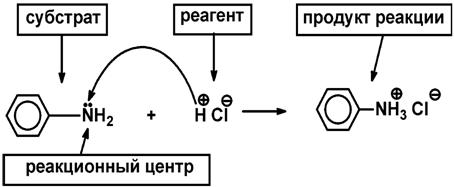
Типы реагентов и характер изменения связей
в реакционном центре субстрата
Кислотные реагенты (кислоты) – доноры протона по отношению к реакционному партнеру: частично или нацело ионизированные в водных растворах нейтральные молекулы (HCl, CH3COOH) или положительно заряженные частицы (NH4+, H3O+).
Основные реагенты (основания) – акцепторы протона по отношению к реакционному партнеру. Отрывают протон от кислотного центра:
отрицательно заряженные частицы B(ASE)- HO-, CH3O-
или нейтральные молекулы B: – NH3 , H2O.
Нуклеофильные реагенты (нуклеофилы) – частицы, образующие новую ковалентную связь за счет своей электронной пары.
Свойства:
- обладают повышенной электронной плотностью, взаимодействуют с любым атомом (кроме водорода), несущим частичный или полный положительный заряд;
- нуклеофил заряжен отрицательно (Nu-, Cl-, HO-, CH3O-, R3C- - карбоанион) или имеет неподеленную пару электронов (Nu, NH3 , H2O) или π-связь CH2= CH2, C6H6.
Электрофильные реагенты (электрофилы) – частицы, образующие новую ковалентную связь за счет пары электронов партнера.
Свойства:
- взаимодействуют с реакционным центром партнера с повышенной электронной плотностью;
- имеют атом, несущий частичный или полный положительный заряд или обладают вакантной орбиталью.
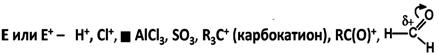
Радикальные реагенты (радикалы) – свободные атомы или частицы с неспаренным электроном (парамагнитные частицы).
R• – Cl•, Br•, HOO•, R•, •O–O• (бирадикал)
| Окислители – нейтральные молекулы или ионы, принимающие электроны или атомы водорода от органического субстрата. [O] (или Ox) – O2, Fe3+, органические окислители | Восстановители – нейтральные молекулы или ионы, отдающие электроны или атомы водорода органическому субстрату. [H] (или Red) – Р2, Fe2+, Н-, органические восстановители |
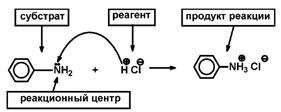
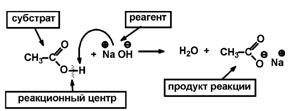
| реакционный центр кислотный, реагент основный | реакционный центр основный, реагент кислотный |
