Классификация органических соединений
Органические соединения отличаются своей многочисленностью и разнообразием. Поэтому необходима их систематизация. Органические соединения классифицируют, учитывая два основных структурных признака:
- строение углеродной цепи (углеродного скелета);
- наличие и строение функциональных групп.
Углеродный скелет (углеродная цепь) - последовательность химически связанных между собой атомов углерода.
Функциональная группа - атом или группа атомов, определяющие принадлежность соединения к определенному классу и ответственные за его химические свойства.
Гомологический ряд образуют соединения, отличающиеся друг от друга на группу —СН2— и обладающие сходными химическими свойствами. Группы СН2 называются гомологической разностью.
Номенклатура органических соединений
Нумерацию атомов углерода в главной цепи начинают с того конца цепи, ближе к которому расположена старшая группа. Если таких возможностей оказывается несколько, то нумерацию проводят таким образом, чтобы либо кратная связь, либо другой заместитель, имеющийся в молекуле, получили наименьший номер.
В карбоциклических соединениях нумерацию начинают от того атома углерода, при котором находится старшая характеристическая группа. Если при этом невозможно выбрать однозначную нумерацию, то цикл нумеруют так, чтобы заместители имели наименьшие номера.
В группе циклических углеводородов особо выделяются ароматические углеводороды, для которых характерно наличие в молекуле бензольного кольца. Некоторые широко известные представители ароматических углеводородов иих производных имеют тривиальные названия, использование которых разрешено правилами ИЮПАК: бензол, толуол, фенол, бензойная кислота.
Тривиальная номенклатура представляет собой совокупность несистематических исторически сложившихся названий органических соединений (пример: ацетон, уксусная кислота, формальдегид и т. д.).
Рациональная номенклатура позволяет строить название вещества на основании его структуры с более простым соединением, выбранным в качестве прототипа.
Билет 10
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи.
Строение алканов
Химическое строение (порядок соединения атомов в молекулах)
В алканах имеются два типа химических связей:
С–С и С–Н.
Электронные и структурные формулы отражают химическое строение, но не дают представления о пространственном строении молекул, которое существенно влияет на свойства вещества.
Пространственное строение, т.е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих атомов.
Пространственное расположение АО углерода в свою очередь зависит от типа его гибридизации.
Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Следовательно, его состояние соответствует sp3-гибридизации.
Получение алканов
Алканы выделяют из природных источников (природный и попутный газы, нефть, каменный уголь). Используются также синтетические методы.
- Крекинг нефти (промышленный способ)
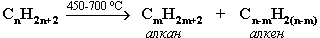
При крекинге алканы получаются вместе с непредельными соединениями (алкенами). Этот способ важен тем, что при разрыве молекул высших алканов получается очень ценное сырье для органического синтеза: пропан, бутан, изобутан, изопентан и др.
- Гидpиpование непpедельных углеводоpодов:
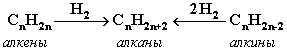
- Газификация твердого топлива (при повышенной температуре и давлении, катализатор Ni):
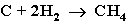
- Из синтез-газа (СО + Н2) получают смесь алканов:
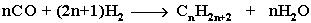
- Синтез более сложных алканов из галогенопpоизводных с меньшим числом атомов углеpода:
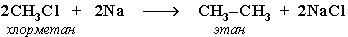
(реакция Вюpца)
- Из солей карбоновых кислот:
а) сплавление со щелочью (реакция Дюма)
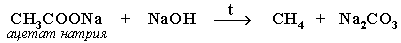
б) электролиз по Кольбе
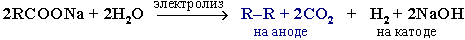
7. Разложение карбидов металлов (метанидов) водой:
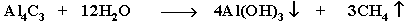
Билет 11
Химические свойства любого соединения определяются его строением, т.е. природой входящих в его состав атомов и характером связей между ними.
Во-первых, предельная насыщенность алканов не допускает реакций присоединения, но не препятствует реакциям разложения, изомеризации и замещения
Во-вторых, симметричность неполярных С–С и слабополярных С–Н ковалентных связей (см. в таблице значения дипольных моментов) предполагает их гомолитический (симметричный) разрыв на свободные радикалы
Следовательно, для реакций алканов характерен радикальный механизм.
Поскольку гетеролитический разрыв связей С–С и С–Н в обычных условиях не происходит, то в ионные реакции алканы практически не вступают. Это проявляется в их устойчивости к действию полярных реагентов (кислот, щелочей, окислителей ионного типа: КMnO4,
К2Сr2O7 и т.п.). Такая инертность алканов в ионных реакциях и послужила ранее основанием считать их неактивными веществами и назвать парафинами.
В зависимости от того, какая связь в молекуле разрывается в первую очередь, реакции алканов подразделяются на следующие типы.
С разрывом связей С–С происходят реакции разложения (крекинг алканов) и изомеризации углеродного скелета.
По связям С–Н возможны реакции замещения атома водорода или его отщепления (дегидрирование алканов).
Кроме того, атомы углерода в алканах находятся в наиболее восстановленной форме (степень окисления углерода, например, в метане равна –4, в этане –3 и т.д.) и в присутствии окислителей в определенных условиях будут происходить реакцииокисления алканов с участием связей С–С и С–Н.
Механизм радикального замещения (символ SR) на примере монохлорирования метана
Стадия 1 – зарождение цепи - появление в зоне реакции свободных радикалов. Под действием световой энергии гомолитически разрушается связь в молекуле Cl:Cl на два атома хлора с неспаренными электронами (свободные радикалы)·Cl:
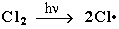
Стадия 2 – рост (развитие) цепи. Свободные радикалы, взаимодействуя с молекулами, порождают новые радикалы и развивают цепь превращений:
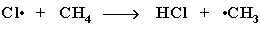
(Реакция Cl· + CH4 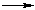 CH3Cl + H· не идет, т.к. энергия атомарного
CH3Cl + H· не идет, т.к. энергия атомарного
водорода H· значительно выше, чем метильного радикала ·СН3).
Стадия 3 – обрыв цепи. Радикалы, соединяясь друг с другом, образуют молекулы и обрывают цепь превращений:
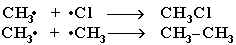
При хлорировании или бромировании алкана с вторичными или третичными атомами углерода легче всего идет замещение водорода у третичного атома, труднее у вторичного и еще труднее у первичного. Это объясняется большей устойчивостью третичных и вторичных углеводородных радикалов по сравнению с первичными вследствие делокализации неспаренного электрона. Поэтому, например, при бромировании пропана основным продуктом реакции является 2-бромпропан:
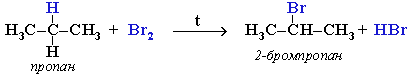
Билет 12
- Циклоалканы (циклопаpафины, нафтены, цикланы, полиметилены) – предельные углеводороды с замкнутой (циклической) углеродной цепью.
Атомы углерода в циклоалканах, как и в алканах, находятся в sp3–гибридизованном состоянии и все их валентности полностью насыщены.
Простейший циклоалкан – циклопpопан С3Н6
Получение циклоалканов
1. Циклоалканы содержатся в значительных количествах в нефтях некоторых месторождений (отсюда произошло одно из их названий - нафтены). При переработке нефти выделяют главным образом циклоалканы С5 - С7.
2. Действие активных металлов на дигалогензамещенные алканы (внутримолекулярная реакция Вюрца) приводит к образованию различных циклоалканов:
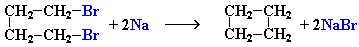
(вместо металлического натрия часто используется порошкообразный цинк).
Строение образующегося циклоалкана определяется структурой исходного дигалогеналкана. Этим путем можно получать циклоалканы заданного строения. Например, для синтеза 1,3-диметилциклопентана следует использовать 1,5-дигалоген-2,4-диметилпентан:
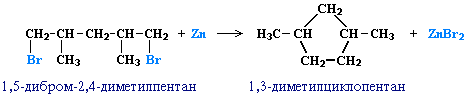
Важным промышленным способом получения циклоалканов С5 и С6 является реакция дегидроциклизации алканов.
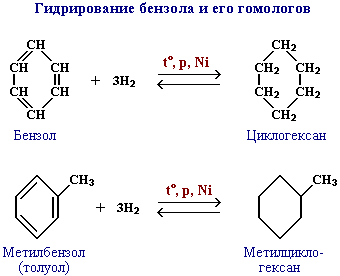
Существуют и другие методы получения циклоалканов. Так, например, циклогексан и его алкильные производные получают гидрированием бензола и его гомологов, являющихся продуктами нефтепереработки.
Химические свойства циклоалканов сильно зависят от размера цикла, определяющего его устойчивость. Трех- и четырехчленные циклы (малые циклы), являясь насыщенными, тем не менее, резко отличаются от всех остальных предельных углеводородов. Валентные углы в циклопропане и циклобутане значительно меньше нормального тетраэдрического угла 109°28’, свойственного sp3-гибридизованному атому углерода.
Это приводит к большой напряженности таких циклов и их стремлению к раскрытию под действием реагентов. Поэтому циклопропан, циклобутан и их производные вступают в реакции присоединения, проявляя характер ненасыщенных соединений. Легкость реакций присоединения уменьшается с уменьшением напряженности цикла в ряду:
циклопропан > циклобутан >> циклопентан.
Малые циклы (С3 – С4) довольно легко вступают в реакции гидрирования:
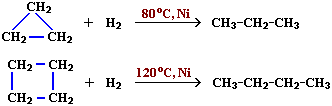
Циклопропан и его производные присоединяют галогены и галогеноводороды:
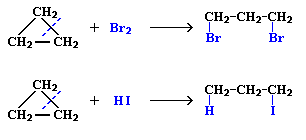
Билет 13
- Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов CnH2n.
Простейшие представители:
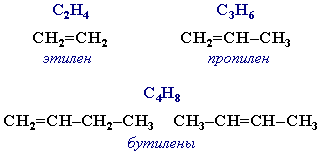
В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4-мя общими электронами:
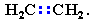
в образовании такой связи участвуют атомы углерода в sp2-гибридизованном состоянии.Каждый из них имеет по три 2sp2-гибридных орбитали, направленных друг к другу под углом 120°, и одну негибридизованную 2р-орбиталь, расположенную под углом 90° к плоскости гибридных АО.
Строение двойной связи С=С
Двойная связь является сочетанием σ- и π-связей (хотя она изображается двумя одинаковыми черточками, всегда следует учитывать их неравноценность). σ-Связь возникает при осевом перекрывании sp2-гибридных орбиталей, а π-связь – при боковом перекрывании р-орбиталей соседних sp2-гибридизованных атомов углерода.
Образование связей в молекуле этилена можно изобразить следующей схемой:
С=С σ-связь (перекрывание 2sp2-2sp2) и π-связь (2рz-2рz)
С–Н σ-связь (перекрывание 2sp2-АО углерода и 1s-АО водорода)
По своей природе π-связь резко отличается от σ-связи: π-связь менее прочная вследствие меньшей эффективности перекрывания р-орбиталей.
В молекуле пропилена СН2=СН–СН3 в одной плоскости лежат 6 атомов: два sp2-атома углерода и четыре связанные с ними атома (3 атома Н и атом С группы СН3). Вне этой плоскости находятся атомы водорода в метильной группе СН3, имеющей тетраэдрическое строение, т.к. этот атом углерода sp3-гибридизован.
Аналогичное строение имеют другие алкены.
Получение алкенов
В природе алкены встречаются в значительно меньшей степени, чем предельные углеводороды, по-видимому, вследствие своей высокой реакционной способности. Поэтому их получают с использованием различных реакций.
I. Крекинг алканов:
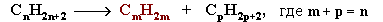
Например:
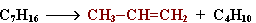
II. Отщепление (элиминирование) двух атомов или групп атомов от соседних атомов углерода с образованием между ними p-связи.
- Дегидрогалогенирование галогеналканов при действии спиртового раствора щелочи
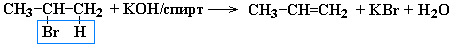
- Дегидратация спиртов при повышенной температуре (выше 140° C) в присутствии водоотнимающих реагентов
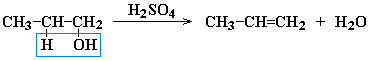
Реакции элиминирования идут в соответствии с правилом Зайцева:
Отщепление атома водорода в реакциях дегидрогалогенирования и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода.
Современная формулировка: реакции отщепления идут с образованием более замещенных при двойной связи алкенов.
Такие алкены обладают более низкой энергией.
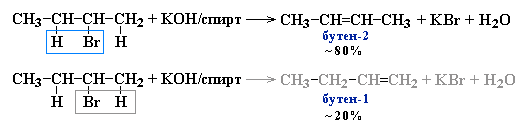
- Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов :
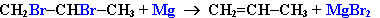
- Дегидрирование алканов при 500°С:
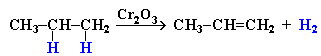
Билет 14
Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее других связей в молекулах этих соединений. Алкены химически более активны, чем алканы.
Для алкенов наиболее характерны реакции, протекающие за счет раскрытия менее прочной π-связи. При этом π-связь (в исходном алкене) преобразуется в σ-связь в продукте реакции. Исходное ненасыщенное соединение превращается в насыщенное без образования других продуктов, т.е. происходит реакция присоединения.
Двойная связь склонна подвергаться атаке электрофильным (электронодефицитным) реагентом. В этом случае будет происходить гетеролический разрыв π-связи и реакция пойдет по ионному механизму как электрофильное присоединение.
Реакции электрофильного присоединения (англ. additionelectrophilicreaction) — реакции присоединения, в которых атаку на начальной стадии осуществляет электрофил — частица, заряженная положительно или имеющая дефицит электронов. На конечной стадии образующийся карбкатион подвергается нуклеофильной атаке.
В органической химии чаще всего атакующей электрофильной частицей является протон H+.
Несмотря на общность механизма различают реакции присоединения по связи углерод—углерод и углерод—гетероатом.
Реакции электрофильного присоединения распространены среди алкенов и алкинов и широко используются в промышленном химическом производстве и лабораторных синтезах.
Билет 15
Реакции окисления алкенов
Строение продуктов окисления алкенов зависит от условий реакции и природы окислителя.
1. Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакцияВагнера):
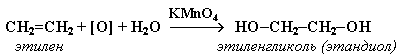
Полное уравнение реакции:
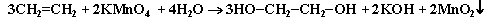
(см. схему электронногобаланса этой реакции).
В ходе этой реакции происходит обесцвечивание фиолетовой окраски водного раствора KMnO4. Поэтому она используется как качественная реакция на алкены.
2. При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
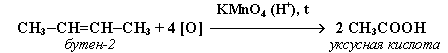
3. Промышленное значение имеет частичное окисление алкенов с образованием циклических оксидов, которые широко используются в органическом синтезе:
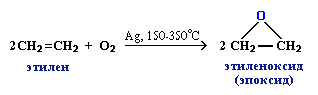
4. Полное окисление (горение):
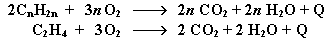
Газообразные гомологи алкенов образуют с воздухом взрывоопасные смеси.
Билет 16
- Алкины (ацетиленовые углеводороды) – непредельные алифатические углеводороды, молекулы которых содержат тройную связь C≡C.
Общая формула алкинов с одной тройной связью СnH2n-2
Простейшие представители:
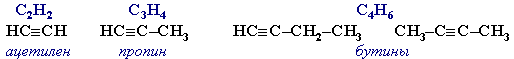
В образовании такой связи участвуют атомы углерода в sp-гибридизованном состоянии .Каждый из них имеет по две sp-гибридных орбитали, направленных друг к другу под углом 180°, и две негибридных р-орбитали, расположенных под углом 90° по отношению друг к другу и к sp-гибридным орбиталям.
Строение тройной связи C≡C
Тройная связь является комбинацией из одной σ- и двух π-связей, образуемых двумя sp-гибридизованными атомами.
σ-Связь возникает при осевом перекрывании sp-гибридных орбиталей соседних атомов углерода; одна из π-связей образуется при боковом перекрывании рy-орбиталей, другая – при боковом перекрывании рz-орбиталей. Образование связей на примере молекулы ацетилена H–C≡C–H можно изобразить в виде схемы:
C≡C σ-связь (перекрывание 2sp-2sp);
π-связь (2рy-2рy);
π-связь (2рz-2рz);
С–Н σ-связь (перекрывание 2sp-АО углерода и 1s-АО водорода).
π-Cвязи располагаются во взаимно перпендикулярных плоскостях:
σ-Cвязи, образуемые sp–гибридными орбиталями углерода, располагаются на одной прямой (под углом 180° друг к другу). Поэтому молекула ацетилена имеет линейное строение
Получение алкинов
Ацетилен является важнейшим исходным продуктом в производстве многих органических веществ и материалов. Его получают в больших количествах, используя ряд промышленных методов.
- Пиролиз метана:
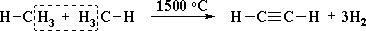
Реакцию проводят электродуговым способом, пропуская метан между электродами с временем контакта 0,1-0,01 секунды. Столь малое время нагревания обусловлено тем, что ацетилен при такой температуре может разлагаться на углерод и водород.
- Пиролиз этана или этилена:
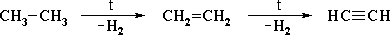
- Гидролиз карбида кальция:
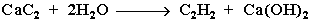
- Карбид кальция образуется при нагревании смеси оксида кальция СаО (жженой извести) и кокса до 2500°С:
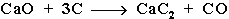
Вследствие большой энергоемкости этот метод экономически менее выгоден.
Для синтеза гомологов ацетилена применяют следующие методы:
1) дегидрогалогенирование дигалогеналканов спиртовым раствором щелочи (щелочь и спирт берутся в избытке)
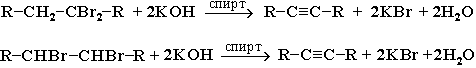
2) удлинение цепи (алкилирование ацетиленидов) при действии на ацетилениды алкилгалогенидами
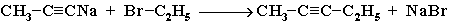
Билет 17
Химические свойства алкинов сходны с алкенами, что обусловлено их ненасыщенностью.
Некоторые отличия в свойствах алкинов и алкенов определяются следующими факторами.
- π-Электроны более короткой тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью (подвижностью). Поэтому реакции электрофильного присоединения к алкинам протекают медленнее, чем к алкенам.
- π-Электронное облако тройной связи сосредоточено в основном в межъядерном пространстве и в меньшей степени экранирует ядра углеродных атомов с внешней стороны. Следствием этого является доступность ядер углерода при атаке нуклеофильными реагентами и способность алкинов вступать в реакции нуклеофильного присоединения.
- Связь атома водорода с углеродом в sp-гибридизованном состоянии значительно более полярна по сравнению сС–Н-связями в алканах и алкенах. Это объясняется различным вкладом в гибридизованное состояние s-орбитали, которая более прочно, чем р-АО, удерживает электроны (сравните форму и энергию s- и р-АО). Доля s-АО в sp3-состоянии составляет 25%, в sp2 – 33%, а в sp – 50%. Чем больше вклад s-АО, тем выше способность атома удерживать внешние электроны, т.е. его электроотрицательность. Повышенная полярность связи С(sp)–Н приводит к возможности её гетеролитического разрыва с отщеплением протона (Н+). Таким образом, алкины с концевой тройной связью(алкины-1) проявляют кислотные свойства и способны, вступая в реакции с активными металлами, образовывать соли.
Ацетилен и его гомологи с концевой тройной связью R–C≡C–H (алкины-1) вследствие полярности связи С(sp)-Н проявляют слабые кислотные свойства: атомы водорода могут замещаться атомами металла. При этом образуются соли – ацетилениды:
4. 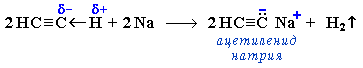
Ацетилениды щелочных и щелочноземельных металлов используются для получения гомологов ацетилена.
Билет 18.
- Алкадиены (диены) – непредельные алифатические углеводороды, молекулы которых содержат две двойные связи.
Общая формула алкадиенов СnH2n-2.
Свойства алкадиенов в значительной степени зависят от взаимного расположения двойных связей в их молекулах. По этому признаку различают три типа двойных связей в диенах.
1.Изолированные двойные связи разделены в цепи двумя или более σ-связями:
СН2=СН–СН2–СН=СН2
Разделенные sp3-атомами углерода, такие двойные связи не оказывают друг на друга взаимного влияния и вступают в те же реакции, что и двойная связь в алкенах. Таким образом, алкадиены этого типа проявляют химические свойства, характерные для алкенов.
2. Кумулированные двойные связи расположены у одного атома углерода:
СН2=С=СН2 (аллен)
Подобные диены (аллены) относятся к довольно редкому типу соединений.
3.Сопряженные двойные связи разделены одной σ-связью:
СН2=СН–СН=СН2
Сопряженные диены представляют наибольший интерес. Они отличаются характерными свойствами, обусловленными электронным строением молекул, а именно, непрерывной последовательностью 4-х sp2-атомов углерода.
Отдельные представители этих диенов широко используются в производстве синтетических каучуков и различных органических веществ.
Галогенирование
1,4-присоединение:
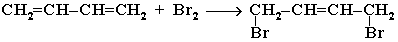
1,2-присоединение:
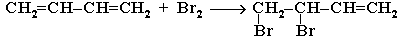
При избытке брома присоединяется еще одна его молекула по месту оставшейся двойной связи с образованием 1,2,3,4-тетрабромбутана.
Присоединение галогенов, галогеноводородов, воды и других полярных реагентов происходит по электрофильному механизму (как в алкенах).
К реакциям присоединения относятся реакции полимеризации, характерные для диенов. Этот процесс имеет важное значение в производстве синтетических каучуков.
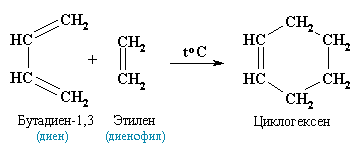
3. Диеновый синтез (реакция Дильса-Альдера)
В органическом синтезе широко применяется реакция присоединения к сопряженным диенам соединений, содержащих кратные связи (так называемых диенофилов). Реакция идет как 1,4-присоединение и приводит к образованию циклических продуктов:
Билет 19.
- Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Простейшие представители (одноядерные арены):
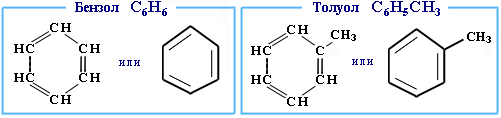
Многоядерные арены: нафталин С10Н8, антрацен С14Н10 и др.
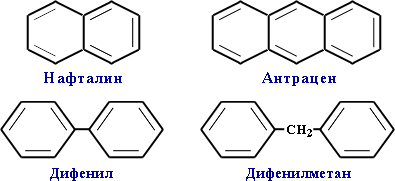
Термин "ароматические соединения" возник давно в связи с тем, что некоторые представители этого ряда веществ имеют приятный запах. Однако в настоящее время в понятие "ароматичность" вкладывается совершенно иной смысл.
Ароматичность молекулы означает ее повышенную устойчивость, обусловленную делокализацией π-электронов в циклической системе.
Критерии ароматичности аренов:
- Атомы углерода в sp2-гибридизованном состоянии образуют циклическую систему.
- Атомы углерода располагаются в одной плоскости (цикл имеет плоское строение).
- Замкнутая система сопряженных связей содержит
4n+2 π-электронов (n – целое число).
Этим критериям полностью соответствует молекула бензола С6Н6.
Бензол С6Н6 – родоначальник ароматических углеводородов.
Каждый из шести атомов углерода в его молекуле находится в состоянии sp2-гибридизации и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. Валентные углы между каждой парой π-связей равны 120°. Таким образом, скелет σ-связей представляет собой правильный шестиугольник, в котором все атомы углерода и все σ-связи С–С и С–Н лежат в одной плоскости:
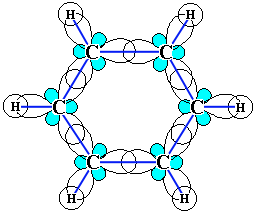
р-Электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2р-АО, расположенных перпендикулярно плоскости σ-скелета бензольного кольца. Они образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца.
Поэтому структурную формулу бензола изображают в виде правильного шестиугольника (σ-скелет) и кружка внутри него, обозначающего делокализованные π-связи:
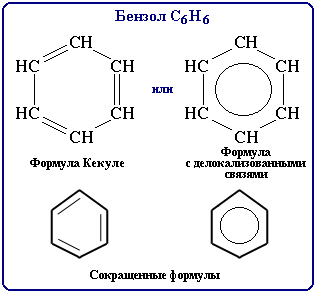
Формула Кекуле также нередко используется, но при этом учитывается, что она лишь условно передает строение молекулы.
Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
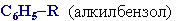
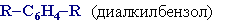
Общая формула гомологического ряда бензола CnH2n-6 (n ≥ 6).
Номенклатура. Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия углеводородного радикала (приставка) и слова бензол (корень):
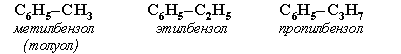
Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с которыми они связаны. Нумерацию кольца проводят так, чтобы номера радикалов были наименьшими. Например:
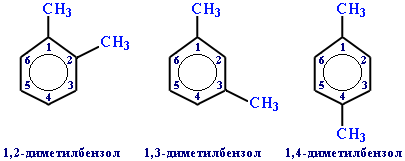
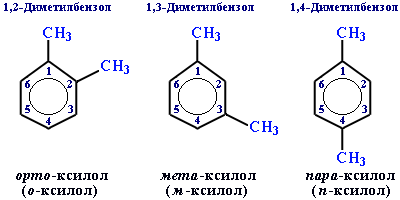
Для дизамещенных бензолов R-C6H4-R используется также и другой способ построения названий, при котором положение заместителей указывают перед тривиальным названием соединения приставками:
орто- (о-) заместители у соседних атомов углерода кольца, т.е. 1,2-;
мета- (м-) заместители через один атом углерода (1,3-);
пара- (п-) заместители на противоположных сторонах кольца (1,4-).
Ароматические одновалентные радикалы имеют общее название "арил". Из них наиболее распространены в номенклатуре органических соединений два: C6H5- (фенил) и C6H5CH2- (бензил).
Изомерия (структурная):
1) положения заместителей для ди-, три- и тетра-замещенных бензолов (например, о-, м- и п-ксилолы);
2) углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:
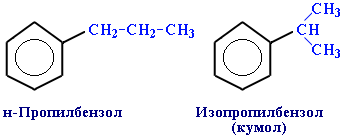
3) изомерия заместителей R, начиная с R = С2Н5.
Например, молекулярной формуле С8Н10 соответствуют 4 изомера:
три ксилола CH3-C6H4-CH3 (о-, м-, п-) и этилбензол C6H5-C2H5.
Пространственная изомерия относительно бензольного кольца в алкилбензолах отсутствует.
Билет 20.
По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация шести π-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов.
Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
Для аренов более характерны реакции, идущие с сохранением ароматической системы, а именно, реакции замещения атомов водорода, связанных с циклом.
Наличие областей повышенной π-электронной плотности с двух сторон плоского ароматического цикла ведет к тому, что бензольное кольцо является нуклеофилом и в связи с этим склонно подвергаться атаке электрофильным реагентом. Таким образом, для ароматических соединений наиболее типичны реакции электрофильного замещения.
Механизм электрофильного замещения обозначается символом SЕ
(по первым буквам английских терминов: S – substitution [замещение],
E – electrophil [электрофил]).
Другие реакции (присоединение, окисление), в которых участвуют делокализованные углерод-углеродные связи бензольного кольца и нарушается его ароматичность, идут с трудом.
