Лабораторная работа №3. «Получение и свойства этилена»
Цель: получить этилен и его идентификация его по химическим свойствам.
Формируемые умения:
· собирать прибор для получения газа
· нагревать стеклянную посуду с жидкостью, обеспечивая равномерное кипение
· поджигать газ
· получать этилен из этанола;
· проводить качественную реакцию на кратную связь при помощи бромной воды
· проводить качественную реакцию на кратную связь посредством раствора перманганата калия (при рН=7 и рН<7);
Реактивы и оборудование: смесь для получения этилена, бромная вода (насыщенная), 2%-ный раствор перманганата калия, 10%-ный раствор карбоната натрия, 1%-ный раствор перманганата калия, концентрированная серная кислота; прибор для получения этилена, кипятильники (кусочки битого фарфора или кварцевый песок), газоотводные трубки, соединенные с хлоркальциевыми трубками, заполненными кусочками натронной извести, крышки от тиглей.
Методика
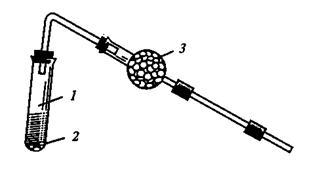 1. Получение этилена. В сухую пробирку наливают 4—5 мл смеси для получения этилена, состоящей из 96%-ного этилового спирта и концентрированной серной кислоты в объемном соотношении 1:2. При смешивании этанола с серной кислотой образуется этилсерная кислота (кислый сложный эфир):
1. Получение этилена. В сухую пробирку наливают 4—5 мл смеси для получения этилена, состоящей из 96%-ного этилового спирта и концентрированной серной кислоты в объемном соотношении 1:2. При смешивании этанола с серной кислотой образуется этилсерная кислота (кислый сложный эфир):
В реакционную смесь помещают несколько кипятильников (для равномерного кипения). Пробирку закрывают пробкой с газоотводной трубкой, которую предварительно соединяют с хлоркальциевой трубкой, заполненной натронной известью.
Необходимо помнить, что гранулированная натронная известь не должна плотно заполнять хлоркальциевую трубку, чтобы выделяющиеся при реакции газы не выбили пробку из пробирки и не произошел выброс реакционной смеси.
Перед получением этилена в штатив ставят три пробирки с реактивами: в первую наливают 3—4 мл бромной воды, во вторую — 2 мл 2%-ного раствора перманганата калия и 0,5 мл 10%-ного раствора карбоната натрия, а в третью — 2 мл 1%-ного раствора перманганата калия и 1 каплю концентрированной серной кислоты.
Выделяющийся этилен пропускают через бромную воду, которая моментально обесцвечивается (качественная реакция на кратные связи):
2. Реакция этилена с бромной водой. Пробирку с реакционной смесью для получения этилена закрепляют в лапке штатива и осторожно нагревают таким образом, чтобы кипящую жидкость не перебросило в хлоркальциевую трубку. При нагревании из этилсерной кислоты образуется этилен.
Кроме основной реакции, при получении этилена протекают побочные реакции. Так, концентрированная серная кислота при высокой температуре окисляет органическое вещество до углерода и оксида углерода (IV), в результате чего смесь чернеет, а сама кислота восстанавливается до оксида серы (IV). Выделяющиеся кислотные оксиды активно поглощаются натронной известью, помещенной в хлоркальциевую трубку.
Напишите механизм реакции образования этилена (сернокислотная дегидратация) из этилсерной кислоты.
Напишите уравнения реакций взаимодействия оксидов углерода (IV) и серы (IV) с натронной известью. Рассмотрите механизм реакции электрофильного присоединения (АЕ) брома к этилену и укажите, какую роль в этом процессе играет вода.
3. Взаимодействие этилена с водным раствором перманганата калия (реакция Вагнера). Этилен пропускают через 2%-ный раствор перманганата калия, подщелоченный 10%-ным раствором карбоната натрия. Наблюдают исчезновение фиолетовой окраски перманганата калия и образование бурого хлопьевидного осадка (качественная реакция на кратные связи). Напишите уравнение реакции.
4. Окисление этилена в кислой среде. Через подкисленный серной кислотой раствор перманганата калия пропускают этилен. В результате реакции происходит его обесцвечивание, при этом бурые хлопья не образуются, так как окисление происходит более глубоко.
Расставьте коэффициенты в уравнении реакции, используя метод электронного баланса.
2.4. Горение этилена. После проведения вышеперечисленных реакций этилен поджигают у конца газоотводной трубки. Он горит светящимся пламенем. При внесении в пламя фарфоровой чашки на ней образуется черное пятно, появление которого можно объяснить большим содержанием (%) углерода в молекуле этилена и его неполным окислением. Рассчитайте массовые доли углерода и водорода в молекуле этилена. Напишите уравнение реакции полного сгорания этилена.
Литература для самостоятельной работы
1. Органическая химия: Учебник для вузов: В 2 кн./В.Л. Белобородов, С.Э. Зурабян, А.П. Тюкавкина; Под ред. Н.А. Тюкавкиной. - М.: Дрофа, 2002. – Кн. 1: Основной курс. С. 185-186; 206-207; 215-217.
