Лабораторно-практическое занятие № 14. «Предельные углеводороды: получение и идентификация» (3ч)
Цель:расширятьзнания о получении и идентификации предельных углеводородов, формирование умений получать метан и идентифицировать его химическими методами.
Вопросы для обсуждения:
1. Основные способы получения алканов: гидрирование алкенов и алкинов, восстановление галогеноалканов, восстановление карбонильных соединений, реакция Вюрца, анодный синтез.
2. Основные способы получения циклоалканов: внутримолекулярная реакция Вюрца 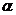 ,
, 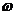 - дигалогеналканов; синтезы на основе малонового или ацетоуксусного эфиров; пиролиз солей дикарбоновых кислот; внутри- и межмолекулярная конденсация эфиров дикарбоновых кислот по Дикману—Кляйзену; ацилоиновая конденсация; реакции карбенов с непредельными соединениями; реакции циклоприсоединения (реакция Дильса—Альдера и другие); реакции восстановления ароматических соединений.
- дигалогеналканов; синтезы на основе малонового или ацетоуксусного эфиров; пиролиз солей дикарбоновых кислот; внутри- и межмолекулярная конденсация эфиров дикарбоновых кислот по Дикману—Кляйзену; ацилоиновая конденсация; реакции карбенов с непредельными соединениями; реакции циклоприсоединения (реакция Дильса—Альдера и другие); реакции восстановления ароматических соединений.
Материалы и примеры для самостоятельного изучения
Пример 1. Предложите пять способов получения 2,3- диметилбутана?
Решение:
1. Реакция Вюрца:
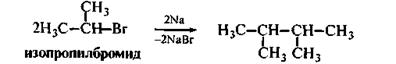
2. Способ Кольбе:
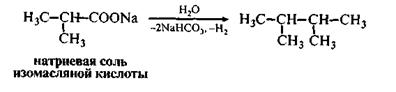
3. Каталитическое гидрирование непредельных углеводородов:
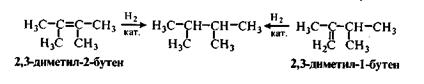
4. Восстановление галогеноалканов:
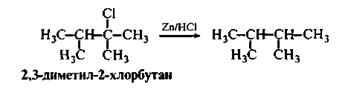
5. Гидролиз магнийорганических соединений.
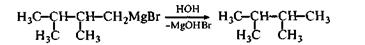
Пример 2. Как получить 1,2-диметилциклопропан и метилциклобутан из дигалогеналканов и выход какого из них будет выше?
Решение. Эти соединения можно получить внутримолекулярной реакцией Вюрца из 2,4- и 1,4-дибромпентанов. 1,2-диметилциклопропан будет образовываться с большим выходом, так как в этом случае вероятностный фактор значительно выше, чем в случае замыкания четырехчленного цикла:
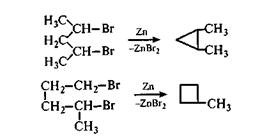
Пример 3. Каковы основные методы получения циклопентанов и циклогексанов?
Решение. Для получения производных этих циклоалканов широко используются внутримолекулярные сложноэфирная и ацилоиновая конденсации эфиров двухосновных кислот и пиролиз юс кальциевых, бариевых или магниевых солей.
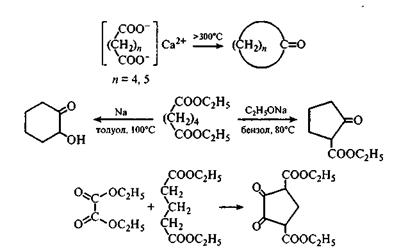
Для синтеза циклогексенов, легко превращаемых в циклогексаны, широко применяется реакция Дильса—Альдера (диеновый синтез, [4+2]-циклоприсоединение):
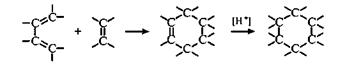
Циклогексан и гомологи могут быть получены гидрированием соответствующих бензолов
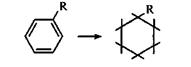
Циклопентаны и циклогексаны можно извлекать из некоторых нефтей.
Задачи для самостоятельного решения
Способы получения и химические превращения
Задача 14.1.Назовите алканы, являющиеся продуктами следующих реакций:
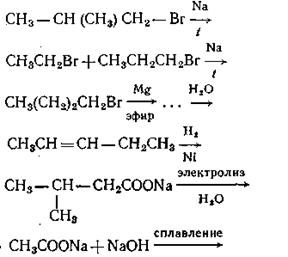
Задача 14.2.Как можно получить н-бутан из указанных соединений:
а) н-бутилбромида;
б) втор-бутилбромида;
в) хлористого этила;
г) 2-бутена;
д) валериановой кислоты;
е) пропионовой кислоты?
Приведите схемы реакций.
Задача 14.3.Напишите схему получения н-гексана электролизом водного раствора калиевой соли соответствующей карбоновой кислоты. Разберите механизмы реакций, проходящих на аноде и катоде.
Задача 14.4.Из каких алкилгалогенидов можно получить н-гексан по
реакции Вюрца? Укажите наиболее целесообразный вариант.
Задача 14.5.Назовите соединения, образующиеся в следующих реакциях:
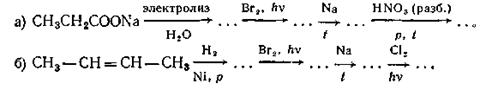
Задача 14.6.Назовите алициклические соединения, которые являются продуктами следующих реакций:
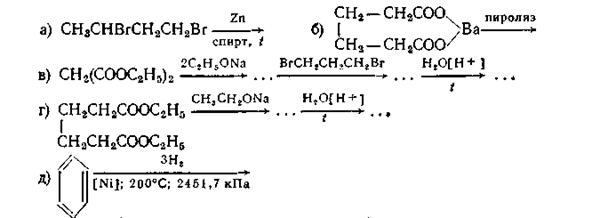
Задача 14.7. Из дигалогеналканов получите: а) этилциклопропан; б) 1,2-диметилциклобутан; в) метилциклопентан. Для какого соединения можно ожидать большой выход? Почему?
Установление строения соединений по их свойствам
Задача 14.8.Углеводород C5H12 при хлорировании образует только одно монохлорзамещенное соединение. Какое строение имеет исходный углеводород?
Задача 14.9.Какое строение имеет углеводород С10Н22, если известно, что он был получен электролизом водного раствора соли карбоновой кислоты, которая при сплавлении со щелочью образует тетраметилметан?
Задача 14.10.Установите строение алкилиодида, который при нагревании с HI дает изобутан, а с Na образует 2,5-диметилгексан. Приведите схемы реакций.
Задача 14.11.Соединение состава C7H14 присоединяет бром с образованием вещества С7Н14Вг2, но не реагирует с KMnO4 в воде при комнатной температуре. Каково строение исходного соединения, если известно также, что оно является цис-изомером?
Задача 14.12.Установите строение карбоновой кислоты, которая при сплавлении со щелочью образует изобутан, а электролиз водного раствора ее соли приводит к 2,5-диметилгексану. Напишите схемы реакций.
Задача 14.13.Алкан с молекулярной массой 72 образует при радикальном бромировании только одно третичное монобромопроизводное. Приведите строение исходного соединения.
Задача 14.14.При сжигании 1,85 мг вещества было получено 4,363 мг СО2 и 2,25 мг Н2О. Определите процентный состав вещества и его эмпирическую формулу, если плотность вещества по воздуху равна 2,55.
Задача 14.15.При сжигании 2,3 мг вещества было получено 4,43 мг СО2 и 2,691 мг Н2О. Определите процентный состав вещества и его эмпирическую формулу, если плотность вещества по водороду равна 23.
 Лабораторная работа № 3. «Получение и свойства алканов»
Лабораторная работа № 3. «Получение и свойства алканов»
Цель: получить метан и его идентификация его по химическим свойствам.
Формируемые умения:
· собирать прибор для получения газа
· нагревать стеклянную посуду с веществом
· поджигать выделяющийся газ
· получать метан из ацетата натрия
· изучать отношения выделяющего газа к раствору бромной воды и раствора перманганата калия
Реактивы и оборудование: смесь для получения метана — безводный ацетат натрия и прокаленная натронная известь (1: 2), разбавленный раствор перманганата калия, 5%-ный раствор карбоната натрия, бромная вода (насыщенная); изогнутые газоотводные трубки, крышки от тиглей, стеклянный цилиндр или химический стакан на 200 мл.
Методика
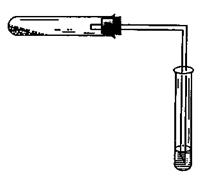 1. Получение и горение метана. В сухую пробирку насыпают смесь для получения метана (на 1/3 часть объема пробирки), размещая ее таким образом, чтобы метан мог свободно выходить из пробирки. Пробирку закрывают пробкой с газоотводной трубкой и закрепляют ее в лапке штатива с небольшим наклоном в сторону пробки (рис. ).
1. Получение и горение метана. В сухую пробирку насыпают смесь для получения метана (на 1/3 часть объема пробирки), размещая ее таким образом, чтобы метан мог свободно выходить из пробирки. Пробирку закрывают пробкой с газоотводной трубкой и закрепляют ее в лапке штатива с небольшим наклоном в сторону пробки (рис. ).
Перед получением метана в штатив ставят две пробирки: в первую наливают разбавленный раствор перманганата калия и 5%-ный раствор карбоната натрия в соотношении 3:1, во вторую — 3—4 мл насыщенной бромной воды.
Равномерно прогревают всю пробирку, а затем сильно нагревают ту ее часть, где находится основная часть смеси. Сначала из пробирки вытесняется воздух, потом начинает выделяться метан. Напишите уравнение реакции. Метан поджигают у конца газоотводной трубки, он горит несветящимся голубоватым пламенем. Напишите уравнение реакции.
Если внести в пламя метана фарфоровую крышку от тигля, то черного пятна от сажи на ней не образуется. Почему?
2. Отношение метана к водному раствору перманганата калия и бромной воде.Газоотводную трубку вводят в пробирку с водным раствором перманганата калия и пропускают метан в течение 1 мин. Затем ту же процедуру повторяют с бромной водой. Растворы не изменяют своей окраски, что свидетельствует о том, что метан при комнатной температуре не взаимодействует с водным раствором перманганата калия и бромной водой.
Литература для самостоятельной работы
1. Органическая химия: Учебник для вузов: В 2 кн./В.Л. Белобородов, С.Э. Зурабян, А.П. Тюкавкина; Под ред. Н.А. Тюкавкиной. - М.: Дрофа, 2002. – Кн. 1: Основной курс. – 620с ( С. 157-180)
2. Органическая химия (в вопросах и ответах) / Под ред. Б. А. Ивина и Л. Б. Пиотровского. — СПб.: Наука, 2002. — 510 с. (С. 319-322; 391-397)
