Поверхностная энергия и поверхностное натяжение.
Поверхностный слой, возникающий на границе различных фаз, следует рассматривать как самостоятельную фазу толщиной в несколько молекул. В отдельных случаях поверхностный слой имеет толщину, равную диаметру молекулы, и его называют мономолекулярным.Поэтому поверхностный слой нужно рассматривать как микрогетерогенную систему.
Поверхностный слой резко отличается по своим свойствам от свойств фаз, которые он разделяет. Молекулы, атомы, ионы, находящиеся на границе раздела фаз, не равноценны тем же частицам, находящимся в объеме фазы.
Силы, действующие на молекулы, находящиеся внутри жидкости, одинаковы со всех сторон, и их равнодействующая F равна нулю. Силы, действующие на молекулы повехностного слоя границы раздела жидкости с ее паром, не одинаковы со стороны раствора (снизу и с боков) и газообразной фазы (сверху). Молекулярные взаимодействия сверху отсутствуют, равнодействущая сил F не равна нулю и направлена внутрь жидкой фазы (рис. 22). Для выхода молекул на поверхность требуется выполнить работу Ws против этой силы. В итоге формируется поверхностный слой с избыточной поверхностной энергией Гиббса Gs.
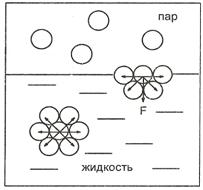
Рис. 22.Взаимодействие между молекулами в объеме жидкости и в поверхностном слое.
Все возможные поверхности раздела в зависимости от агрегатного состояния граничащих фаз делят на подвижные поверхности раздела между жидкостью и газом (ж-г), двумя несмешивающимися жидкостями (ж-ж) и неподвижные поверхности раздела между твердым телом и газом (т-г), твердым телом и жидкостью (т-ж), твердым телом и твердым телом (т-т).
При измельчении какой-либо твердой или жидкой фазы суммарный объем и масса остаются теми же самыми, тогда как суммарная площадь поверхности раздела возрастает.
Чтобы учесть влияние поверхности на свойства системы, вводят понятие удельной поверхности(Sya) фазы - величины, измеряемой суммарной площадью граничной поверхности фазы (ScyM), отнесенной к ее объему (V):
Sуд = Sсум/V
Влияние поверхности раздела фаз на свойства системы возрастает с увеличением удельной поверхности.
Энергия Гиббса G системы из двух фаз состоит из двух слагаемых - энергии Гиббса объемных фаз Gv и поверхностной энергии Гиббса GS:
G = GV + GS.
Энергия Гиббса объемных фаз пропорциональна их массе, а, следовательно, объему, занимаемому системой:
GV = kV.
Поверхностная энергия Гиббса системы пропорциональна межфазной поверхности:
GV = σS,
где σ- коэффициент пропорциональности, называемый поверхностным натяжением. Его величину измеряют в кДж/м2 (Н/метр) или в Дж/см2.
Поверхностное натяжение σ есть величина, измеряемая энергией Гиббса, приходящейся на единицу площади поверхностного слоя. Оно численно равно работе, которую необходимо совершить в данной системе для образования в ней единицы поверхности раздела фаз при постоянной температуре.
С учетом предыдущего получим уравнение:
G = kV + σ S
G/V= k + σ Sуд.
Следовательно, энергия Гиббса, приходящаяся на единицу объема системы, линейно увеличивается с увеличением ее удельной поверхности. При малых значениях удельной поверхности Syд. поверхностной энергией Гиббса можно пренебречь. При больших значениях Sуд. с ней необходимо считаться.
Если поверхность кожи человека составляет 1.5 м2, то поверхность эритроцитов имеет величину уже 3000м2. Трудно оценить величину суммарной поверхности, разделяющей все клетки организма, если помнить, что их общее число составляет около 1014, а к ним еще следует добавить микроорганизмы кишечной флоры, количество которых больше, чем общее количество клеток организма. Организм представляет собой совокупность систем с сильно развитыми поверхностями раздела (кожные покровы, стенки кровеносных сосудов, оболочки органов, клеточные мембраны, мембраны органелл, то есть клеточных структур и т. д.). В живых системах, следовательно, величина поверхностной энергии должна иметь большую величину.
Поверхностное натяжение различных жидкостей на границе жидкость - газ возрастает с увеличением взаимодействия между молекулами жидкости, являясь максимальным для воды из числа веществ, представленных в табл. 23.
Таблица 23
