Нуклеотидный состав и структура ДНК и РНК.
Нуклеотидный состав, т.е. набор и соотношение нуклеотидных компонентов, служит очень важной характеристикой нуклеиновых кислот. Один из основных путей установления состава нуклеиновых кислот основан на исследовании продуктов их гидролитического расщепления. Поскольку межнуклеотидные связи в полинуклеотидах являются сложноэфирными, то полинуклеотидные цепи способны гидролизоваться как в кислой, так и щелочной среде.
Химический гидролиз ДНК почти не используется из-за осложнения его побочными процессами. Более предпочтителен ферментативный гидролиз ДНК под действием нуклеаз. Обычно для этой цели используют змеиный яд, в котором содержатся ферменты, расщепляющие сложноэфирную связь с фосфорной кислотой (фосфодиэстеразы и фосфомоноэстеразы). Нуклеазы проявляют специфичность по отношению к типу нуклеиновых кислот; их делят на рибонуклеазы и дезоксирибонуклезы.
Выделение и идентификацию компонентов нуклеиновых кислот производят с помощью физико-химических методов. Очень важную роль в разделении сложных смесей играют хроматографические методы. Пиримидиновые и пуриновые основания, обладающие вследствие ароматического характера заметным поглощением около 260 нм, обычно идентифицируют с помощью УФ-спектроскопии. Поскольку нуклеотиды имеют кислотный характер и способны находиться в ионизированном состоянии, то для их идентификации используют также электрофорез.
Наряду с определением нуклеотидного состава важнейшая задача состоит и в установлении нуклеотидной последовательности, т.е. порядка чередования нуклеотидных звеньев. Общий подход заключается в использовании блочного метода: сначала полинуклеотидную цепь направленно расщепляют на более мелкие блоки – олигомеры и определяют в них нуклеотидную последовательность. Такой анализ повторяют дважды, используя во второй раз такие расщепляющие агенты, которые делят цель на фрагменты в иных местах по сравнению с первым разом. Полинуклеотидную цепь расщепляют на довольно короткие фрагменты. Более длинные олигонуклеотиды пока еще трудно поддаются изучению.
Первичная структура нуклеиновых кислот определяется природой и последовательностью нуклеотидных звеньев, связанных сложноэфирными связями между пентозами и фосфатными группами (рис 13).
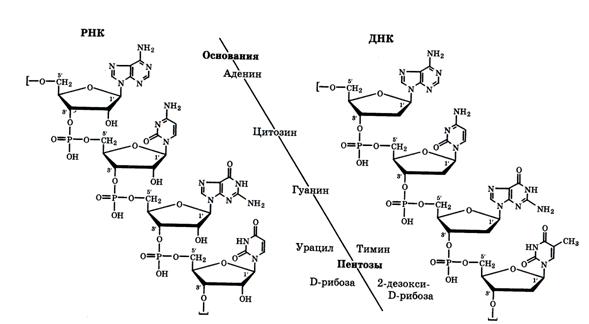
Рис. 13. Первичная структура участка цепи нуклеиновых кислот
В составе молекулы ДНК выделено значительно большее число нуклеотидных остатков, чем в молекуле РНК. Молекулярная масса ДНК порядка 10 млн; ДНК в условиях клетки нерастворима. Длина молекул ДНК человека составляет примерно 3 — 5 см; молекула РНК значительно короче — менее 0,01 см.
Вторичная структура нуклеиновых кислот. Согласно вторичной структуре полинуклеотидная цепь ДНК представляет собой двойную спираль, в которой пуриновые и пиримидиновые основания направлены внутрь. Между пуриновым основаниями одной цепи и пиримидиновым основанием другой цепи имеются водородные связи, стабилизирующие такую структуру. Основания, образующие пары, связанные водородными связями,называются комплементарными. В ДНК комплементарными будут: аденин – тимин, образующие между собой две водородные связи, и гуанин – цитозин, связанные тремя водородными связями (рис 14). Это означает, что пуриновым основаниям аденину и гуанину в одной цепи будут соответствовать пиримидиновые основания тимин и цитозин в другой цепи. Полинуклеотидные цепи, образующие двойную спираль, не идентичны, но комплементарны между собой.
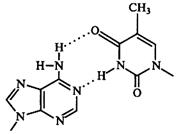
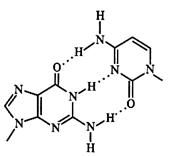
а б
Рис. 14. Водородные связи в паре оснований гуанин -цитозин (а), аденин – тимин (б)
Макромолекулы ДНК связаны между собой попарно при помощи водородных связей в виде двойной спирали постоянного диаметра (рис. 15). Остатки нуклеиновых оснований направлены внутрь спирали, диаметр которой равен примерно 2 нм.
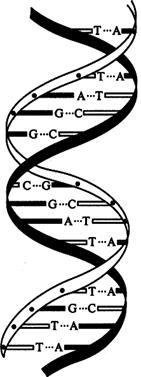 На один виток спирали приходится 10 пар оснований. Для обеспечения наибольшей устойчивости этой структуры водородных связей должно быть максимально много. Только при выполнении этого условия обеспечивается экспериментально доказанное постоянство суммарных размеров боковых групп и неизменность диаметра двойной спирали на всем ее протяжении. В этой взаимной обусловленности последовательности звеньев в обеих цепях заключается принцип комплементарности.
На один виток спирали приходится 10 пар оснований. Для обеспечения наибольшей устойчивости этой структуры водородных связей должно быть максимально много. Только при выполнении этого условия обеспечивается экспериментально доказанное постоянство суммарных размеров боковых групп и неизменность диаметра двойной спирали на всем ее протяжении. В этой взаимной обусловленности последовательности звеньев в обеих цепях заключается принцип комплементарности.
Комплементарность цепей и последовательность звеньев составляют химическую основу важнейших функций нуклеиновых кислот: ДНК — хранение и передача наследственной информации, а РНК — непосредственное участие в биосинтезе белка. Молекулярная масса ДНК варьирует от нескольких миллионов до десятка миллиардов, у РНК - от десятка тысяч до нескольких миллионов.
Комплементарность оснований лежит в основе закономерностей, сформулированных Э. Чаргаффом, которым подчиняется нуклеотидный состав ДНК различного происхождения.

Правила Чаргаффа:
1)  количество пуриновых оснований равно количеству пиримидиновых оснований, т.е. (А+Г)=(Ц+Т).
количество пуриновых оснований равно количеству пиримидиновых оснований, т.е. (А+Г)=(Ц+Т).
2) Количество аденина равно количеству тимина (А=Т); аналогично количество гуанина равно количеству цитозина (Г=Ц).
3) Количество оснований, содержащих аминогруппу в положении 4 пиримидинового и положении 6 пуринового ядра, равно количеству оснований, содержащих в этих же положениях оксогруппу. Это означает, что А+Ц=Г+Т.
Для РНК правила Чаргаффа либо не выполняются, либо выполняются с некоторым приближением. Это обусловлено тем, что в составе РНК содержится много минорных оснований.
Сравнение макромолекулы ДНК с винтовой лестницей наводит на мысль об ее хиральности. Действительно, природные ДНК обладают оптической активностью. В то же время смеси нуклеотидов, составляющих ДНК, а также разупорядоченные полинуклеотические цепи оптически неактивны. Это свидетельствует о том, что оптическая активность природных ДНК связана с хиральностью их вторичной структуры.
Каркас спирали образован чередующимися углеводными и фосфатными остатками. Окружающая водная среда контактирует с гидрофильной частью спирали, а внутренняя часть спирали (основания) с водой не контактирует.
Молекула ДНК, в отличие от молекулы РНК, в большинстве случаев состоит из двух комплементарных взаимозакрученных цепей. В зависимости от длины витка и угла спирали, а также ряда других ее геометрических параметров, различают, более десяти разнообразных упорядоченных спиральных структур ДНК. В стабилизации этих структур наряду с водородными связями, действующими поперек спирали, большую роль играют межмолекулярные взаимодействия, направленные вдоль спирали между соседними пространственно сближенными азотистыми основаниями. Поскольку эти взаимодействия направлены вдоль стопки азотистых оснований молекулы ДНК, их называют стэкинг-взаимодействиями. Таким образом, взаимодействия азотистых оснований между собой скрепляют двойную спираль молекулы ДНК и вдоль, и поперек ее оси.
Сильное стэкинг-взаимодействие всегда усиливает водородные связи между основаниями, способствуя уплотнению спирали. Вследствие этого молекулы воды из окружающего раствора связываются в основном с пентозофосфатным остовом ДНК, полярные группы которого находятся на поверхности спирали. При ослаблении стэкинг-взаимодействия молекулы воды, проникая внутрь спирали, конкурентно взаимодействуют с полярными группами оснований, инициируют дестабилизацию и способствуют дальнейшему распаду двойной спирали. Все это свидетельствует о динамичности вторичной структуры ДНК под воздействием компонентов окружающего раствора. Двойная спираль характерна для большинства молекул ДНК. Однако ДНК может иметь и другие формы. В некоторых вирусах содержится одноцепочечная ДНК, встречаются также кольцевые формы.
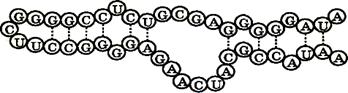 |
Биспиральные структуры в молекулах РНК возникают в пределах одной и той же цепи в тех зонах, где расположены комплементарные азотистые основания аденин - урацил и гуанин - цитозин (рис. 16). В результате вторичная структура молекулы РНК содержит биспиральные участки и петли, число и размеры которых определяются первичной структурой молекулы и составом окружающего раствора.
Рис. 16. Вторичная структура молекулы РНК
Третичная структура нуклеиновых кислот. Двойная спираль молекул ДНК существует в виде линейной, кольцевой, суперкольцевой и компактных клубковых форм. Между этими формами совершаются взаимные переходы при действии особой группы ферментов – топоизомераз, изменяющих пространственную структуру (рис 17).
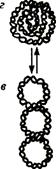 | 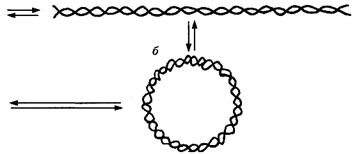 | ||
Рис. 17. Третичная структура молекулы ДНК:
а -линейная, б - кольцевая, в - суперкольцевая, г - компактный клубок
Третичная структура многих молекул РНК пока еще требует окончательного выяснения, но уже установлено, что она зависит не только от первичной и вторичной структуры, но и от состава окружающего раствора.
