Скорость химических реакций.
Любая термодинамически разрешенная химическая реакция должна быть обусловлена определенными факторами, от которых зависят скорость и стадийность (механизм) ее протекания. Скорость и механизм химических процессов составляют основу химическойкинетики. Формальная кинетика позволяет количественно описать ход химического процесса во времени при постоянной температуре в зависимости от концентрации реагирующих веществ и их фазового состава.
Скорость гомогенной химической реакции определяется по изменению концентрации любого из реагирующих веществ в единицу времени. Обычно концентрации выражают в моль/л, а время в секундах. Например, скорость реакции
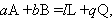 |
может быть, с одной стороны, определена по убыли веществ A или В, а с другой стороны, по приращению продуктов реакции L и Q. Поскольку все вещества этой реакции взаимодействуют в стехиометрических соотношениях, то скорость реакции может быть выражена через изменение концентрации любого реагента. Другими словами, при фиксированной температуре скорость гомогенной реакции Vi определяется убылью или приращением концентрации реагента Ci за бесконечно малое время dτ:
| (5.1) |
Так, скорость реакции N2(г) + 3H2(г) = 2NH3(г) может быть выражена соотношением
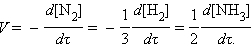 |
Выполнить вопрос из теста №16.
Закон действующих масс.
Скорость реакции в момент τ – мгновенная скорость Vτ – подчиняется закону действующих масс, который был экспериментально открыт и теоретически обоснован в середине XIX столетия и получил свое название от термина «действующая масса» – синонима современного понятия «концентрация».
Рассмотрим взаимодействие молекулы А с молекулой В в неком объеме (рис. 5.1).
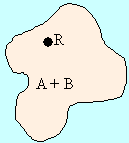 |
| Рисунок 5.1. Схема взаимодействияА и В (к выводу ЗДМ). |
Пусть реакция происходит в некоторой точке R через предшествующее взаимодействию столкновение. Если молярные концентрации веществ А и В выразить через их символы в квадратных скобках, то вероятность нахождения веществ А в точке R будет пропоциональна [A], т. е. ωA=α[A]. Вероятность ωB нахождения вещества в этой точке равна ωB = β[B], а вероятность их одновременного присутствия в точке R (точке столкновения) равна произведению ωA∙ωВ = α[A]∙β[B]. Поскольку только часть столкновений приводит к химической реакции, то скорость реакции образования АВ равна VAB = γ∙α[A]∙β[B] = γαβ[A][B]. Обозначив γ·α·β = k, получаем для реакции A + B, VAB = k [A] [B]
Коэффициент пропорциональности называют константой скорости. Очевидно, для реакции aA + bB, то есть для a молей вещества А и b молей вещества В ЗДМ формально запишется в виде
|
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов. Это определение относится к гомогенным реакциям. Если реакция геторогенная (реагенты находятся в разных агрегатных состояниях), то в уравнениие ЗДМ входят только жидкие или только газообразные реагенты, а твердые исключаются, оказывая влияние только на константу скорости k. Константа скорости k численно равна скорости, если концентрации реагентов постоянны и равны единице.
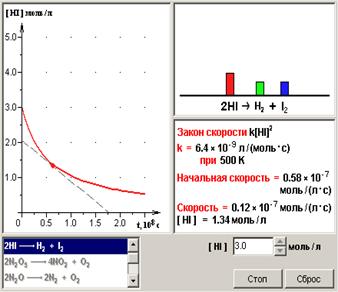 |
| Модель 5.1. Скорости химических реакций. На примере этой модели вам предлагается изучить зависимость скорости реакции от ее вида и концентрации реагентов. Важную роль в этой зависимости играет величина, называемая порядком реакции. Порядок реакции – это степень, в которую нужно возвести концентрацию реагента, чтобы, домножив ее на константу скорости, получить скорость реакции в данный момент. Порядок реакции при малых концентрациях реагентов определяется количеством взаимодействующих молекул вещества в одном акте реакции. В данной модели собраны реакции первого и второго порядков. Обратите внимание на графики зависимости концентраций от времени. Вы можете, запуская процесс для нескольких начальных концентраций в одной и той же реакции, увидеть все кривые на одном и том же рисунке. Интересно сравнить поведение этих семейств кривых для реакций первого и второго порядков. В реакции первого порядка зависимость от начальных параметров прослеживается гораздо сильнее (пучок кривых достаточно широк в конечной части). В реакциях второго порядка, где скорость сильнее зависит от концентрации, зависимость от начальных параметров из-за этого быстро уменьшается. В результате расстояние между кривыми для разных начальных концентраций быстро становится очень небольшим. Обратите также внимание, что графики различных реакций одного порядка весьма похожи по виду, несмотря на большие различия в константе скорости. Это вызвано тем, что масштаб, в котором рисуется график, в данной модели также выбирается в зависимости от константы скорости. Сама скорость реакции в процессе ее протекания выводится в числовом виде (чтобы детальнее рассмотреть ситуацию в процессе реакции, нажмите на кнопку «Стоп»). Также эта скорость может быть получена как тангенс угла наклона касательной к графику в рассматриваемой точке, взятый с обратным знаком. Касательная показана в виде пунктирной прямой. Видно, что ее наклон в процессе реакции уменьшается так же как и уменьшается скорость реакции из-за уменьшения концентрации реагентов. |
Закон действующих масс безусловно выполняется только для элементарных химических реакций, протекающих в одну стадию. В других случаях фактическая и вычисленная по закону действующих масс скорости совпадают редко.
Порядок химических реакций.
Молекулярность реакции – это минимальное число молекул, участвующих в элементарном химическом процессе. По молекулярности элементарные химические реакции делятся на молекулярные (А →) и бимолекулярные (А + В →); тримолекулярные реакции встречаются чрезвычайно редко. Если реакция протекает последовательно через несколько гомогенных или гетерогенных элементарных стадий, то суммарная скорость всего процесса определяется самой медленной его частью, а молекулярность заменяется порядком реакции – формальным показателем при концентрации реагирующих веществ. Поэтому весь процесс в целом лучше характеризует порядок реакции. Кинетическое уравнение реакции только для элементарных стадий совпадает с выражением ЗДМ. В этих случаях молекулярность и порядок реакции совпадают, хотя и не всегда. Так, при избытке одного из компонентов элементарной реакции А + В (А >> В) скорость реакции будет практически зависеть от изменения концентрации вещества В (А = const), поэтому порядок бимолекулярной реакции понижается до первого. Аналогично тому, что скорость реакции может характеризоваться по любому веществу, участвующему в реакции, для реакции aА + bВ → кинетические уравнения по веществу А и веществу В выглядят соответственно
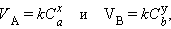 |
а общее кинетическое уравнение –
| (5.2) |
Здесь z = x + y – общий порядок реакции. Запишем кинетическое уравнение в дифференциальной форме для разных исходных реагентов:
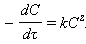 |
Разделение переменных и интегрирование в пределах от нуля до τ дает приведенные в таб. 5.1 уравнения для реакций первого, второго и третьего порядков.
| ||||||||||||
| Таблица 5.1. Кинетические уравнения и период полупревращения реакций первого, второго и третьего порядков. |
Решения кинетических уравнений 2-го и 3-го порядка, приведенные в таблице 5.1, справедливы только при равных начальных концентрациях веществ
В каждом случае кинетическое уравнение линейно в соответствующих координатах С(τ), что позволяет графически определить порядок реакции (рис. 5.2).
 |
| Рисунок 5.2. Зависисмости C = f (τ) для реакций первого, второго и третьего порядков. |
Прологарифмировав уравнение (5.2), получим lgV = lgK + z lgC; из графической зависимости (рис. 5.2) получаем lgK и z = tg φ.
Порядок реакции, особенно гетерогенной, может быть не только целочисленным (в том числе и нулевым), но и дробным. Нулевой порядок реакции указывает на постоянство скорости во времени.
Для гетерогенной реакции C(тв) + О2(г) = СО2(г) можно создать концентрационнные условия, при которых порядок реакции будет меняться в пределах от нуля до единицы. Действительно, при больших парциальных давлениях кислорода 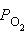 в приповерхностном слое твердого углерода большой концентрационный градиент способствует практически мгновенному восполнению прореагировавшего кислорода. Следствием этого оказывается постоянство скорости реакции по кислороду, поскольку
в приповерхностном слое твердого углерода большой концентрационный градиент способствует практически мгновенному восполнению прореагировавшего кислорода. Следствием этого оказывается постоянство скорости реакции по кислороду, поскольку 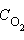 ~ const. Поэтому реакция горения углерода будет в этих условиях подчиняться кинетическому уравнению нулевого порядка. При уменьшении парциального давления кислорода, начиная с некоторого
~ const. Поэтому реакция горения углерода будет в этих условиях подчиняться кинетическому уравнению нулевого порядка. При уменьшении парциального давления кислорода, начиная с некоторого 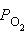 скорость реакции будет соответствовать кинетическому уравнению первого порядка
скорость реакции будет соответствовать кинетическому уравнению первого порядка 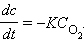 При промежуточных давлениях кислорода порядок реакции изменяется в интервале от 0 до 1.
При промежуточных давлениях кислорода порядок реакции изменяется в интервале от 0 до 1.
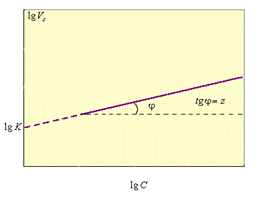 |
| Рисунок 5.3. Зависимость V = f (lgC). |

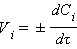
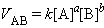
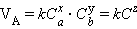
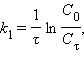 [с–1]
[с–1] 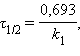 [с–1]
[с–1] 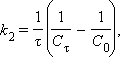 [л∙моль∙с–1]
[л∙моль∙с–1] 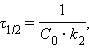 [л∙моль–1∙с–1]
[л∙моль–1∙с–1] 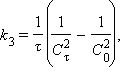 [л2∙моль–2∙с–1]
[л2∙моль–2∙с–1] 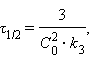 [л2∙моль–2∙с–1]
[л2∙моль–2∙с–1]