Корпускулярно-волновые свойства частиц.
В 20-х годах XX столетия было установлено, что любая частица имеет корпускулярно-волновую природу. Согласно теории Л. де Бройля (1924 г.), каждой частице с импульсом  соответствует волновой процесс с длиной волны λ, т.е. λ = h / p. Чем меньше масса частицы, тем больше длина волны. Для элементарных частиц В. Гейзенберг сформулировал принцип неопределенности, согласно которому невозможно одновременно определить положение частицы в пространстве и ее импульс. Следовательно, нельзя рассчитать траекторию движения электрона в поле ядра, можно лишь оценить вероятность его нахождения в атоме с помощью волновой функции ψ, которая заменяет классическое понятие траектории. Волновая функция ψ характеризует амплитуду волны в зависимости от координат электрона, а ее квадрат ψ2 определяет пространственное распределение электрона в атоме. В наиболее простом варианте волновая функция зависит от трех пространственных координат и дает возможность определить вероятность нахождения электрона в атомном пространстве или его орбиталь. Таким образом, атомная орбиталь (АО) – область атомного пространства, в котором вероятность нахождения электрона наибольшая. Волновые функции получаются при решении основополагающего соотношения волновой механики – уравнения Шредингера. (Точное решение получается для атома водорода или водородоподобных ионов, для многоэлектронных систем используются различные приближения). Поверхность, ограничивающая 90–95 % вероятности нахождения электрона или электронной плотности, называют граничной. Атомная орбиталь и плотность электронного облака имеют одинаковую граничную поверхность (форму) и одинаковую пространственную ориентацию. Атомные орбитали электрона, их энергия и направление в пространстве зависят от четырех параметров – квантовых чисел.
соответствует волновой процесс с длиной волны λ, т.е. λ = h / p. Чем меньше масса частицы, тем больше длина волны. Для элементарных частиц В. Гейзенберг сформулировал принцип неопределенности, согласно которому невозможно одновременно определить положение частицы в пространстве и ее импульс. Следовательно, нельзя рассчитать траекторию движения электрона в поле ядра, можно лишь оценить вероятность его нахождения в атоме с помощью волновой функции ψ, которая заменяет классическое понятие траектории. Волновая функция ψ характеризует амплитуду волны в зависимости от координат электрона, а ее квадрат ψ2 определяет пространственное распределение электрона в атоме. В наиболее простом варианте волновая функция зависит от трех пространственных координат и дает возможность определить вероятность нахождения электрона в атомном пространстве или его орбиталь. Таким образом, атомная орбиталь (АО) – область атомного пространства, в котором вероятность нахождения электрона наибольшая. Волновые функции получаются при решении основополагающего соотношения волновой механики – уравнения Шредингера. (Точное решение получается для атома водорода или водородоподобных ионов, для многоэлектронных систем используются различные приближения). Поверхность, ограничивающая 90–95 % вероятности нахождения электрона или электронной плотности, называют граничной. Атомная орбиталь и плотность электронного облака имеют одинаковую граничную поверхность (форму) и одинаковую пространственную ориентацию. Атомные орбитали электрона, их энергия и направление в пространстве зависят от четырех параметров – квантовых чисел.
 |
| Модель 2.1. Принцип неопределенности. |
Программа представляет компьютерный эксперимент по прохождению электронного пучка через одну или две щели. Она позволяет познакомиться с проявлением двойственной природы микрообъектов, то есть наличием у них волновых и корпускулярных свойств. Иллюстрируется принцип неопределенности Гейзенберга.
Известно, что свет обладает как волновыми, так и корпускулярными свойствами. Волновые свойства проявляются при распространении света (интерференция, дифракция). Корпускулярные свойства проявляются при взаимодействии света с веществом (фотоэффект, излучение и поглощение света атомами).
Свойства фотона как частицы (энергия E и импульс p) связаны с его волновыми свойствами (частотой ν и длиной волны λ) соотношениями
| E = hν; p = hν / c = h / λ, |
где h = 6,63·10–34 Дж∙c – постоянная Планка.
Французский физик Луи де Бройль в 1924 г. высказал предположение, что сочетание волновых и корпускулярных свойств присуще не только свету, но и любому материальному телу. Согласно де Бройлю, каждому телу массой m, движущемуся со скоростью v, соответствует волновой процесс с длиной волны
| λ = h / p. |
Наиболее отчетливо волновые свойства проявляются у элементарных частиц. Это происходит потому, что из-за малой массы частиц длина волны оказывается сравнимой с расстоянием между атомами в кристаллических решетках. В этом случае при взаимодействии пучка частиц с кристаллической решеткой возникает дифракция. Например, электронам с энергией 150 эВ соответствует длина волны λ ≈ 10–10 м. Такого же порядка межатомные расстояния в кристаллах. Поэтому пучок электронов будет рассеиваться на кристалле как волна, т. е. по законам дифракции.
Для иллюстрации волновых свойств частиц часто используют мысленный эксперимент – прохождение пучка электронов (или других частиц) через щель шириной Δx. С точки зрения волновой теории после дифракции на щели пучок будет уширяться с угловой расходимостью θ ≈ λ / Δx. С корпускулярной точки зрения уширение пучка после прохождения щели объясняется появлением у частиц некоторого поперечного импульса. Разброс значений этого поперечного импульса («неопределенность») есть
| Δpx ≈ θp ≈ (λ / Δx)p ≈ h / Δx |
Соотношение
| ΔpxΔx ≈ h |
носит название соотношения неопределенностей. Это соотношение на корпускулярном языке выражает наличие волновых свойств у частиц.
Эксперимент по прохождению пучка электронов через две близко расположенные щели может служить еще более яркой иллюстрацией волновых свойств частиц. Этот эксперимент является аналогом оптического интерференционного опыта Юнга.
Квантовые числа электрона.
Квантовое число n – главное. Оно определяет энергию электрона в атоме водорода и одноэлектронных системах (He+, Li2+ и т. д.). В этом случае энергия электрона
 |
n принимает значения от 1 до ∞. Чем меньше n, тем больше энергия взаимодействия электрона с ядром. При n = 1 атом водорода находится в основном состоянии, при n > 1 – в возбужденном.
В многоэлектронных атомах электроны с одинаковыми значениями n образуют слой или уровень, обозначаемый буквами K, L, M, N, O, P и Q. Буква K соответствует первому уровню, L – второму и т. д.
 | ||||||||||||
| Модель 2.2. Атом водорода. Программа предназначена для изучения квантовых свойств атомных систем. Она позволяет познакомиться с понятием энергетических уровней атома водорода, с правилом квантования стационарных боровских орбит, а также с квантовыми переходами между уровнями. Первый шаг на пути создания квантовой теории атомов был сделан Н. Бором (1913 г.). Свои представления об особых свойствах атомов Бор сформулировал в виде постулатов. 1. Атомная система может находиться только в особых стационарных или квантовых состояниях, каждому из которых соответствует определенная энергия; в стационарных состояниях атом не излучает. 2. При переходе атома из одного стационарного состояния в другое испускается или поглощается квант электромагнитного излучения (фотон). Энергия излученного или поглощенного фотона равна разности энергий стационарных состояний:
3. где h = 6,63·10–34 Дж – постоянная Планка, ν – частота фотона. Оба этих постулата противоречат законам классической физики, но они хорошо согласуются с экспериментальными результатами. 4. Третий постулат Бора определяет правило квантования стационарных орбит. Для случая круговых орбит электронов в планетарной модели атома третий постулат Бора записывается в виде:
5. где m – масса электрона, v – его скорость, r – радиус стационарной орбиты. Целое число n называют квантовым числом. В применении к круговым орбитам атома водорода квантовые постулаты Бора приводят к следующим соотношениям: Радиусы стационарных орбит:
где r1 = ε0h2 / πme2 = 5·10–11 м – радиус первой боровской орбиты. Энергия стационарных состояний:
Низшее энергетическое состояние атома (n=1) называется основным. Для атома водорода E1 = –21,7·10–19 Дж = –13,6 эВ. Эта энергия называется энергией ионизации. Процесс перехода на более высокую орбиту сопровождается поглощением, а на более низкую - испусканием фотона соответствующей частоты. Спектральная линия, соответствующая последнему переходу, начинает мигать на спектре (изображен в нижней части модели), а также изображается стрелкой на энергетической диаграмме. Обратите внимание, что переходы с наименьшей энергией возникают между наиболее удаленными от ядра боровскими орбитами. |
Орбитальное квантовое число l характеризует форму орбиталей и принимает значения от 0 до n – 1. Кроме числовых l имеет буквенные обозначения
| l | = | … | |||||
| l | = | s | p | d | f | g | … |
Электроны с одинаковым значением l образуют подуровень.
Квантовое число l определяет квантование орбитального момента количества движения электрона  в сферически симметричном кулоновском поле ядра.
в сферически симметричном кулоновском поле ядра.
Квантовое число ml называют магнитным. Оно определяет пространственное расположение атомной орбитали и принимает целые значения от –l до +l через нуль, то есть 2l + 1 значений. Расположение орбитали характеризуется значением проекции вектора орбитального момента количества движения Mz на какую-либо ось координат (обычно ось z):
 |
Все вышесказанное можно представить таблицей:
| ||||||||||||||||||
| Таблица 2.1. Число орбиталей на энергетических подуровнях. |
Орбитали одного подуровня (l = const) имеют одинаковую энергию. Такое состояние называют вырожденным по энергии. Так p-орбиталь – трехкратно, d – пятикратно, а f – семикратно вырождены.
Граничные поверхности s-, p-, d-, f- орбиталей показаны на рис. 2.1.
 |
| Рисунок 2.1. Изображение с помощью граничных поверхностей s-, p-, d- и f-орбиталей. |
s-Орбитали сферически симметричны для любого n и отличаются друг от друга только размером сферы. Их максимально симметричная форма обусловлена тем, что при l = 0 и μl = 0.
p-Орбитали существуют при n ≥ 2 и l = 1, поэтому возможны три варианта ориентации в пространстве: ml = –1, 0, +1. Все p-орбитали обладают узловой плоскостью, делящей орбиталь на две области, поэтому граничные поверхности имеют форму гантелей, ориентированных в пространстве под углом 90° друг относительно друга. Осями симметрии для них являются координатные оси, которые обозначаются px, py, pz.
d-Орбитали определяются квантовым числом l = 2 (n ≥ 3), при котором ml = –2, –1, 0, +1, +2, то есть характеризуются пятью вариантами ориентации в пространстве. d-Орбитали, ориентированные лопастями по осям координат, обозначаются dz² и dx²–y², а ориентированные лопастями по биссектрисам координатных углов – dxy, dyz, dxz.
Семь f-орбиталей, соответствующих l = 3 (n ≥ 4), изображаются в виде граничных поверхностей, приведенных на рис. 2.1.
Квантовые числа n, l и ml не полностью характеризуют состояние электрона в атоме. Экспериментально установленно, что электрон имеет еще одно свойство – спин. Упрощенно спин можно представить как вращение электрона вокруг собственной оси. Спиновое квантовое число ms имеет только два значения ms = ±1/2, представляющие собой две проекции углового момента электрона на выделенную ось. Электроны с разными ms обозначаются стрелками, направленными вверх 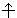 и вниз
и вниз 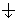 .
.
В многоэлектронных атомах, как и в атоме водорода, состояние электрона определяется значениями тех же четырех квантовых чисел, однако в этом случае электрон находится не только в поле ядра, но и в поле других электронов. Поэтому энергия в многоэлектронных атомах определяется не только главным, но и орбитальным квантовым числом, а вернее их суммой: энергия атомных орбиталей возрастает по мере увеличения суммы n + l; при одинаковой сумме сначала заполняется уровень с меньшим n и большим l. Энергия атомных орбиталей возрастает согласно ряду
| 1s < 2s < 2p < 3s < 3p < 4s ≈ 3d < 4p < 5s ≈ 4d < 5p < 6s ≈ 4f ≈ 5d < 6p < 7s ≈ 5f ≈ 6d < 7p. |
Итак, четыре квантовых числа описывают состояние электрона в атоме и характеризуют энергию электрона, его спин, форму электронного облака и его ориентацию в пространстве. При переходе атома из одного состояния в другое происходит перестройка электронного облака, то есть изменяются значения квантовых чисел, что сопровождается поглощением или испусканием атомом квантов энергии.
Выполнить вопросы №11, №13 из теста.
