Реакции с участием гидроксогруппы (OH)
Взаимодействуют со щелочными металлами
2C2H5 OH+2Na--->2C2H5 ONa + H2
Взаимодействуют с галогеноводородными кислотами
C2H5 OH + HBr--->C2H5Br +HOH
Реакции этерификации
(при этом образуются сложные эфиры)
CH3-COOH + OH-C2H5 →HOH + CH3-CO– O -C2H5 (t°, к.H2SO4 )
Дегидратация спиртов
а) внутримолекулярная
H3С-СH2OH →CH2=CH2 + H2O (t°>140°С, к.H2SO4 в избытке)
б) межмолекулярная (t°<140°С, к.H2SO4 )
2 C2H5 OH →H2O + C2H5 -O–C2H5
Реакции окисления
Горение - полное окисление
C2H5 OH + 3O2→2CO2 + 3H2O
Окисление окислителями
H3C-CН2-OH + CuO → H2O + Cu + CH3-CОH (t°)


| Билет 11. |
1. Электрохимический ряд напряжений металлов. Вытеснение металлов из растворов солей другими металлами.    |
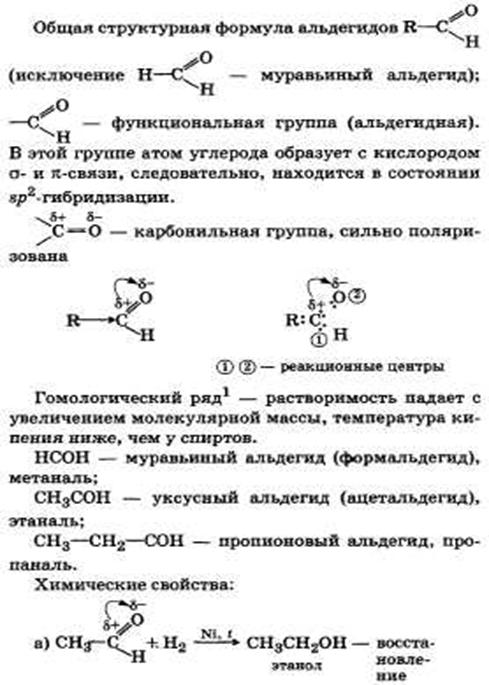
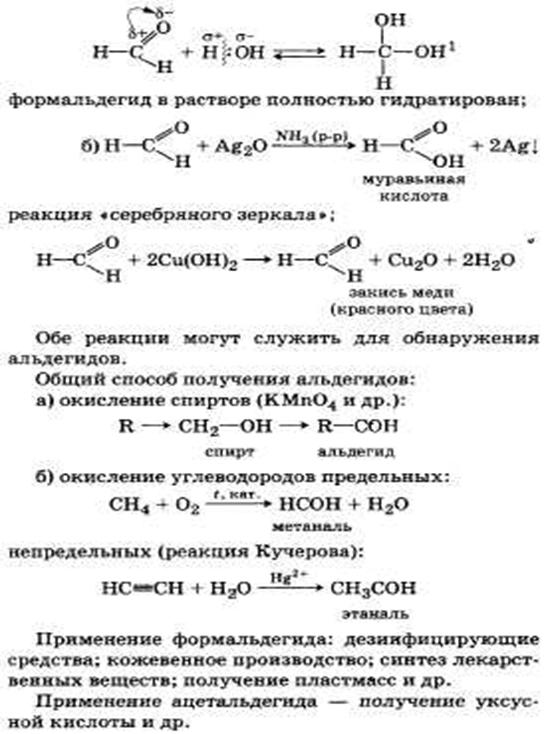
Альдегиды, их химическое строение и свойства. Получение, применение муравьиного и уксусного альдегидов.
Билет 12.
Водородные соединения неметаллов. Закономерности в изменении их свойств в связи с положением химических элементов в периодической системе Д. И. Менделеева.




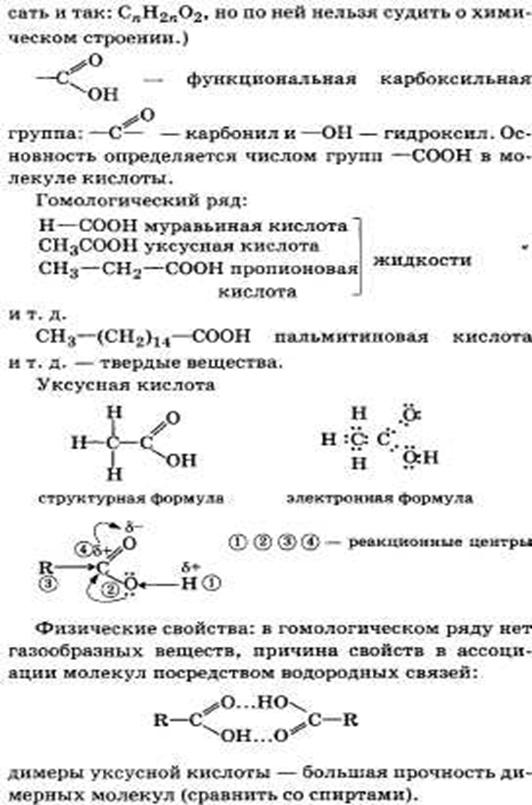
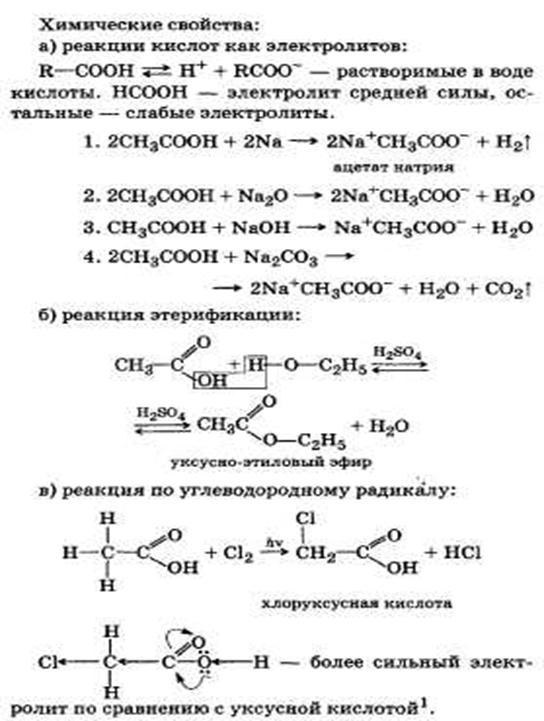
2. Предельные одноосновные карбоновые- кислоты, их строение и свойства на примере уксусной кислоты.


Билет 13.
Высшие оксиды химических элементов третьего периода. Закономерности в изменении их свойств в связи с положением химических элементов в периодической системе Д. И. Менделеева. Характерные химические свойства оксидов: основных, амфотерных, кислотных.
Реакционная способность элементов во взаимодействии с кислородом, вообще говоря, уменьшается при перемещении вправо вдоль каждого периода. Например, в 3-м периоде два s-металла, натрий и магний, и два р-элемента, алюминий и фосфор, бурно реагируют с кислородом, образуя оксиды. В том же периоде элементы кремний и сера способны только медленно реагировать с кислородом. Хлор и аргон, расположенные в правом конце периода, вообще не реагируют с кислородом.
Электроположительные s-металлы образуют ионные оксиды, как, например, оксид натрия Na2O и оксид магния MgO. Оксиды элементов, расположенных в средней и правой частях периода, являются преимущественно ковалентными соединениями, как, например, оксиды азота и серы.
Кислотно-основный характер оксидов тоже изменяется от основного у оксидов элементов левой части периода к амфотерному у оксидов элементов средней части периода и далее к кислотному у оксидов элементов правой части периода. Например, s-металлы обычно образуют оксиды, которые растворяются в воде с образованием щелочных растворов:
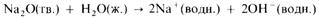
Молекулярные оксиды р-элементов, например диоксид углерода и триоксид серы, обычно обладают кислотными свойствами. Закономерное изменение основных свойств с переходом к кислотным свойствам наглядно проявляется у оксидов элементов 3-го периода.
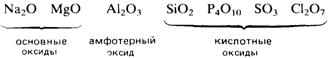
Жиры, их состав и свойства. Жиры в природе, превращение жиров в организме. Продукты технической переработки жиров, понятие о синтетических моющих средствах.


Билет 14.
1. Кислоты, их классификация и химические свойства на основе представлений об электролитической диссоциации. Особенности свойств концентрированной серной кислоты на примере взаимодействия с медью.
