Адсорбция и абсорбция. Изотермы адсорбции.
Адсорбция-процесс изменения концентрации у поверхности раздела двух фаз, а в более узком и употребительном- это повышение концентрации одного вещества у поверхности раздела двух фаз, из которых одна обычно является твердым телом.
Поглощаемое вещество, ещё находящееся в объёме фазы, называют адсорбтив, поглощённое — адсорбат. В более узком смысле под адсорбцией часто понимают поглощение примеси из газа или жидкости твёрдым веществом — адсорбентом. При этом, как и в общем случае адсорбции, происходит концентрирование примеси на границе раздела адсорбент-жидкость либо адсорбент-газ. Процесс, обратный адсорбции, то есть перенос вещества с поверхности раздела фаз в объём фазы, называется десорбция.
Абсорбция- поглощения сорбата всем объёмом сорбента. Абсорбция — частный случай сорбции.
Абсорбция, как правило, означает поглощение газов в объёме жидкости или реже твёрдого тела. Поглощение твёрдым абсорбентом, например, водорода палладием, называют окклюзией. Для процесса поглощения молекул газа или жидкости поверхностью твёрдого тела в русском языке используется термин адсорбция.
На практике абсорбции подвергают не отдельные газы, а газовые смеси, составные части которых поглощаются жидкостью. Эти составные части смеси называют абсорбируемыми компонентами (абсорбат), а непоглощаемые части — инертным газом.
Поверхностное натяжение – избыток свободной энергии в поверхностном слое, отнесенный к 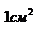 поверхности поглощающего тела.
поверхности поглощающего тела. 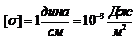 Поверхностное растяжение растворов зависит от природы растворителя и растворенного вещества, от концентрации последнего и от температуры. Поверхностное натяжение как функция концентрации растворенного вещества при Т-const - изотерма поверхностного натяжения.
Поверхностное растяжение растворов зависит от природы растворителя и растворенного вещества, от концентрации последнего и от температуры. Поверхностное натяжение как функция концентрации растворенного вещества при Т-const - изотерма поверхностного натяжения. 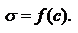
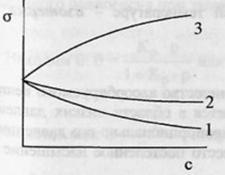
1 и 2 – поверхностно-активные вещества (ПАВ).3 – поверхностно-инактивные вещества (ПИАВ).Разность с в поверхностном слое– поверхностный избыток вещества Г (гамма).Для ПАВ Г>0, для ПИАВ Г<0.Поверхность твердых тел, как и жидкостей, обладает избыточной свободной энергией Гиббса. Твердые тела не могут (в отличие от жидкостей) самопроизвольно изменять площадь поверхности.Величина адсорбции зависит от природы адсорбента и адсорбата, от давления газа, температуры.Зависимость адсорбируемого количества газа от давления адсорбата при постоянной температуре – изотерма адсорбции. С ростом давления увеличивается количество адсорбируемого вещества.Лэнгмюр при выводе уравнения изотермы сделал следующие допущения: 1. все 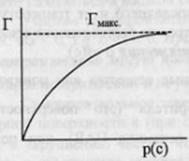 места адсорбента одинаковы. 2. взаимодействие между частицами пренебрежимо мало. 3. адсорбционный слой состоит из одного слоя молекул, адсорбция локализованная – нет перемещения адсорбционного комплекса вдоль поверхности адсорбента.Степень заполнения адсорбента адсорбатом:
места адсорбента одинаковы. 2. взаимодействие между частицами пренебрежимо мало. 3. адсорбционный слой состоит из одного слоя молекул, адсорбция локализованная – нет перемещения адсорбционного комплекса вдоль поверхности адсорбента.Степень заполнения адсорбента адсорбатом: 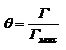 Скорость адсорбции:
Скорость адсорбции: 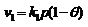
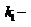 константа скорости адсорбции.Скорость десорбции:
константа скорости адсорбции.Скорость десорбции: 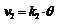
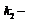 константа скорости десорбции.Адсорбционное равновесие наступает при
константа скорости десорбции.Адсорбционное равновесие наступает при 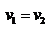 Уравнение изотермы хорошо передает зависимости в области низких и области высоких давлений, но не всегда оправдывается в промежуточной области.Процесс адсорбции экзотермичен: поглощение вещества протекает с выделением теплоты, десорбция – с поглощением теплоты.Если адсорбируются несколько газов:
Уравнение изотермы хорошо передает зависимости в области низких и области высоких давлений, но не всегда оправдывается в промежуточной области.Процесс адсорбции экзотермичен: поглощение вещества протекает с выделением теплоты, десорбция – с поглощением теплоты.Если адсорбируются несколько газов: 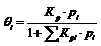 Для адсорбции на неоднородной поверхностибыло предложено эмпирическое уравнение Фрейндлиха.
Для адсорбции на неоднородной поверхностибыло предложено эмпирическое уравнение Фрейндлиха. 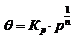
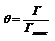
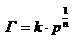 к и n – коэффициенты, постоянные для данного адсорбента и газа при данной температуре. Уравнение Фрейндлиха, наоборот, не отражает особенностей изотермы в области высоких и низких давлений, но для области промежуточных давлений согласуются с опытными данными.
к и n – коэффициенты, постоянные для данного адсорбента и газа при данной температуре. Уравнение Фрейндлиха, наоборот, не отражает особенностей изотермы в области высоких и низких давлений, но для области промежуточных давлений согласуются с опытными данными.
