Кристаллическое состояние вещества. Химическая связь в кристаллах.
Твердые вещества могут находиться в аморфном или кристаллическом состояниях. Вещества в аморфном состоянии не имеют четкой структуры, их иногда называют «переохлажденными жидкостями с аномально высокой вязкостью». Кристаллические структуры.Наименьшая структурная единица – элементарная ячейка. В зависимости от решеток и углов между характеристическими осями различают 7 основных видов (кубическая, ромбоэдрическая и пр.).Тип кристаллической системы определяется природой и размерами частиц, видом химических связей между ними, температурой и другими факторами.Многие соединения могут существовать в двух и более кристаллических структурах. Это явление – полиморфизм. Все кристаллы можно разделить по видам химической связи. Стоит отметить, что существуют кристаллы со смешанными связями.
1. Молекулярная связь.В узлах кристаллических решеток находятся молекулы, между которыми дейтсвуют вандерваальсовы силы, имеющие невысокую энергию.Для кристаллов с молекулярными связями характерны низкие температуры плавления и высокая сжимаемость.
2. Ковалентная связь.В узлах кристаллов располагаются атомы, образующие прочные ковалентные связи. Это обуславливает высокую энергию решетки. Кристаллы с ковалентной связью - диэлектрики или полупроводники. Типичными примеры: алмаз и кремний.
3. Ионная связь.Структурные единицы – положительно и отрицательно заряженные ионы, между которыми происходит электростатическое взаимодействие, характеризуемое высокой энергией. Кристаллы с ионной связью при низких температурах являются диэлектриками. При температурах близких к температуре плавления они становятся проводниками электричества.
4. Металлическая связь.Специфические свойства металлов (высокая проводимость, теплопроводность, ковкость, пластичность, металлический блеск) можно объяснить особым типом связи – металлическая.Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно движутся валентные электроны, отщепившиеся от атомов при образовании ионов. Эти электроны удерживают вместе положительные ионы, в противном случае решётка распалась бы под действием сил отталкивания между ионами.
5. Смешанная связь.Тот или иной вид связи встречается редко, обычно – наложение двух или более связей.
63. Составные части системы и компоненты. Правило фаз. Диаграмма состояния однокомпонентной системы (на примере воды). ???? ДИАГРАММА
Составные части системы – химически индивидуальные вещества, составляющие данную систему и способные к самостоятельному существованию.В равновесной системе 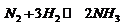 имеются 3 составных части.Константа равновесия:
имеются 3 составных части.Константа равновесия: 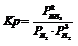 Если известны парциальные давления двух участников реакции, система определена.Независимые компоненты – индивидуальные вещества, наименьшее число которых необходимо и достаточно для образования всех фаз системы.Число независимых компонентов – разница между числом составных частей и числом связывающих уравнений.В данном примере: 3-1=2.Степени свободы – независимые переменные, которые можно произвольно менять, не нарушая состояния системы (числа и характера фаз).Правило фаз позволяет определить число фаз в системе при равновесии и изменение этого числа при изменении какого-либо параметра.
Если известны парциальные давления двух участников реакции, система определена.Независимые компоненты – индивидуальные вещества, наименьшее число которых необходимо и достаточно для образования всех фаз системы.Число независимых компонентов – разница между числом составных частей и числом связывающих уравнений.В данном примере: 3-1=2.Степени свободы – независимые переменные, которые можно произвольно менять, не нарушая состояния системы (числа и характера фаз).Правило фаз позволяет определить число фаз в системе при равновесии и изменение этого числа при изменении какого-либо параметра.  С – число степеней свободы, К – компоненты, Ф – фазы.Если
С – число степеней свободы, К – компоненты, Ф – фазы.Если 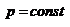 и
и 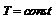 выражение
выражение 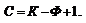 Пример. Определить кол-во фаз в системе
Пример. Определить кол-во фаз в системе 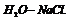 С=К-Ф+2=4-Ф. Максимальное число фаз=минимум С.
С=К-Ф+2=4-Ф. Максимальное число фаз=минимум С.