Кристаллическое состояние вещества
Агрегатные состояния вещества.
В этом разделе мы рассмотрим агрегатные состояния, в которых пребывает окружающая нас материя и силы взаимодействия между частицами вещества, свойственные каждому из агрегатных состояний.
Принято считать, что вещество может находиться в одном из трёх агрегатных состояниях:
1. Состояние твёрдого тела,
2. Жидкое состояние и
Газообразное состояние.
Часто выделяют четвёртое агрегатное состояние – плазму.
Иногда, состояние плазмы считают одним из видов газообразного состояния.
Плазма — частично или полностью ионизированный газ, чаще всего существующий при высоких температурах.
Плазма является самым распространённым состоянием вещества во вселенной, поскоьку материя звёд пребывает именно в этом состоянии.
Для каждого агрегатного состояния характерны особенности в характере взаимодействия между частицами вещества, что влияет на его физические и химические свойства.
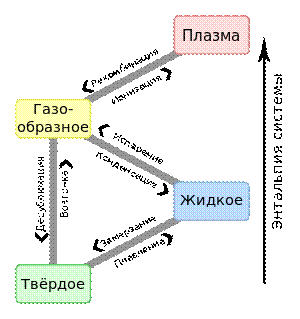
Каждое вещество может пребывать в разных агрегатных состояниях. При достаточно низких температурах все вещества находятся в твёрдом состоянии. Но по мере нагрева они становятся жидкостями, затем газами. При дальнейшем нагревании они ионизируются (атомы теряют часть своих электронов) и переходят в состояние плазмы.
Газ
Газообразное состояние (от нидерл. gas, восходит к др.-греч. Χάος) характеризующееся очень слабыми связями между составляющими его частицами.
Образующие газ молекулы или атомы хаотически движутся и при этом преобладающую часть времени находятся на больших (в сравнении с их размерами) растояниях друг от друга. Вследствие этого силы взаимодействия между частицами газа пренебрежимо малы.
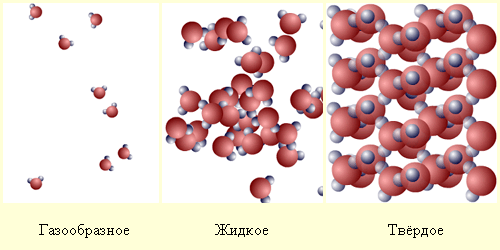
Основной особенностью газа является то, что он заполняет все доступное пространство, не образуя поверхности. Газы всегда смешиваются. Газ — изотропное вещество, то есть его свойства не зависят от направления.
При отсутствии сил тяготения давление во всех точках газа одинаково. В поле сил тяготения плотность и давление не одинаковы в каждой точке, уменьшаясь с высотой. Соответственно, в поле сил тяжести смесь газов становится неоднородной. Тяжелые газы имеют тенденцию оседать ниже, а более легкие — подниматься вверх.
Газ имеет высокую сжимаемость — при увеличении давления возрастает его плотность. При повышении температуры расширяются.
При сжатии газ может перейти в жидкость, но конденсация происходит не при любой температуре, а при температуре, ниже критической температуры. Критическая температура является характеристикой конкретного газа и зависит от сил взаимодействия между его молекулами. Так, например, газ гелий можно ожижить только при температуре, ниже от 4,2 К.
Существуют газы, которые при охлаждении переходят в твердое тело, минуя жидкую фазу. Превращения жидкости в газ называется испарением, а непосредственное превращение твердого тела в газ — сублимацией.
Твёрдое тело
Состояние твёрдого тела в сравнении с другими агрегатными состояниямихарактеризуется стабильностью формы.
Различают кристаллические и аморфные твёрдые тела.
Кристаллическое состояние вещества
Стабильность формы твёрдых тел связана с тем, что большинство, находящихся в твёрдом состоянии имеет кристалическое строение.
В этом случае расстояния между частицами вещества малы, а силы взаимодействия между ними велики, что и определяет стабильность формы.
В кристаллическом строении многих твёрдых тел легко убедиться, расколов кусок вещества и рассмотрев полученный излом. Обычно на изломе (например, у сахара, серы, металлов и пр.) хорошо заметны расположенные под разными углами мелкие грани кристаллов, поблескивающие вследствии различного отражения ими света.
В тех случаях, когда кристаллы очень малы, кристаллическое строение вещества можно установить при помощи микроскопа.
Формы кристаллов
Каждое вещество образует кристаллы совершенно определённой формы.
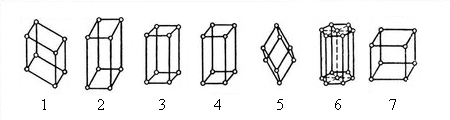
Разнообразие кристаллических форм может быть сведено к семи группам:
1. Триклинная (параллелепипед),
2.Моноклинная (призма с параллелограммом в основании),
3. Ромбическая (прямоугольный параллелепипед),
4. Тетрагональная (прямоугольный параллелепипед с квадратом в основании),
5. Тригональная,
6. Гексагональная (призма с основанием правильного центрированного
шестиугольника),
7. Кубическая (куб).
Многие вещества, в частности железо, медь, алмаз, хлорид натрия кристализуются вкубической системе. Простейшими формами этой системы являются куб, октаэдр, тетраэдр.
Магний, цинк, лёд, кварц кристализуются в гексагональной системе. Основные формы этой системы – шестигранные призмы и бипирамида.
Природные кристаллы, а также кристаллы, получаемые искусственным путём, редко в точности соответствуют теоретическим формам. Обычно при затвердевании расплавленного вещества кристаллы срастаются вместе и потому форма каждого из них оказывается не вполне правильной.
Однако как бы неравномерно не происходило развитие кристалла, как бы ни была искажена его форма, углы, под которыми сходятся грани кристалла у одного и того же вещества остаются постоянными.
Анизотропия
Особенности кристаллических тел не ограничиваются только формой кристаллов. Хотя вещество в кристалле совершенно однородно, многие из его физических свойств – прочность, теплопроводность, отношение к свету и др. – не всегда одинаковы по различным направлениям внутри кристалла. Эта важная особенность кристаллических веществ называется анизотропией.
Внутреннее строение кристаллов. Кристаллические решётки.
Внешняя форма кристалла отражает его внутреннее строение и обусловлена правильным расположением частиц, составляющих кристалл, - молекул, атомов или ионов.
Это расположение можно представить в виде кристаллической решётки – пространственного каркаса, образованного пересекающимися прямыми линиями. В точках пересечения линий – узлах решётки – лежат центры частиц.
В зависимости от природы частиц, находящихся в узлах кристаллической решётки, и от того, какие силы взаимодействия между ними преобладают в данном кристалле, различают следующие виды кристаллических решёток:
1. молекулярные,
2. атомные,
3. ионные и
4. металлические.
Молекулярные и атомные решётки присущи веществам с ковалентной связью, ионные – ионным соединениям, металические – металам и их сплавам.
· Атомные кристаллические решётки
В узлах атомных решёток находятся атомы. Они связаны друг с другомковалентной связью.
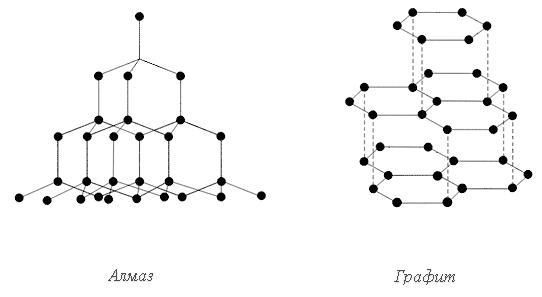
Веществ, обладающих атомными решётками, сравнительно мало. К ним принадлежаталмаз, кремний и некоторые неорганические соединения.
Эти вещества характеризуются высокой твёрдостью, они тугоплавки и нерастворимы практически ни в каких растворителях. Такие их свойства объясняются прочностьюковалентной связи.
· Молекулярные кристаллические решётки
В узлах молекулярных решёток находятся молекулы. Они связаны друг с другоммежмолекулярными силами.
Веществ с молекулярной решёткой очень много. К ним принадлежат неметаллы, за исключением углерода и кремния, все органические соединения с неионной связью имногие неорганические соединения.
Силы межмолекулярного взаимодействия значительно слабее сил ковалентной связи, поэтому молекулярные кристаллы имеют небольшую твёрдость, легкоплавки и летучи.
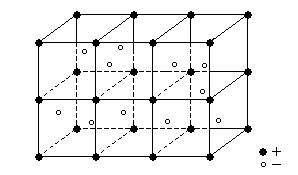
· Ионные кристаллические решётки
В узлах ионных решёток располагаются, чередуясь положительно и отрицательно заряженные ионы. Они связаны друг с другом силамиэлектростатического притяжения.
К соединениям с ионной связью, образующим ионные решётки, относится большинство солей и небольшое число оксидов.
По прочности ионные решётки уступают атомным, но превышают молекулярные.
Ионные соединения имеют сравнительно высокие температуры плавления. Летучесть их в большинстве случаев не велика.
· Металлические кристаллические решётки
В узлах металлических решёток находятся атомы металла, между которыми свободно движутся общие для этих атомов электроны.
Наличием свободных электронов в кристаллических решётках металлов можно объяснить их многие свойства: пластичность, ковкость, металлический блеск, высокую электро- и теплопроводность
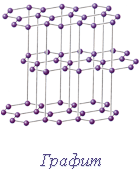
Существуют вещества, в кристаллах которых значительную роль играют два рода взаимодействия между частицами. Так, в графите атомы углерода связаны друг с другом в одних направлениях ковалентной связью, а в других – металлической. Поэтому решётку графита можно рассматривать и как атомную, и как металлическую.
Во многих неорганических соединениях, например, в BeO, ZnS, CuCl, связь между частицами, находящимися в узлах решётки, является частично ионной, а частичноковалентной. Поэтому решётки подобных соединений можно рассматривать как промежуточные между ионными и атомными.
