Кислоты и основания. Влияние положения элемента в периодической системе и степени окисления элемента на состав и кислотно-основные свойства гидроксидов элементов.
Форма гидроксидов с х ОН.Общая формула Э(ОН)х, где х = 1и 2, содержащая больше атомов кислорода и водорода, называется орто-формой, А форма с меньшим числом – мета-формой.
Основания – сложные вещества, молекулы которых состоят из атома металла (или иона NH4+) и одной или нескольких гидроксогрупп ОН, способных замещаться на кислотный остаток. Общая формула оснований Ме(ОН)х, где х – степень окисления металла.
Кислоты – сложные вещества, содержащие атомы водорода, которые могут замещаться катионами металла (или ионами аммония). Общая формула кислот НхАn.
Соли – продукты замещения (полного или частичного) атомов водорода в молекулах кислот катионами металла (а также ионами аммония), либо гидроксогрупп в молекулах оснований кислотными остатками.
Соли делятся на средние, кислые, основные, двойные, смешанные и комплексные. Средние соли – это продукт полного замещения атомов водорода. МехAny.
Кислотные соли – это продукт не полного замещения атомов водорода в молекулах только многоосновных кислот.
Основные соли – продукт неполного замещения гидроксогрупп в молекулах только многокислотных оснований кислотными остатками.
Двойные соли – содержит два химически разных катиона и один тип аниона.
Смешанные соли – содержат один тип катиона, но два типа аниона.
В состав комплексных солей входят сложные комплексные ионы (заключённые в квадратные скобки), устойчивые как в кристаллическом состоянии, так и при растворении в воде.
Название средней соли = Название кислотного остатка + Название металла (р.п.) + Степень окисления металла.
Кислотные и основные гидроксиды. Соли
Гидроксиды тип сложных веществ, в состав которых входят атомы некоторого элемента Е (кроме фтора и кислорода) и гидроксогруппы ОН; общая формула гидроксидов Е(ОН)n, где n = 1÷6. Форма гидроксидов Е(ОН)n называется орто-формой; при n > 2 гидроксид может находиться также в мета-форме, включающей кроме атомов Е и групп ОН еще атомы кислорода О, например Е(ОН)3 и ЕО(ОН), Е(ОН)4 и Е(ОН)6 и ЕО2(ОН)2.
Гидроксиды делят на две противоположные по химическим свойствам группы: кислотные и основные гидроксиды. Кислотные гидроксиды содержат атомы водорода, которые могут замещаться на атомы металла при соблюдении правила стехиометрической валентности. Большинство кислотных гидроксидов находится в мета-форме, причем атомы водорода в формулах кислотных гидроксидов ставят на первое место, например H2SO4, HNO3 и H2CO3, а не SO2(OH)2, NO2(OH) и CO(OH)2. Общая формула кислотных гидроксидов НхЕОу, где электроотрицательную составляющую ЕОух называют кислотным остатком. Если не все атомы водорода замещены на металл, то они остаются в составе кислотного остатка.
Названия распространенных кислотных гидроксидов состоят из двух слов: собственного названия с окончанием “ая” и группового слова “кислота”. Названия кислотных остатков используют при построении названий солей.
Кислоты - сложные вещества, состоящие из атомов водорода и кислотного остатка. (С точки зрения теории электролитической диссоциации: кислоты - электролиты, которые при диссоциации в качестве катионов образуют только H+).
Классификация
1. По составу: бескислородные и кислородсодержащие.
2. По числу атомов водорода, способных замещаться на металл: одно-, двух-, трёхосновные...
Бескислородные:
HCl - хлористоводородная (соляная), одноосновная, хлорид
HBr – бромистоводородная, одноосновная, бромид
HI – йодистоводородная, одноосновная, йодид
H2S – сероводородная, двухосновная. сульфид
Кислородсодержащие:
HNO3 – азотная, одноосновная, нитрат .
H2SO3 – сернистая, двухосновная, сульфит.
H2SO4 – серная, двухосновная, сульфат .
H2CO3 – угольная, двухосновная, карбонат .
H2SiO3 – кремниевая, двухосновная, силикат .
H3PO4 – ортофосфорная, трёхосновная,ортофосфат .
Получение :
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
SO3 + H2O = H2SO4
P2O5 + 3H2O = 2H3PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
H2 + Cl2 = 2HCl
H2 + S = H2S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + H2SO4 = BaSO4¯ + 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl = H2SiO3 + 2NaCl
2NaCl(тв.) + H2SO4(конц.) –t°® Na2SO4 + 2HCl
Химические свойства
1. Действие на индикаторы.
лакмус - красный
метилоранж - розовый
2. Взаимодействие с основаниями (реакция нейтрализации):
H2SO4 + 2KOH = K2SO4 + 2H2O
2HNO3 + Ca(OH)2 = Ca(NO3)2 + 2H2O
3. Взаимодействие с основными оксидами:
CuO + 2HNO3 –t°= Cu(NO3)2 + H2O
4. Взаимодействие с металлами:
Zn + 2HCl = ZnCl2 + H2
2Al + 6HCl= 2AlCl3 + 3H2
(металлы, стоящие в ряду напряжений до водорода, кислоты-неокислители).
5. Взаимодействие с солями (реакции обмена), при которых выделяется газ или образуется осадок:
H2SO4 + BaCl2 = BaSO4 +2HCl
2HCl + K2CO3 = 2KCl + H2O + CO2
Основные гидроксиды содержат гидроксид-ионы, которые могут замещаться на кислотные остатки при соблюдении правила стехиометрической валентности. Все основные гидроксиды находятся в орто-форме; их общая формула М(ОН)n, где n = 1,2 (реже 3,4) и Мn+ катион металла.
Получение:
1. Реакции активных металлов (щелочных и щелочноземельных металлов) с водой:
2Na + 2H2O = 2NaOH + H2
Ca + 2H2O = Ca(OH)2 + H2
2. Взаимодействие оксидов активных металлов с водой:
BaO + H2O = Ba(OH)2
3. Электролиз водных растворов солей
2NaCl + 2H2O = 2NaOH + H2 + Cl2
Химические свойства:
Щёлочи. Нерастворимые основания
1. Действие на индикаторы.
лакмус - синий
метилоранж - жёлтый
фенолфталеин - малиновый
2. Взаимодействие с кислотными оксидами.
2KOH + CO2 = K2CO3 + H2O
KOH + CO2 = KHCO3
3. Взаимодействие с кислотами (реакция нейтрализации) с образованием солей (реакция солеобразования), например:
Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
Ca(OH)2 + 2H2SO4 = Ca(HSO4)2 + 2H2O
2Ca(OH)2 + H2SO4 = Ca2SO4(OH)2 + 2H2O
NaOH + HNO3 = NaNO3 + H2O
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
4. Обменная реакция с солями
Ba(OH)2 + K2SO4 = 2KOH + BaSO4
3KOH+Fe(NO3)3 = Fe(OH)3 + 3KNO3
5. Термический распад.
Cu(OH)2 –t°= CuO + H2O
Соли тип сложных веществ, в состав которых входят катионы Мn+ и кислотные остатки*. Соли с общей формулой Мх(ЕОу) n называют среднимисолями, а соли с незамещенными атомами водорода, кислыми солями. Иногда соли содержат в своем составе также гидроксид или(и) оксид ионы; такие соли называют основными солями. Кислые и основные соли могут быть превращены в средние соли взаимодействием с соответствующим основным и кислотным гидроксидом, например:
Ca(HSO4)2 + Ca(OH) = CaSO4 + 2H2O
Ca2SO4(OH)2 + H2SO4 = 2CaSO4 + 2H2O
Соли - сложные вещества, которые состоят из атомов металла и кислотных остатков. Это наиболее многочисленный класс неорганических соединений.
Классификация
СОЛИ бывают: средние,кислые,основные,двойные,смешанные,комплексные
Средние. При диссоциации дают только катионы металла (или NH4+)
Na2SO4 → 2Na+ +SO42-
CaCl2 → Ca2+ + 2Cl-
Кислые. При диссоциации дают катионы металла (NH4+), ионы водорода и анионы кислотного остатка.
NaHCO3 → Na+ + HCO3- → Na+ + H+ + CO32-
Продукты неполного замещения атомов водорода многоосновной кислоты на атомы металла.
Основные. При диссоциации дают катионы металла, анионы гидроксила и кислотного остатка.
Zn(OH)Cl → [Zn(OH)]+ + Cl- → Zn2+ + OH- + Cl-
Продукты неполного замещения групп OH соответствующего основания на кислотные остатки.
Двойные. При диссоциации дают два катиона и один анион.
KAl(SO4)2 → K+ + Al3+ + 2SO42-
Смешанные. Образованы одним катионом и двумя анионами:
CaOCl2 → Ca2+ + Cl- + OCl-
Комплексные. Содержат сложные катионы или анионы.
[Ag(NH3)2]Br → [Ag(NH3)2]+ + Br -
Na[Ag(CN)2] → Na+ + [Ag(CN)2]-
Средние соли.Получение:
Большинство способов получения солей основано на взаимодействии веществ с противоположными свойствами:
1) металла с неметаллом: 2Na + Cl2 = 2NaCl
2) металла с кислотой: Zn + 2HCl = ZnCl2 + H2
3) металла с раствором соли менее активного металла
Fe + CuSO4 = FeSO4 + Cu
4) основного оксида с кислотным оксидом:
MgO + CO2 = MgCO3
5) основного оксида с кислотой
CuO + H2SO4 –t°= CuSO4 + H2O
6) основания с кислотным оксидом
Ba(OH)2 + CO2 = BaCO3 + H2O
7) основания с кислотой:
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
8) соли с кислотой:
MgCO3 + 2HCl = MgCl2 + H2O + CO2
BaCl2 + H2SO4 = BaSO4 + 2HCl
9) раствора основания с раствором соли:
Ba(OH)2 + Na2SO4 = 2NaOH + BaSO4
10) растворов двух солей
3CaCl2 + 2Na3PO4 = Ca3(PO4)2 + 6NaCl
Химические свойства:
1. Термическое разложение.
CaCO3 = CaO + CO2
2Cu(NO3)2 = 2CuO + 4NO2 + O2
NH4Cl = NH3 + HCl
2. Гидролиз.
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
FeCl3 + H2O = Fe(OH)Cl2 + HCl
Na2S + H2O = NaHS +NaOH
3. Обменные реакции с кислотами, основаниями и другими солями.
AgNO3 + HCl = AgCl + HNO3
Fe(NO3)3 + 3NaOH = Fe(OH)3 + 3NaNO3
CaCl2 + Na2SiO3 = CaSiO3 + 2NaCl
4. Окислительно-восстановительные реакции, обусловленные свойствами катиона или аниона.
2KMnO4 + 16HCl = 2MnCl2 + 2KCl + 5Cl2 + 8H2O
Кислые соли. Получение:
1. Взаимодействие кислоты с недостатком основания.
KOH + H2SO4 = KHSO4 + H2O
2. Взаимодействие основания с избытком кислотного оксида
Ca(OH)2 + 2CO2 = Ca(HCO3)2
3. Взаимодействие средней соли с кислотой
Ca3(PO4)2 + 4H3PO4 = 3Ca(H2PO4)2
Химические свойства:
1. Термическое разложение с образованием средней соли
Ca(HCO3)2 = CaCO3 + CO2 + H2O
2. Взаимодействие со щёлочью. Получение средней соли.
Ba(HCO3)2 + Ba(OH)2 = 2BaCO3 + 2H2O
Основные соли.Получение:
1. Гидролиз солей, образованных слабым основанием и сильной кислотой
ZnCl2 + H2O = [Zn(OH)]Cl + HCl
2. Добавление (по каплям) небольших количеств щелочей к растворам средних солей металлов
AlCl3 + 2NaOH = [Al(OH)2]Cl + 2NaCl
3. Взаимодействие солей слабых кислот со средними солями
2MgCl2 + 2Na2CO3 + H2O = [Mg(OH)]2CO3 + CO2 + 4NaCl
Химические свойства:
1. Термическое разложение.
[Cu(OH)]2CO3(малахит) = 2CuO + CO2 + H2O
2. Взаимодействие с кислотой: образование средней соли.
Sn(OH)Cl + HCl = SnCl2 + H2O
Понятие о механизме химических реакций. Простые и сложные реакции, применение закона действия масс к простым и сложным реакциям. Кинетический порядок и молекулярность реакций. Цепные реакции: зарождение, развитие, и обрыв цепи (на примере неразветвленной цепной реакции водорода и хлора)
Понятие о механизме химической реакции
Механизм реакции - детальное ее описание с учетом всех промежуточных стадий и промежуточных веществ, природы взаимодействия реагирующих частиц, характера разрыва связей, изменения энергии химической системы на всем пути ее перехода из исходного в конечное состояние. Цель изучения механизма реакции - возможность управлять ходом реакции, ее направлением и эффективностью.
Реакции, протекающие в одну стадию, называют простыми (элементарными) реакциями, а реакции, включающие несколько стадий - сложными. Многие органические реакции являются сложными и идут в несколько элементарных стадий (последовательных или параллельных). Общая скорость сложной химической реакции определяется скоростью ее наиболее медленной (лимитирующей) стадии.
В случае сложных реакций на некоторых стадиях образуются нестабильные промежуточные частицы - органические ионы или свободные радикалы. Их относительная устойчивость и, следовательно, вероятность образования растут с увеличением возможности делокализации (рассредоточения) заряда в ионе или неспаренного электрона в радикале.
Зако́нде́йствующих масс: соотношение между массами реагирующих веществ в химических реакциях при равновесии, а также зависимость скорости химической реакции от концентрации исходных веществ.
Закон действующих масс в кинетической форме (основное уравнение кинетики) гласит, что скорость элементарной химической реакции пропорциональна произведению концентраций реагентов в степенях, равных стехиометрическим коэффициентам в уравнении реакции. Для элементарной химической реакции:
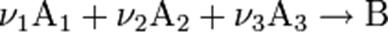
закон действующих масс может быть записан в виде кинетического уравнения вида:
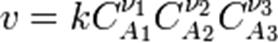
где 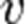 — скорость химической реакции,
— скорость химической реакции, 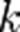 — константа скорости реакции.
— константа скорости реакции.
Для сложных реакций в общем виде это соотношение не выполняется. Тем не менее, многие сложные реакции условно можно рассматривать как ряд последовательных элементарных стадий с неустойчивыми промежуточными продуктами, формально эквивалентный переходу из начального состояния в конечное в. Такие реакции называют формально простыми. Для формально простых реакций кинетическое уравнение может быть получено в виде:
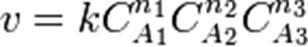
(для трех исходных веществ, аналогично приведённому выше уравнению). Здесь 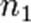 ,
, 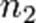 ,
, 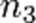 — порядок реакции по веществам
— порядок реакции по веществам 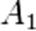 ,
, 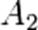 ,
, 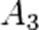 соответственно, а сумма
соответственно, а сумма 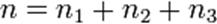 — общий (или суммарный) порядок реакции.
— общий (или суммарный) порядок реакции. 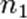 ,
, 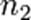 ,
, 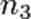 могут быть не равны стехиометрическим коэффициентам и не обязательно целочисленные. при определённых условиях может быть равно и нулю.
могут быть не равны стехиометрическим коэффициентам и не обязательно целочисленные. при определённых условиях может быть равно и нулю.
Химическая кинетика или кинетика химических реакций — раздел физической химии, изучающий закономерности протекания химических реакций во времени, зависимости этих закономерностей от внешних условий, а также механизмы химических превращений.
Реакция нулевого порядка
Кинетическое уравнение имеет следующий вид:
V0 = k0
Скорость реакции нулевого порядка постоянна во времени и не зависит от концентраций реагирующих веществ. Нулевой порядок характерен, например, для гетерогенных реакций в том случае, если скорость диффузии реагентов к поверхности раздела фаз меньше скорости их химического превращения.
Реакция первого порядка
Кинетическое уравнение реакции первого порядка:
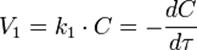
Кинетическое уравнение реакции первого порядка:
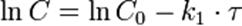
Приведение уравнения к линейному виду даёт уравнение:
Константа скорости реакции вычисляется как тангенс угла наклона прямой к оси времени:
k1 = − tgα
Период полупревращения:
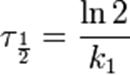
Реакция второго порядка
Для реакций второго порядка кинетическое уравнение имеет следующий вид:
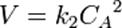 или
или 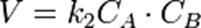
В первом случае скорость реакции определяется уравнением
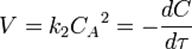
Линейная форма уравнения:
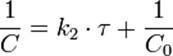
Константа скорости реакции равна тангенсу угла наклона прямой к оси времени:
k2 = − tgα
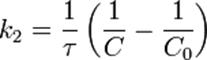
Во втором случае выражение для константы скорости реакции будет выглядеть так:
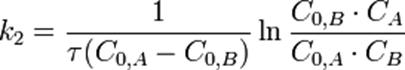
Период полупревращения (для случая равных начальных концентраций!):
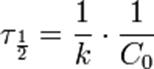
Молекулярность реакции
Молекулярность элементарной реакции — число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия.
Мономолекулярные реакции — реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д.):
H2S → H2 + S
Бимолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных):
СН3Вr + КОН → СН3ОН + КВr
Тримолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении трех частиц:
О2 + NО + NО → 2NО2
Реакции с молекулярностью более трёх неизвестны.
Для элементарных реакций, проводимых при близких концентрациях исходных веществ, величины молекулярности и порядка реакции совпадают. Чётко определенной взаимосвязи между понятиями молекулярности и порядка реакции нет, так как порядок реакции характеризует кинетическое уравнение реакции, а молекулярность — механизм реакции.
Простые вещества. Молекулярное и немолекулярное строение простых веществ. Металлические и неметаллические свойства в зависимости от положения элемента в периодической системе, граница между металлами и неметаллами.
Простые вещества — вещества, состоящие исключительно из атомов одного химического элемента (из гомоядерных молекул), в отличие от сложных веществ. Являются формой существования химических элементов в свободном виде; или, иначе говоря, элементы, не связанные химически ни с каким другим элементом, образуют простые вещества. Известно свыше 400 разновидностей простых веществ.
Молекулярные и немолекулярные вещества — один из признаков химических веществ относительно их строения.
Молекулярные вещества — это вещества, мельчайшими структурными частицами которых являются молекулы
Молекулы — наименьшая частица молекулярного вещества, способная существовать самостоятельно и сохраняющая его химические свойства. Молекулярные вещества имеют низкие температуры плавления и кипения и находятся в стандартных условиях в твердом, жидком или газообразном состоянии.
Немолекулярные вещества — это вещества, мельчайшими структурными частицами которых являются атомы или ионы.
Ион — это атом или группа атомов, обладающих положительным или отрицательным зарядом.
Немолекулярные вещества находятся в стандартных условиях в твердом агрегатном состоянии и имеют высокие температуры плавления и кипения.
Металлические и неметаллические свойства в зависимости от положения элемента в периодической системе, граница между металлами и неметаллами.
Металлы ― это элементы, атомы которых отдают свои внешние электроны.
Неметаллы ― это элементы, атомы которых стремятся принять на внешний энергетический уровень электроны, недостающие до восьми.
1. При перемещении СПРАВА НАЛЕВО вдоль ПЕРИОДА МЕТАЛЛИЧЕСКИЕ свойства р-элементов УСИЛИВАЮТСЯ. В обратном направлении - возрастают неметаллические. Это объясняется тем, что правее находятся элементы, электронные оболочки которых ближе к октету. Элементы в правой части периода менее склонны отдавать свои электроны для образования металлической связи и вообще в химических реакциях. Например, углерод - более выраженный неметалл, чем его сосед по периоду бор, а азот обладает еще более яркими неметаллическими свойствами, чем углерод. Слева направо в периоде также увеличивается и заряд ядра. Следовательно, увеличивается притяжение к ядру валентных электронов и затрудняется их отдача. Наоборот, s-элементы в левой части таблицы имеют мало электронов на внешней оболочке и меньший заряд ядра, что способствует образованию именно металлической связи. За понятным исключением водорода и гелия (их оболочки близки к завершению или завершены!), все s-элементы являются металлами; p-элементы могут быть как металлами, так и неметаллами, в зависимости от того - в левой или правой части таблицы они находятся. У d- и f-элементов, как мы знаем, есть "резервные" электроны из "предпоследних" оболочек, которые усложняют простую картину, характерную для s- и p-элементов. В целом d- и f-элементы гораздо охотнее проявляют металлические свойства. Подавляющее число элементов является металлами и только 22 элемента относят к неметаллам: H, B, C, Si, N, P, As, O, S, Se, Te, а также все галогены и инертные газы.
Некоторые элементы в связи с тем, что они могут проявлять лишь слабые металлические свойства, относят к полуметаллам. Что такое полуметаллы? Если выбрать из Периодической таблицы p-элементы и записать их в отдельный "блок" (это сделано в “длинной” форме таблицы), то обнаружится закономерность. Левая нижняя часть блока содержит типичные металлы, правая верхняя - типичные неметаллы. Элементы, занимающие места на границе между металлами и неметаллами, называются полуметаллами.
Полуметаллы имеют ковалентную кристаллическую решетку при наличии металлической проводимости (электропроводности). Валентных электронов у них либо недостаточно для образования полноценной "октетной" ковалентной связи (как в боре), либо они не удерживаются достаточно прочно (как в тeллуре или полонии) из-за больших размеров атома. Поэтому связь в ковалентных кристаллах этих элементов имеет частично металлический характер. Некоторые полуметаллы (кремний, германий) являются полупроводниками. Полупроводниковые свойства этих элементов объясняются многими сложными причинами, но одна из них - существенно меньшая (хотя и не нулевая) электропроводность, объясняемая слабой металлической связью. Роль полупроводников в электронной технике чрезвычайно важна.
2. При перемещении СВЕРХУ ВНИЗ вдоль групп УСИЛИВАЮТСЯ МЕТАЛЛИЧЕСКИЕ свойства элементов. Это связано с тем, что ниже в группах расположены элементы, имеющие уже довольно много заполненных электронных оболочек. Их внешние оболочки находятся дальше от ядра. Они отделены от ядра более толстой "шубой" из нижних электронных оболочек и электроны внешних уровней удерживаются слабее. Граница между металлами и неметаллами в периодической таблице (в ее длинном варианте) проводится по диагонали от В до At.
Водородные соединения. Зависимость строения и свойств водородных соединений от положения элемента в периодической системе. Особенности строения и химических свойств солеподобных гидридов s- элементов. Строение молекул и химические свойства ковалентных гидридов р- элементов.
С металлами водород образует (за некоторорым исключение) летучие соединения, которые являются твердыми веществами немолекулярного строенияю поэтому их температуры плавления сравнительно высоки. Эти вещества подвергаются полному гидролизу:
NaH+H2O=NaOH+H2
NaH=Na++H-
H-+H++OH=H2+OH-
С неметаллами водород образует летучие соединения молекулярного строения. В обычных условиях это газы или летучие жидкости.
Проследим как изменяются свойства летучих водородных соединений неметаллов в периодах слева направо. Так, например, рассмотрим водородные соединений элементов 2-го периода – азота и фтора. Аммиак NH3 обладает основными свойствами, а фтороводород кислотными. Такими же свойствами обладают водородные соединения 3-го периода – фосфин PH3 и хлороводород.
В периодах слева направо кислотные свойства летучих водородных соединений неметаллов в водных растворах усиливаются.
С очень активными металалми водород взаимодействует непосредственно как окислитель, превращаясь в анион, называемый гидрид-анионом. Эти кристаллические вещества относятся к классу солей и при действии воды полностью разлагаются с выделением водорода и образованием щелочи.
Практически все элементы образуют с водородом соединения, которые можно разделить на 3 основные группы: ковалентные, ионные и металлические.
Атомы всех элементов с IVA по VIIA группу устанавливают с атомами водорода ковалентные связи, что приводит к образованию отдельных молекул, и поэтому соединения водорода с элементами этих групп являются летучими веществами с низкими температурами кипения. Атомы металлов IA и IIA групп (за исключением бериллия и магния), являясь сильными восстановителями, устанавливают ионные связи с атомами водорода, восстанавливая их в ионы H-, в результате чего образуются ионные кристаллы, и внешне и по структуре сходные с солями. Такие солеобразные соединения водорода называются гидридами.
Наиболее обширную группу соединений с водородом образуют d-элементы, т.е. элементы всех B-групп. Эти соединения называются металлическими гидридами. По внешнему виду и по структуре они мало отличаются от порошков соответствующих металлов, обладают электрической проводимостью и теплопроводностью. Гибриды d-металлов имеют переменный состав и этим напоминают сплавы.
Выводы:
1. В периодах слева направо у ионов элементов положительный заряд увеличивается. В связи с этим кислотные свойства летучих водородных соединений элементов в водных растворах усиливаются.
2. В группах сверху вниз отрицаительно заряженные анионы все слабее притягивают положительно заряженные ионы водорода. В связи с этим облегчается процесс отщепления ионов водорода и кислотные свойства водородных соединений увеличиваются.
3. Водородные соединения неметаллов, обладающие в водных растворах кислотными свойствами реагируют со щелочами. Водородные же соединения, обладающие в водных растворах основными свойствами реагируют с кислотами.
4. Окислительная активность водородных соединений неметаллов в группах сверху вниз сильно увеличивается. Например, окислить фтор из водородного соединения HF химическим путем нельзя, окислить же хлор из водородного соединения HCl можно различными окислителями. Это объясняется тем, что в группах сверху вниз резко возрастают атомные радиусы, в связи с чем отдача электронов облегчается.
