Катализ. Гомогенный и гетерогенный катализ.
Изменение скорости реакции под действием некоторых веществ (катализаторов) - катализ.
Различают положительный катализ (просто катализ) и антикатализ. При катализе скорость реакции увеличивается, при антикатализе - уменьшается.
Вещества, увеличивающие скорость реакции - катализаторы, уменьшающие - ингибиторы.
Как правило катализатор при реакции не расходуется, ингибитор расходуется.
Существует также и автокатализ - в роли катализатора вытсупают продукты реакции.
Пример: 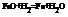
Катализаторы не оказывают влияния на величину 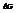 (изменение свободной энергии системы) реакции, следовательно и на константу равновесия. Катализатор лишь ускоряет наступление равновесия реакции, но не смещает его.
(изменение свободной энергии системы) реакции, следовательно и на константу равновесия. Катализатор лишь ускоряет наступление равновесия реакции, но не смещает его.
Для катализаторов присуща определенная избирательность.
_______________________________________
Различают гомогенный и гетерогенный катализ. В первом случае реагирующие вещества и катализатор составляют одну фазу.
Пример: 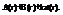
Скорость реакции прямо пропорциональна количеству катализатора.
Механизм можно объяснить образованием промежуточных нестойких соединений. Реакции идут с меньшей энергией активации => быстрее.
Пример: 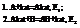
Основная причина ускоряющего действия – уменьшение энергии активации.
Во втором случае – разные фазы.
Пример: 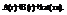
Имеет значение не количество катализатора, а состояние его поверхности.
Катализатор чаще всего находится в твердой фазе.
Твердые катализаторы – оксиды, сульфиды, металлы и соли.
Иногда достаточно простого контакта для огромного увеличения скорости.
Пример. 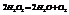 при добавлении
при добавлении 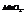
Твердые катализаторы могут терять свою активность под действием каталитических «ядов» - соединений мышьяка, фосфора, цианидов, сероводорода, ацетилена, кислорода.
Поскольку малые количества ядов способны отравлять большие массы катализатора. Это говорит о том, что работает не весь катализатор, а лишь его активные центры.
Согласно теории мультиплетов, существуют определенные закономерности, связывающие расстояния между атомами и расстояния между активными центрами катализатора.
Мультиплет – активный центр на поверхности катализатора, состоящий из нескольких атомов или ионов, имеющий правильную конфигурацию, зависящую от строения всей кристаллической решетки катализатора.
Для протекания определенной реакции молекула должна расположиться особым образом относительно двух активных центров.
Отрицательный катализ вызывается ингибиторами. Они могут расходоваться при протекании процесса. Их действие заключается в том, что они связывают положительные катализаторы либо мешают положительному катализу.
С помощью ингибиторов защищают металл от коррозии в жидких средах, тормозят окислительные процессы в маслах и топливе.
Примерно 80% всех производственных процессов основано на катализе: производство аммиака, серной кислоты, азотной кислоты, крекинг (переработка нефтепродуктов), моторное топливо (из каменного угля).

