Тема 12. Электрохимические процессы. Электролиз
12-1. Электролизом называется окислительно-восстановительная реакция,
а) при осуществлении которой возникает электрический ток
б) протекающая в растворе при пропускании электрического тока
в) протекающая на электродах при пропускании электрического тока
г) при осуществлении которой в растворе образуются катионы и анионы
12-2. Катод при электролизе
| а) заряжен положительно | в) не имеет заряда |
| б) заряжен отрицательно | г) изменяет знак заряда во время электролиза |
12-3. Анод при электролизе
| а) заряжен положительно | в) не имеет заряда |
| б) заряжен отрицательно | г) изменяет знак заряда во время электролиза |
12-4. Процесс ... протекает на катоде при электролизе.
| а) восстановления | в) нейтрализации |
| б) окисления | г) перезарядки |
12-5. Процесс ... протекает на аноде при электролизе.
| а) восстановления | в) нейтрализации |
| б) окисления | г) перезарядки |
12-6. Масса вещества, выделяющегося на электроде при электролизе, находится по формуле:
а) 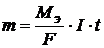 | в) 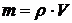 |
б) 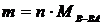 | г) 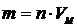 |
12-7. Наиболее вероятный процесс на катоде при электролизе
а) окисление частиц с наименьшим потенциалом
б) восстановление частиц с наименьшим потенциалом
в) окисление частиц с наибольшим потенциалом
г) восстановление частиц с наибольшим потенциалом
12-8. Наиболее вероятный процесс на аноде при электролизе
а) восстановление частиц с наибольшим потенциалом
б) восстановление частиц с наименьшим потенциалом
в) окисление частиц с наибольшим потенциалом
г) окисление частиц с наименьшим потенциалом
12-9. Только молекулы воды восстанавливаются на катоде при электролизе водных растворов, если
а)  | в) 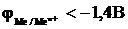 |
б) 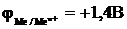 | г) 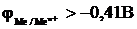 |
12-10. Ионы металла восстанавливаются на катоде при электролизе водных растворов, если
а) 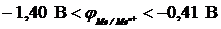 | в) 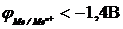 |
б) 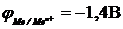 | г) 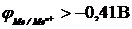 |
12-11. Инертный анод при электролизе
| а) цинковый | в) медный |
| б) платиновый | г) хромовый |
12-12. Инертный анод при электролизе
| а) графитовый | в) серебряный |
| б) натриевый | г) никелевый |
12-13. Активный анод при электролизе
| а) графитовый | в) серебряный |
| б) платиновый | г) полиэтиленовый |
12-14. Процесс окисления ___ протекает на графитовом аноде при электролизе водных растворов кислородсодержащих солей.
| а) материала анода | в) кислородсодержащих анионов |
| б) бескислородных анионов | г) молекул воды |
12-15. Процесс окисления ___ протекает на графитовом аноде при электролизе водных растворов бескислородных солей.
| а) материала анода | в) кислородсодержащих анионов |
| б) бескислородных анионов | г) молекул воды |
12-16. Последовательность восстановления катионов металла на катоде:
а) Zn2+ ( 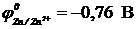 ) ) | в) Cu2+ ( 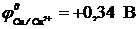 ) ) |
б) Hg2+ ( 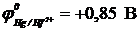 ) ) | г) Au+ ( 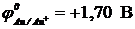 ) ) |
12-17. Процесс ___ протекает на медном аноде при электролизе раствора CuCl2.
| а) Cu2+ + 2e– = Cu0 | в) Cu0 – 2e– = Cu2+ |
| б) 2H+ + 2e– = H20 | г) Cl2 + 2e– = 2Cl– |
12-18. Восстанавливаться на катоде при электролизе растворов будут ионы
| а) Cu2+ | б) Bi3+ | в) Cl– | г) OH– | д) Ag+ |
12-19. Процесс ___ будет происходить на катоде при электролизе водного раствора Na2SO4 ( 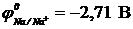 ).
).
| а) Na+ + e – = Na0 | в) 2H2O – 4e– = O20+4H+ |
| б) 2H2O + 2e– = H20 + 2OH– | г) 2SO42– – 2e– = S2O82 |
12-20. Последовательность восстановления катионов металла на катоде
а) Cu2+ ( 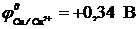 ) ) | в) Pb2+ ( 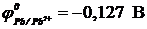 ) ) |
б) Ag+ ( 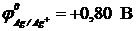 ) ) | г) Ni2+ ( 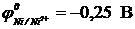 ) ) |
12-21. Процесс ___ протекает на катоде при электролизе раствора NiCl2 ( 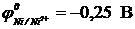 ).
).
| а) Ni2+ + 2e– = Ni0 | в) 2H2O – 4e– = O20 + 4H+ |
| б) 2H2O + 2e– = H20 + 2OH– | г) Ni2+ + 2e– = Ni0 и 2H2O + 2e– = H20 + 2OH– |
12-22. Процесс ___ будет протекать на катоде при электролизе раствора ZnSO4 ( 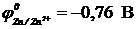 ).
).
| а) Zn2+ + 2e– = Zn0 | в) 2H2O + 2e– = H20 + 2OH– |
| б) 2H2O – 4e– = O20 + 4H+ | г) Zn2+ + 2e– = Zn0 и 2H2O + 2e– = H20 + 2OH– |
12-23. Кислород выделяется на аноде при ___ воды.
| а) окислении | б) восстановлении | в) замещении |
12-24. Продуктами электролиза водного раствора хлорида цинка ( 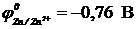 ) с инертными электродами будут
) с инертными электродами будут
| а) цинк и хлор | в) цинк, хлор, водород и гидроксид цинка |
| б) цинк, хлор и кислород | г) гидроксид цинка и хлор |
12-25. Ионы OH– образуются у электрода при электролизе водного раствора соли. Этот электрод называется
| а) катод | в) анод |
| б) металл | г) щелочной электрод |
12-26. Продуктами электролиза с графитовыми электродами водного раствора сульфата меди ( 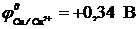 ) будут
) будут
| а) медь | г) медь, кислород и серная кислота |
| б) медь и водород | д) медь, водород, кислород и серная кислота |
| в) медь, водород и кислород |
12-27. Ионы Н+ образуются у электрода при электролизе водного раствора соли. Этот электрод –
| а) катод | в) анод |
| б) металл | г) щелочной электрод |
12-28. Практическая и теоретическая массы вещества, выделившегося на катоде, составляют 48 и 80 г соответственно. Выход по току (в %) равен ___ .
_*_ _*_ _*_
12-29. Продуктами, выделяющимися на электродах при электролизе водного раствора хлорида калия, являются
| а) H2 и Cl2 | б) K и Cl2 | в) K и O2 | г) H2 и O2 |
12-30. Уравнение процесса, протекающего на аноде при электролизе водного раствора CaCl2 с графитовыми электродами, имеет вид
| а) Ca+2 + 2e = Ca0 | в) 2Cl– – 2e = Cl2 |
| б) 4OH– –4e = O2 + 2H2O | г) 2H2O – 4e = O2 + 4H+ |
12-31. Уравнение процесса, протекающего на аноде при электролизе водного раствора бромида калия с инертными электродами, имеет вид
| а) 2Br– – 2e = Br2 | в) 2H2O + 2e = H2 + 2OH– |
| б) 4OH– – 4e = O2 + 4H+ | г) 2H2O –4e = O2 + 4H+ |
12-32. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора сульфата меди, являются
| а) Cu и SO2 | б) Cu и O2 | в) H2 и O2 | г) Cu и H2 |
12-33. Уравнение процесса, протекающего на катоде при электролизе водного раствора нитрата серебра с инертными электродами, имеет вид
| а) 2H2O + 2e = H2 + 2OH– | в) 2H+ + 2e = H2 |
| б) Ag+ + e = Ag | г) 2NO3– –2e = 2NO2 + O2 |
12-34. Уравнение процесса, протекающего на катоде при электролизе водного раствора бромида меди, имеет вид
| а) Cu2+ + 2e =Cu0 | в) 2H+ + 2e = H2 |
| б) 2H2O + 2e = H2 + 2OH– | г) 2Br– – 2e = Br2 |
12-35. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора бромида меди, являются
| а) Cu(OH)2 и Br2 | в) Cu и O2 |
| б) H2 и O2 | г) Cu и Br2 |
12-36.Уравнение процесса, протекающего на инертном аноде при электролизе водного раствора хлорида натрия, имеет вид
| а) 2Cl– – 2e = Cl2 | в) O2 + 2H2O + 4e = 4OH– |
| б) 2H2O – 4e = O2 + 4H+ | г) 4OH– – 4e = 4OH |
12-37. Уравнение процесса, протекающего на аноде при электролизе водного раствора йодида калия, имеет вид
| а) 2H2O – 4e = O2 + 4H+ | в) O2 + 2H2O + 4e = 4OH– |
| б) 4OH– – 4e = 4OH | г) 2I– – 2e = I2 |
12-38. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора серной кислоты, являются
| а) H2 и SO2 | в) O2 и SO2 |
| б) H2 и O2 | г) H2 и S |
12-39. Уравнение процесса, протекающего на катоде при электролизе водного раствора йодида калия, имеет вид
| а) K+ + e = K0 | в) O2 + 2H2O + 4e = 4OH– |
| б) 2H2O + 2e = H2 + 2OH– | г) 2H2O – 4e = O2 + 4H+ |
12-40. Продуктами электролиза на инертных электродах при электролизе водного раствора нитрата серебра, являются
| а) Ag и O2 | б) H2 и O2 | в) Ag и NO2 | г) H2 и NO2 |
12-41. Металлом, который можно получить электролизом водного раствора его соли, является
| а) K | б) Na | в) Cu | г) Al |
12-42. Массу вещества, выделившегося или разложившегося в результате электролиза, можно вычислить, используя закон
| а) Вант-Гоффа | в) Фарадея |
| б) Гесса | г) Аррениуса |
12-43. Металлом, который нельзя получить электролизом водного раствора его соли, является
| а) Ag | б) Ni | в) Cu | г) Na |
12-44. Продуктами, выделяющимися на инертных электродах при электролизе водного раствора сульфата натрия, являются
| а) H2 и S | в) H2 и O2 |
| б) Na и O2 | г) Na и SO2 |
