Электролиз расплавов и растворов электролитов. Электролиз с инертным и растворимым анодом.
Электролиз - это ещё один способ получения чистых металлов и неметаллов. Кроме того, электролиз можно провести и в домашних условиях. Нужен источник тока, два электрода (какие электроды бывают и какой в каком случае брать - расссказано дальше) и, конечно, электролит. Электролит - это раствор, который проводит электрический ток.
Различают электролиз растворов и электролиз расплавов. Оба эти процесса существенно отливчаются друг от друга. Отличие - в наличии растворителя. При электрролизе растворов кроме ионов самого вещества в процессе учавствуют ионы растворителя. При электролизе расплавов - только ионы самого вещества.
Для того, чтобы получить нужный продукт (газ, металл или неметалл), нужно правильно выбрать электрод и раствор электролита.
Электродами могут служить любые материалы, проводящие электрический ток. В основном применяют металлы и сплавы, из неметаллов электродами могут служить, например, графитовые стержни (или углерод). Реже в качестве электрода используют жидкости.
Электрод, заряженный положительно - анод. Электрод, заряженный отрицательно - катод. При электролизе происходт окисление анода (он растворяется) и восстановление катода. Именно поэтому анод следует брать таким, чтобы его растворение не повлияло на химический процесс, протекающий в растворе или расплаве. Такой анод называют инертным электродом. В качестве инертного анода можно взять графит (углерод) или платину.
В качестве катода можно взять металлическую пластину (она не будет растворяться). Подойдёт медь, латунь, углерод (или графит), цинк, железо, алюминий, нержавейка.
При электролизе расплавов в процессе учавствуют только ионы вещества, которое подвергается электролизу. Например, если подвергнуть электролизу расплав поваренной соли (NaCl), то на аноде будет выделяться тот же газ - хлор, а вот на катоде вместо водорода будет восстанавливаться чистый металл - натрий (Na). Именно таком способом в промышленности получают металлический натрий и другие щелочные и щелочноземельные металлы.Таким же образом получают другие щелочные металлы (калий (K), литий (Li), кальций (Ca)), проводя ток через расплавы их солей.
Законы электролиза. Применение электролиза.
Первый закон Фарадея
Основная статья: Законы электролиза Фарадея
В 1832 годуФарадей установил, что масса m вещества, выделившегося на электроде, прямо пропорциональна электрическому заряду q, прошедшему через электролит:
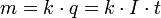
если через электролит пропускается в течение времени t постоянный ток с силой тока I. Коэффициент пропорциональности 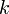 называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
называется электрохимическим эквивалентом вещества. Он численно равен массе вещества, выделившегося при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
Вывод закона Фарадея
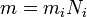 (1)
(1)
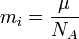 (2)
(2)
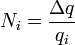 (3)
(3)
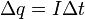 (4)
(4)
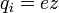 , где z — валентностьатома (иона) вещества, e — заряд электрона (5)
, где z — валентностьатома (иона) вещества, e — заряд электрона (5)
Подставляя (2)-(5) в (1), получим
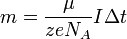
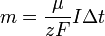 где
где 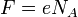 — постоянная Фарадея.
— постоянная Фарадея.
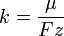
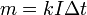
Второй закон Фарадея
Электрохимические эквиваленты различных веществ относятся, как их химические эквиваленты.
Химическим эквивалентом иона называется отношение молярной массы A иона к его валентности z. Поэтому электрохимический эквивалент
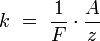 где
где 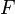 — постоянная Фарадея.
— постоянная Фарадея.
Второй закон Фарадея записывается в следующем виде:
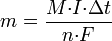
где 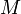 — молярная масса данного вещества, образовавшегося (однако не обязательно выделившегося — оно могло и вступить в какую-либо реакцию сразу после образования) в результате электролиза, г/моль;
— молярная масса данного вещества, образовавшегося (однако не обязательно выделившегося — оно могло и вступить в какую-либо реакцию сразу после образования) в результате электролиза, г/моль; 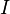 — сила тока, пропущенного через вещество или смесь веществ (раствор, расплав), А;
— сила тока, пропущенного через вещество или смесь веществ (раствор, расплав), А; 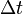 — время, в течение которого проводился электролиз, с;
— время, в течение которого проводился электролиз, с; 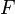 — постоянная Фарадея, Кл·моль−1;
— постоянная Фарадея, Кл·моль−1; 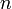 — число участвующих в процессе электронов, которое при достаточно больших значениях силы тока равно абсолютной величине заряда иона (и его противоиона), принявшего непосредственное участие в электролизе (окисленного или восстановленного). Однако это не всегда так; например, при электролизе раствора соли меди(II) может образовываться не только свободная медь, но и ионы меди(I) (при небольшой силе тока).
— число участвующих в процессе электронов, которое при достаточно больших значениях силы тока равно абсолютной величине заряда иона (и его противоиона), принявшего непосредственное участие в электролизе (окисленного или восстановленного). Однако это не всегда так; например, при электролизе раствора соли меди(II) может образовываться не только свободная медь, но и ионы меди(I) (при небольшой силе тока).
Электролиз находит весьма широкое применение. Для защиты металлических изделий от коррозии на их поверхность наносится тончайший слой другого металла — хрома, серебра, золота, меди, никеля и т.д. Иногда применяют многослойное покрытие. Например, внешние детали автомобиля сначала покрывают тонким слоем меди, на медь наносят тончайший слой никеля, а на него — слой хрома.
Нанесенные на металлы электролизом покрытия получаются ровными по толщине, прочными, служат долго, и, кроме того, таким способом можно покрывать изделия любой формы. Эту отрасль прикладной электрохимии называют гальваностегией. Кроме защиты от коррозии, гальванические покрытия иногда придают красивый декоративный вид предметам.
Другая отрасль электрохимии, близкая по принципу к гальваностегии, называется гальванопластикой. Это получение точных металлических копий с различных предметов. Предмет, с которого хотят изготовить копию, покрывают воском, дают воску застыть и получают восковую матрицу, на которой все углубления копируемого предмета будут выпуклостями. Внутреннюю поверхность матрицы покрывают тонким слоем графита, проводящим электрический ток. Этот графитовый катод опускают в ванную с раствором сульфата меди; анодом служит медь. При электролизе медный анод растворяется, а на катоде осаждается | медь. Таким образом получается точная копия предмета. С помощью гальванопластики изготовляют клише для печати, грампластинки, металлизируют различные предметы. Гальванотехника разработана русским ученым Б. С. Якоби (1838).
Электролиз используется для получения многих металлов — щелочных, щелочноземельных, алюминия, лантаноидов и др. также для очистки некоторых металлов от примесей
