Общие представления о гидролизе солей
Гидролиз – это обменная реакция взаимодействия вещества с водой. В переводе на русский язык слово «гидролиз» означает «разложение водой».
Гидролизу подвергаются вещества различных классов. В качестве примера можно привести гидролиз хлорида фосфора (PCl3 + 3 HOH ® H3PO3 + 3 HCl), гидролиз различных органических веществ: галогенпроизводных углеводородов, сложных эфиров, белков, углеводов. Важным частным случаем гидролиза является гидролиз солей.
При растворении в воде любой соли происходит диссоциация этой соли на катионы и анионы. Если соль образована катионом слабого основания и анионом сильной кислоты (например, хлорид аммония NH4Cl), то катионы NH4+ слабого основания будут отщеплять ионы OH– от молекул воды и образовывать слабодиссоциирующий электролит – гидроксид аммония. В результате этого взаимодействия в растворе установится равновесие, в котором ионы водорода и аммония конкурируют за гидроксид-ионы:
NH4Cl + HOH ⇆ NH4OH + HCl; NH4+ + HOH ⇆ NH4OH + H+.
Если соль образована катионом сильного основания и анионом слабой кислоты (например, нитрит натрия NaNО2), то анионы слабой кислоты (в данном случае нитрит-ионы) будут частично связываться с ионами H+, отщепляя их от молекул воды, в результате чего образуется слабая азотистая кислота, и в растворе устанавливается равновесие, в котором нитрит- и гидроксид-ионы конкурируют за ионы водорода.
NaNО2 + HOH ⇆ HNО2 + NaOH; NО2– + HOH ⇆ HNО2 + OH–
Таким образом, при гидролизе солей имеет место смещение равновесия диссоциации воды HOH ⇆ H+ + OH– вследствие связывания одного из её ионов (или обоих) ионами растворённой соли с образованием малодиссоциирующего соединения. Как видно из приведённых выше уравнений, гидролиз солей есть реакция обратная реакции нейтрализации.
При растворении в воде соли, образованной катионом сильного основания и анионом сильной кислоты (например, NaCl), равновесие диссоциации воды не смещается, так как ионы этой соли (Na+ и Cl–) не могут образовать с ионами воды (H+ и OH–) малодиссоциирующих продуктов. Такие соли не гидролизуются.
Образующиеся в результате гидролиза солей слабые кислоты и основания обычно являются гораздо более сильными электролитами, чем вода. Поэтому гидролиз большинства солей, гидролизующихся только по катиону или только по аниону, протекает незначительно.
Если соль гидролизуется только по катиону, то реакция среды – кислая (в растворе появляется избыток ионов H+); pH < 7. Если же соль гидролизуется только по аниону, то реакция среды – щелочная (в растворе появляется избыток ионов OH–); pH > 7.
Ещё один тип гидролизующихся солей – соли, образованные катионом слабого основания и анионом слабой кислоты (например, нитрит аммония NH4NO2). При гидролизе такой соли катионы слабого основания NH4+ связываются с ионами OH–, отщепляя их от молекул воды, а анионы слабой кислоты NO2– связываются с ионами H+, в результате чего образуется слабое основание NH4OH и слабая кислота HNO2: NH4+ + NO2– + HOH ⇆ NH4OH + HNO2
NH4NO2 + HOH ⇆ NH4OH + HNO2 .
Очевидно, что если соль гидролизуется и по катиону, и по аниону, то равновесие гидролиза сильнее смещено вправо, чем в тех случаях, когда соль гидролизуется только по одному из её ионов.
Реакция среды в растворе соли, гидролизующейся и по катиону, и по аниону определяется тем, какой из образующихся в результате гидролиза малодиссоциирующих электролитов является более сильным. Например, в случае гидролиза нитрита аммония NH4+ + NO2– + HOH ⇆ NH4OH + HNO2 реакция среды будет кислой (pH < 7), поскольку HNO2 – более сильный электролит, чем NH4OH: KNH4OH = 1,8·10–5 < KHNO2 = 4·10–4. В случае гидролиза ацетата аммония NH4+ + CH3COO– + HOH ⇆ NH4OH + CH3COOH реакция среды будет нейтральной (pH = 7), потому что соль образована одинаковыми по силе кислотой и основанием: KNH4OH = KCH3COOH = 1,8·10–5.
Константа гидролиза
Гидролиз солей в большинстве случаев протекает обратимо. Поэтому для процесса гидролиза, как и любого равновесного процесса можно записать выражение константы равновесия. Константа равновесия в данном случае называется константой гидролиза.
Для соли, гидролизующейся по катиону Me+ + HOH ⇆ MeOH + H+
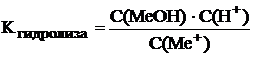 . (8.1)
. (8.1)
Поскольку в разбавленных водных растворах концентрация воды постоянна (см. раздел 7.7 предыдущей лекции), то её не записывают в выражении константы гидролиза. Формулу 8.1 можно преобразовать, выразив концентрацию ионов водорода из уравнения ионного произведения воды C(H+)·C(OH–) = Kw .
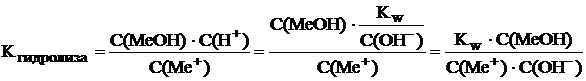
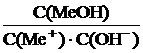 Выражение есть ни что иное, как величина, обратная
Выражение есть ни что иное, как величина, обратная
константе диссоциации слабого основания KMeOH . Таким образом, окончательно получается следующее уравнение для расчёта константы гидролиза соли, гидролизующейся по катиону:
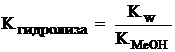
. (8.2)
Это уравнение показывает, что константа гидролиза соли, гидролизующейся только по катиону тем больше, чем меньше константа диссоциации основания, которым образована соль. Это означает, что соль гидролизуется тем сильнее, чем более слабым основанием, она образована.
Можно также показать, что для соли гидролизующейся только по аниону An– + HOH ⇆ HAn + OH– константа гидролиза
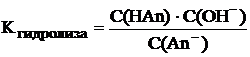
(8.3)
может быть вычислена по следующему уравнению, аналогичному уравнению 8.2:
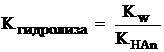
. (8.4)
В формуле 8.4 KHAn – константа диссоциации слабой кислоты, которой образована соль. Последнее уравнение показывает, что Kгидролиза тем больше, чем меньше KHAn, т.е. гидролиз по аниону протекает тем сильнее, чем слабее кислота, которой образована соль.
Ниже приводится вывод формулы константы гидролиза для соли, гидролизующейся одновременно и по катиону, и по аниону.
Me+ + An– + HOH ⇆ MeOH + HAn.
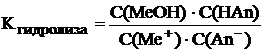 (8.5)
(8.5)
Уравнение 8.5 можно преобразовать, умножая и числитель, и знаменатель на константу ионного произведения воды.
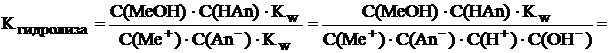
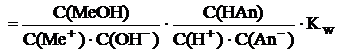
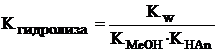 (8.6)
(8.6)
