Молекулярные вещества имеют низкие температуры плавления и кипения и находятся в стандартных условиях в твердом, жидком или газообразном состоянии.
Например: Вода - жидкость, tпл=0°С; tкип=100°С
Вода – самое известное и весьма распространенное вещество на нашей планете: поверхность Земли на 3/4 покрыта водой, человек на 65 % состоит из воды, без воды невозможна жизнь, так как в водном растворе протекают все клеточные процессы организма. Вода – молекулярное вещество. Это одно из немногих веществ, которое в природных условиях встречается в твердом, жидком и газообразном состояниях, и единственное вещество, для которого в каждом из этих состояний есть свое название.
Особенностями строения воды вызваны ее необычные свойства. Например, при замерзании вода увеличивается в объеме, поэтому лед плавает в своем расплаве – жидкой воде, а наибольшая плотность воды наблюдается при 4 oС, поэтому зимой большие водоемы до дна не промерзают. На свойствах воды основана и сама шкала температур Цельсия (0 o – температура замерзания, 100 o – температура кипения). С причинами этих явлений и с химическими свойствами воды вы познакомитесь позже.
Немолекулярные вещества - это вещества, мельчайшими структурными частицами которых являются атомы или ионы.
Ион - это атом или группа атомов, обладающих положительным или отрицательным зарядом.
Например: Na+, Cl-.
Немолекулярные вещества находятся в стандартных условиях в твердом агрегатном состоянии и имеют высокие температуры плавления и кипения.
Например: Поваренная соль - твердое вещество, tпл=801°С; tкип=1465°С; Железо
Железо – серебристо-белый, блестящий, ковкий металл. Это немолекулярное вещество. Среди металлов железо занимает второе место после алюминия по распространенности в природе и первое место по значению для человечества. вместе с другим металлом – никелем – оно образует ядро нашей планеты. Чистое железо не имеет широкого практического применения. Знаменитая Кутубская колонна, расположенная в окрестностях Дели, высотой около семи метров и весом 6,5 т, имеющая возраст почти 2800 лет (она поставлена в IX в. до н. э.) – один из немногих примеров использования чистого железа (99,72 %); возможно, что именно чистотой материала и объясняется долговечность и коррозионная устойчивость этого сооружения.
В виде чугуна, стали и других сплавов железо используется буквально во всех отраслях техники. Его ценные магнитные свойства используются в генераторах электрического тока и электромоторах. Железо является жизненно необходимым элементом для человека и животных, так как оно входит в состав гемоглобина крови. При его недостатке клетки тканей получают недостаточно кислорода, что ведет к очень тяжелым последствиям.
Слева направо по периодуу элементов происходит ослабление металлических свойств, и усиление неметаллических свойств, основные свойства оксидов ослабевают, а кислотные свойства оксидов возрастают.
По главным подгруппамнеметаллические свойства элементов ослабевают, а металлические усиливаются, поэтому: сверху вниз по главной подгруппе возрастают основанные свойства оксидов, а кислотные ослабевают.
59. Окси́д (о́кисел, о́кись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся почти все соединения химических элементов с кислородом. К исключениям относятся, например, дифторид кислорода OF2.
Основные оксиды
1. Основный оксид + cильная кислота → соль + вода
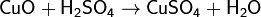
2. Сильноосновный оксид + вода → щелочь
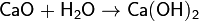
3. Сильноосновный оксид + кислотный оксид → соль
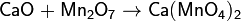
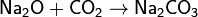
4. Основный оксид + водород → металл + вода
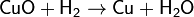
Примечание: металл менее активный, чем алюминий.
[править]Кислотные оксиды
1. Кислотный оксид + вода → кислота
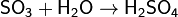
Некоторые оксиды, например SiO2, с водой не вступают в реакцию, поэтому их кислоты получают косвенным путём.
2. Кислотный оксид + основный оксид → соль
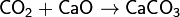
3. Кислотный оксид + основание → соль + вода
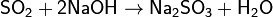
Если кислотный оксид является ангидридом многоосновной кислоты, возможно образование кислых или средних солей:
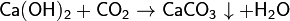
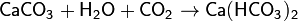
4. Нелетучий оксид + соль1 → соль2 + летучий оксид
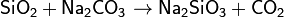
5. Ангидрид кислоты 1 + безводная кислородосодержащая кислота 2 → Ангидрид кислоты 2 + безводная кислородосодержащая кислота 1
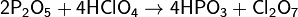
[править]Амфотерные оксиды
При взаимодействии с сильной кислотой или кислотным оксидом проявляют основные свойства:
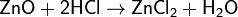
При взаимодействии с сильным основанием или основным оксидом проявляют кислотные свойства:
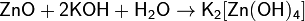 (в водном растворе)
(в водном растворе)
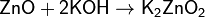 (при сплавлении)
(при сплавлении)
Слева направо по периодуу элементов происходит ослабление металлических свойств, и усиление неметаллических свойств, основные свойства оксидов ослабевают, а кислотные свойства оксидов возрастают.
По главным подгруппамнеметаллические свойства элементов ослабевают, а металлические усиливаются, поэтому: сверху вниз по главной подгруппе возрастают основанные свойства оксидов, а кислотные ослабевают.
Обратите внимание!Если один и тот же элемент образует несколько оксидов с разными степенями окисления, то чем выше степень окисления элемента в оксиде, тем выше его кислотные свойства.
Например: 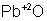 и
и 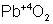 – первый оксид основной, а второй амфотерный.
– первый оксид основной, а второй амфотерный. 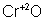
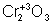 ,
, 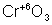 – первый оксид основной, второй – амфотерный, последний – кислотный.
– первый оксид основной, второй – амфотерный, последний – кислотный.
60. Кисло́ты — сложные вещества, в состав которых обычно входят атомы водорода, способные замещаться на атомы металлов, и кислотный остаток. Водные растворы кислот имеют кислый вкус, обладают раздражающим действием, способны менять окраску индикаторов, отличаются рядом общих химич Взаимодействие с основными оксидами с образованием соли и воды:
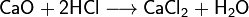
Взаимодействие с амфотерными оксидами с образованием соли и воды:
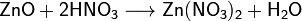
Взаимодействие со щелочами с образованием соли и воды (реакция нейтрализации):
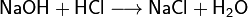
Взаимодействие с нерастворимыми основаниями с образованием соли и воды, если полученная соль растворима:
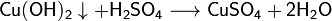
Взаимодействие с солями, если выпадает осадок или выделяется газ:
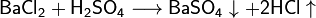
Сильные кислоты вытесняют более слабые из их солей:
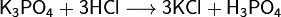
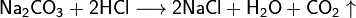
(в данном случае образуется неустойчивая угольная кислота 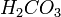 , которая сразу же распадается на воду и углекислый газ)
, которая сразу же распадается на воду и углекислый газ)
Металлы, стоящие в ряду активности до водорода, вытесняют его из раствора кислоты (кроме азотной кислоты 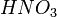 любой концентрации и концентрированной серной кислоты
любой концентрации и концентрированной серной кислоты 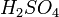 ), если образующаяся соль растворима:
), если образующаяся соль растворима:
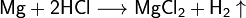
С азотной кислотой и концентрированной серной кислотами реакция идёт иначе:
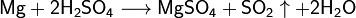
См. статью Взаимодействие кислот с металлами.
Для органических кислот характерна реакция этерификации (взаимодействие со спиртами с образованием сложного эфира и воды):
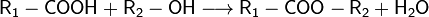
Например,
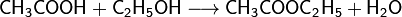
Основания (осно́вные гидрокси́ды) — сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (-OH). В водном растворе диссоциируют с образованием катионов и анионов ОН−. Название основания обычно состоит из двух слов: «гидроксид металла/аммония». Хорошо растворимые в воде основания называются щелочами.
В водных растворах основания диссоциируют, что изменяет ионное равновесие:
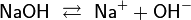
это изменение проявляется в цветах некоторых кислотно-основных индикаторов:
лакмус становится синим,
метилоранж — жёлтым,
фенолфталеин приобретает цвет фуксии.
При взаимодействии с кислотой происходит реакция нейтрализации и образуется соль и вода:
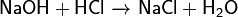
Примечание: реакция не идёт, если и кислота и основание слабые.
При избытке кислоты или основания реакция нейтрализации идёт не до конца и образуются кислые или осно́вные соли, соответственно:
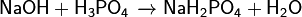
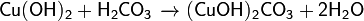
Амфотерные основания могут реагировать с щелочами с образованием гидроксокомплексов:
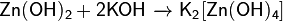
Основания реагируют с кислотными или амфотерными оксидами с образованием солей:
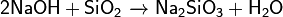
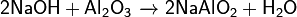
Основания вступают в обменные реакции (реагируют с растворами солей):
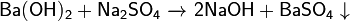
Слабые и нерастворимые основания при нагреве разлагаются на оксид и воду:
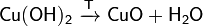
Некоторые основания (Cu(I), Ag, Au(I)) разлагаются уже при комнатной температуре.
Основания щелочных металлов (кроме лития) при нагревании плавятся, расплавы являются электролитами
