Тема 15. Соли и их свойства.
План:
5. Соли как электролиты.
6. Соли средние, кислые и оснóвные.
7. Химически свойства солей в свете теории электролитической диссоциации.
8. Способы получения солей.
Соли как электролиты.
Солями называются электролиты, при диссоциации которых образуются катионы металлов а также катион аммония (NH+4) и анионы кислотных остатков.
2) Соли средние, кислые и оснóвные.
Все соли разделяются на средние, кислые и основные. Средние соли содержат только атомы металла и кислотного остатка. Например, все соли из таблицы 8-6 являются средними солями.
Любую соль можно получить соответствующей реакцией нейтрализации. Например, сульфит натрия образуется в реакции между сернистой кислотой и основанием (едким натром). При этом на 1 моль кислоты требуется взять 2 моля основания:
| H2SO3 | + | 2 NaOH | = | Na2SO3 | + | 2 H2O |
| сульфит натрия (средняя соль) |
Если взять только 1 моль основания – то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль – гидросульфит натрия:
| H2SO3 | + | NaOH | = | NaHSO3 | + | H2O |
| гидросульфит натрия (кислая соль) |
Кислые соли образуются многоосновными кислотами. Одноосновные кислоты кислых солей не образуют.
Кислые соли, помимо ионов металла и кислотного остатка, содержат ионы водорода.
Названия кислых солей содержат приставку "гидро" (от слова hydrogenium – водород). Например:
NaHCO3 – гидрокарбонат натрия,
K2HPO4 – гидрофосфат калия,
KH2PO4 – дигидрофосфат калия.
Основные соли образуются при неполной нейтрализации основания. Названия основных солей образуют с помощью приставки "гидроксо". Ниже приведен пример, показывающий отличие основных солей от обычных (средних):
| Mg(OH)2 | + | 2 HCl | = | MgCl2 | + | 2 H2O | |||
| хлорид магния(средняя соль) | |||||||||
| Mg(OH)2 | + | HCl | = | Mg(OH)Cl | + | H2O | |||
| гидроксохлорид магния(основная соль) | |||||||||
Основные соли, помимо ионов металла и кислотного остатка, содержат гидроксильные группы.
Основные соли образуются только из многокислотных оснований. Одноокислотные основания таких солей образовать не могут.
Химически свойства солей в свете теории электролитической диссоциации.
1-Взаимодействие с металлами, ряд активности металлов
СОЛЬ + МЕТАЛЛ → новая СОЛЬ + Металл↓
Fe + CuSO₄ = FeSO₄ + Cu↓
Mg + FeCl₂ = MgCl₂ + Fe↓
Задание: дописать уравнения реакций
Al + FeSO₄ →
Cu + MgCl₂ →
2 - Взаимодействие с кислотами, ряд активности кислот
соль₁ + кислота₁ → соль₂ + кислота₂
Ряд активности кислот
H₂SO₄ , HNO₃, H₃PO₄, H₂SO₃, H₂CO₃, H₂S, H₂SiO₃
каждая предыдущая кислота вытесняет последующую из раствора ее соли
K₂CO ₃ + 2 HCl = 2KCl + H₂CO₃
Na₂SiO₃ + H₂SO₄ = Na₂SO₄ + H₂SiO₃↓
Задание: дописать уравнения реакций
Na₂S + HNO₃→
AgNO₃ + HCl →
3- Взаимодействие с основаниями
соль₁ +основание₁ = соль₂ +основание₂↓
(р) (щелочь) (н)
CuSO₄ + 2NaOH = Cu(OH)₂↓ + Na₂SO₄
AlCl₃ + 3KOH = 3KCl + Al(OH)₃↓
FeCl₂ + 2NaOH = Fe(OH)₂↓ + 2NaCl
Задание - дописать уравнения реакций
Zn(NO₃)₂ + Ba(OH)₂ →
MgSO₄ + NaOH →
4- Взаимодействие с солями
соль₁ +соль₂= новая соль₁↓+ новая соль₂
BaCl₂ + Na₂SO₄ = BaSO₄↓ + 2NaCl
Cu(NO₃)₂ + K₂S = 2KNO₃ + CuS↓
Задание - дописать уравнения реакций ( слайд 10):
MgCl₂ + Na₂CO₃ →
Ca(NO₃)₂ + K₃PO₄ →
5- Разложение нерастворимых солей при нагревании
соль ↓ → оксид металла + оксид неметалла
BaSiO₃↓ = BaO + SiO₂
CaCO₃↓ = CaO + CO₂
Способы получения солей.
Известно большое число реакций, приводящих к образованию солей. Приведем наиболее важные из них.
1. Взаимодействие кислот с основаниями (реакция нейтрализации):
NаОН + НNO3 = NаNO3 + Н2О
Al(OH)3 + 3НС1 = AlCl3 + 3Н2О
2. Взаимодействие металлов с кислотами:
Fе + 2HCl = FeCl2 + Н2
Zn + Н2SО4 разб.= ZnSO4 + Н2
3. Взаимодействие кислот с основными и амфотерными оксидами:
СuO + Н2SO4 = СuSO4 + Н2О
ZnO + 2HCl = ZnСl2 + Н2О
4. Взаимодействие кислот с солями:
FeCl2 + H2S = FeS¯ + 2HCl
AgNO3 + HCI = AgCl¯ + HNO3
Ba(NO3)2 + H2SO4 = BaSO4¯ + 2HNO3
5. Взаимодействие растворов двух различных солей:
BaCl2 + Na2SO4 = ВаSO4¯ + 2NаСl
Pb(NO3)2 + 2NaCl = РbС12¯ + 2NaNO3
6. Взаимодействие оснований с кислотными оксидами (щелочей с амфотерными оксидами):
Са(ОН)2 + СО2 = СаСО3¯ + Н2О,
2NаОН(тв.) + ZnO 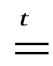 Na2ZnO2 + Н2О
Na2ZnO2 + Н2О
7. Взаимодействие основных оксидов с кислотными:
СаO + SiO2 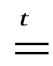 СаSiO3
СаSiO3
Na2O + SO3 = Na2SO4
8. Взаимодействие металлов с неметаллами:
2К + С12 = 2КС1
Fе + S 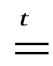 FеS
FеS
9. Взаимодействие металлов с солями.
Cu + Hg(NO3)2 = Hg + Cu(NO3)2
Pb(NO3)2 + Zn = Рb + Zn(NO3)2
10. Взаимодействие растворов щелочей с растворами солей
CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl
NaHCO3 + NaOH = Na2CO3+ H2O
Вопросы для самоконтроля
1 - Напишите уравнения реакций:
Na2 SO₄ + NaOH →
Ca(NO₃)₂ + K2 SO₄ →
BaCO₃↓®
¾ Что такое соли?
¾ Какие соли бывают?
¾ Назовите физические свойства солей.
¾ Где применяются соли?
¾ В вашей специальности соли нашли применение?
2 - Составьте уравнения следующих реакций и, пользуясь таблицей растворимости, определите, пройдут ли они до конца:
а) хлорид бария + сульфат натрия;
б) хлорид алюминия + нитрат серебра;
в) фосфат натрия + нитрат кальция;
г) хлорид магния + сульфат калия;
д) сульфид натрия + нитрат свинца;
е) карбонат калия + сульфат марганца;
ж) нитрат натрия + сульфат калия.
Уравнения записывайте в молекулярной и ионных формах.
ПЛАН ЗАНЯТИЯ № 16
Дисциплина: Химия.
Тема:Гидролиз солей. Оксиды и их свойства.
Цель занятия: Научиться определять реакцию среды раствора соли в воде, составлять уравнения реакций гидролиза неорганических веществ;Углубить, систематизировать, обобщить знания обучающихся об оксидах, способах их получения и областях применения.
Планируемые результаты
Предметные: понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач; владение основополагающими химическими понятиями, теориями, законами и закономерностями; уверенное пользование химической терминологией и символикой;
Метапредметные: использование различных видов познавательной деятельности и основных интеллектуальных операций (постановки задачи, формулирования гипотез, анализа и синтеза, сравнения, обобщения, систематизации, выявления причинно-следственных связей, поиска аналогов, формулирования выводов) для решения поставленной задачи;
Личностные: готовность к продолжению образования и повышения квалификации в избранной профессиональной деятельности и объективное осознание роли химических компетенций в этом;
Норма времени:2 часа
Вид занятия:Лекция.
План занятия:
1. Гидролиз солей.
2. Солеобразующие и несолеобразующие оксиды.
3. Основные, амфотерные и кислотные оксиды. Зависимость характера оксида от степени окисления образующего его металла.
4. Химические свойства оксидов.
5. Получение оксидов.
Оснащение:Учебник, периодическая система химических элементов.
Литература:
1. Химия 11 класс: учеб. для общеобразоват. организаций Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение, 2014. -208 с.: ил..
2. Химия для профессий и специальностей технического профиля: учебник для студ. учреждений сред. проф. образования / О.С.Габриелян, И.Г. Остроумов. – 5 - изд., стер. – М.: Издательский центр «Академия», 2017. – 272с., с цв. ил.
Преподаватель:Тубальцева Ю.Н.
Тема 16. Гидролиз солей. Оксиды и их свойства.
План:
1. Гидролиз солей.
2. Солеобразующие и несолеобразующие оксиды.
3. Основные, амфотерные и кислотные оксиды. Зависимость характера оксида от степени окисления образующего его металла.
4. Химические свойства оксидов.
5. Получение оксидов.
Гидролиз солей.
Кислая среда образуется в растворах кислот, так как кислоты диссоциируют с образованием ионов водорода: HCl ↔ H+ + Cl- Лакмус в кислой среде окрашивается в красный цвет.
Щелочная среда образуется в растворах щелочей и обусловлена наличием ОН-. Щёлочи диссоциируют с образованием гидроксид-ионов: NaOH ↔ Na+ + OH- Лакмус в щелочной среде окрашивается в синий цвет.
Нейтральная среда образуется тогда, когда концентрация ионов Н+ и ионов ОН- будут равны: [H+] = [OH-] Лакмус не изменяет окраску, остаётся фиолетовым.
Можно предположить, что нейтральная среда образуется в растворе любой средней соли, так как в их составе нет ионов водорода или ионов гидроксильных групп.
