Дифференцированный зачёт по химии.
Дифференцированный зачёт по химии.
Вариант 1.
Часть А
При выполнении заданий этой части выберите номер правильного ответа
| 1) | 6 и + 32 | 2) | 6 и + 16 3) 2 и +4 | 4) | 4 и + 32 |
А1. У атома серы число электронов на внешнем энергетическом уровне и заряд ядра равны соответственно
А2. Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно
| 1) | вода и сероводород 3) аммиак и водород |
| 2) | бромид калия и азот 4) кислород и метан |
А3. Степень окисления азота в молекуле NН3 равна
1) -1 2) -3 3) + 3 4) +5
А4. В ряду натрий – магний – алюминий
элементы расположены в порядке увеличения
| 1) | атомного радиуса 3) металлических свойств |
| 2) | электроотрицательности 4) числа энергетических уровней |
А5. Какой из металлов не вытесняет водород из разбавленной серной кислоты?
| 1) | железо | 2) | хром | 3) | медь | 4) | цинк |
А6.Углерод проявляет свойства окислителя при взаимодействии с
| 1) | кислородом 2)водородом 3)кальцием 4)оксидом меди |
А7. При нагревании гидроксида меди (II) образуются
| 1) | Cu и H2O | 2) | СuO и Н2 | 3) | CuO и Н2О | 4) | Сu2O и Н2О |
А8. Соль и вода образуются при взаимодействии растворов
| 1) | K2CO3 и Ba(OH)2 3) Н3РО4 и КОН |
| 2) | AlCl3 и NaOH 4) MgBr2 и Na3PO4 |
А9. В схеме превращений Al(OH)3 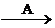 X
X 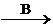 Al(OH)3
Al(OH)3
веществами «А» и «В» могут быть соответственно
| 1) K2SO4 и KOH 3) Na2SO4 и H2SO4 | |
| 2) NaCl и HCl 4) HNO3 и NaOH | |
А10. При взаимодействии карбоновых кислот и спиртов образуются
1) простые эфиры 2) сложные эфиры 3)углеводы 4) аминокислоты
А11. Реакция, уравнение которой Zn(OН)2 + H2SO4 = ZnSO4 + 2H2O,
относится к реакциям
1) обмена 2) соединение 3) разложение 4) замещение
А12. Для увеличения скорости взаимодействия железа с хлороводородной (соляной) кислотой следует
| 1) | добавить ингибитор 3) повысить давление |
| 2) | понизить температуру 4) увеличить концентрацию НС1 |
А13. Среда раствора хлорида натрия
1) Щелочная 2)кислая 3) нейтральная 4) слабокислая
А14. И бутан, и бутилен реагируют с
| 1) | бромной водой 3)водородом |
| 2) | раствором KMnO4 4) хлором |
А15. Для получения уксусной кислоты в одну стадию используют
| 1) | гидролиз карбида кальция |
| 2) | гидратацию этилена |
| 3) | окисление глюкозы |
| 4) | окисление ацетальдегида |
Часть В
В заданиях В1 – В2 установите соответствие цифра-буква.
В1. Установите соответствие между названием вещества и классом (группой) веществ, к которому(ой) оно принадлежит.
| ВЕЩЕСТВО | КЛАСС (ГРУППА) ВЕЩЕСТВ | ||
| 1) | вода | A) | кислая соль |
| 2) | гидрофосфат кальция | Б) | основание |
| 3) | хлорид калия | в) | средняя соль |
| 4) | гидроксид железа (III) | г) | кислота |
| Д) | оксид |
В2. Установите соответствие между исходными веществами и продуктами, которые образуются в ходе реакций.
| ИСХОДНЫЕ BЕЩЕСТBА | ПРОДУКТЫ РЕАКЦИИ | ||
| 1) | Fe + Cl2 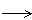 | А) | FeCl2 |
| 2) | Fe + HCl 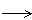 | Б) | FeCl3 |
| 3) | Cu + HNO3(конц.)  | B) | FeCl2 + H2 |
| 4) | Cu + HNO3(разб.)  | Г) | Cu(NO3)2 + H2 |
| Д) | Cu(NO3)2 + NO+ H2O | ||
| Е) | Cu(NO3)2 + NO2+ H2O |
Ответом к заданию В3 является последовательность букв. Запишите выбранные буквы в алфавитном порядке в лист ответов.
В3.Уксусная кислота взаимодействует с:
| а) | N2 Г) С2Н5ОН |
| б) | MgO Д) Na |
| в) | HNO3 Е) C2H6 |
Часть С
| Запишите сначала номер задания (С1 и т.д.), а затем полное решение. Ответы записывайте четко и разборчиво. |
| C1 |
Напишите уравнения реакций, с помощью которых можно осуществить превращения:
С2Н6 → С2Н5СI → С2Н5ОН → СН3СООН → СН3СООК
| C2 |
Вычислите,сколько сгорело угля, если при этом выделилось 33520 кДж. Термохимическое уравнение процесса имеет вид:С + О2 = СО2 + 402,24 кДж.
| C3 |
Вычислите, какой объём оксида углерода(IV) образуется при сгорании 0,25моль сахарозы (н.у.).
Вариант 2.
Часть А
Часть В
В заданиях В1 – В2 установите соответствие цифра-буква.
В 1. Установите соответствие между исходными веществами, вступающими в реакции обмена, и сокращенными ионными уравнениями этих реакций.
| ИСХОДНЫЕ BЕЩЕСТBА | СОКРАЩЕННЫЕ ИОННЫЕ УРАВНЕНИЯ | ||
| 1) | H2SO4 и BaCl2 | А) | Al3+ + 3OH– = Al(OH)3 |
| 2) | Ba(OH)2 и K2CO3 | Б) | Ba2+ + SO42– = BaSO4 |
| 3) | Al(NO3)3 и KOH | B) | Na+ + Br – = NaBr |
| 4) | BaBr2 и Na2SO4 | Г) | Ba2+ + CO32– = BaCO3 |
В 2. Установите соответствие между названием вещества и его химической формулой
Часть С
| Запишите сначала номер задания (С1 и т.д.), а затем полное решение. Ответы записывайте четко и разборчиво. |
С 1. Напишите уравнения реакций, с помощью которых можно осуществить превращения:
СаС2 →С2Н2→С6Н6→C6H5NO2→ C6H5NH2
С 2.На полную нейтрализацию 220 г раствора серной кислоты потребовалось 40 г 10% раствора гидроксида натрия. Рассчитайте массовую долю кислоты в исходном растворе.
С 3.Рассчитайте количество теплоты, которое выделяется при сжигании 15 м3 ацетилена (н.у.), если термохимическое уравнение реакции его горения
С2Н2 + 2,5О2 → 2СО2 + Н2О + 1300кДж
Дифференцированный зачёт по химии.
Вариант 1.
Часть А
