Особенности реакций изотопного обмена
1 Особенность Q=Eпр-Eобр=0 Eпр=Еобр Q=0
2 Особенность Кр=Кпр\Кобр=1 Кпр=Кобр К=х[A*X][BX]/[AX][B*X]=1
3 Особенность Епр=Еобр (1)
4 Особенность Кпр=Кобр (2)
5 Особенность Все реакции изотопного обмена описываются обычными концентрационными уравнениями применяемыми в химии.
Рассмотрим основные термодинамические и кинетические особенности реакций идеального изотопного обмена. Эти реакции протекают без изменения термодинамической активности участвующих в обмене веществ. Это обусловлено тем, что концентрация обменивающихся форм не меняется, а изменение изотопного состава частиц не приводит к изменению их силовых полей. По-этому значения термодинамических и концентрационных констант равновесия для реакций с участием этих частиц совпадают:
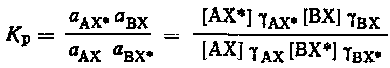
так как ¡AX = ¡AX*, ¡BX = ¡BX*.
Важной особенностью процессов изотопного обмена является о т с у т с т в и е т е п л о в ы х э ф ф е к т о в. Это следует из совпадения энергий связи и теплот образования изотопных разновидностей химических форм, участвующих в обмене. Следствием является строгая изотермичность процессов изотопного обмена и независимость константы равновесия от температуры. Действительно:
| DG0 = DH0 - TDS0 = -RT ln Kp, | (3.3) |
где DG0, DH0, DS0 — изменения стандартных энергии Гиббса, энтальпии и энтропии соответственно. Отсюда
ln Kp = -DH / RT + DS / R.
Дифференцируя это выражение, получим
DH = 0, то d(ln Kp) / d T = 0.
d(ln Kp) / d T = - DH / RT2.
Поскольку ,т. е. константа равновесия реакций идеального изотопного обмена не зависит от температуры.
Как следует из рассмотрения термодинамического поведения изотопных атомов, в случае идеального обмена DG0 = 0. Принимая во внимание, что для этих процессов DH0 = 0, из соотношения (3.3) следует, что DS0 = 0 и константа равновесия реакций идеального изотопного обмена равна единице. Поэтому состоянию равновесия реакций идеального изотопного обмена отвечает равнораспределение изотопов между обменивающимися формами, т. е. идентичность изотопного состава этих форм. Действительно, если
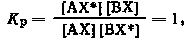
то
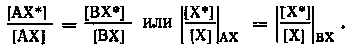
Одной из основных кинетических особенностей процессов идеального изотопного обмена является постоянство общей скорости обмена атомами данного элемента между всеми изотопными разновидностями, участвующими в обмене. Это постоянство обусловлено отсутствием химических изменений, неизменностью концентраций веществ, участвующих в обмене, и постоянством констант скорости обмена для различных идеальных изотопов данного элемента.
Носители. Их класификация
Носители – это соединения которое вводится в раствор в макроколичествах при определении макроэлемента и предназначено для уменьшения потерь микроэлемента.
Классификация:
1) Специфический изотопный носитель
Изотопный носитель – стабильный нуклид (макро) радиоактивного нуклида (микро)
2) Специфический не изотопный носитель- химичесий эллемент (соединение) не являющейси нуклидом опрелеояемого элемента , предназначеный для выделения конкретного элемента.
3) Не специфический не изотопный носитель- хим. Элемент (соединение) не являющейся нуклидом опр. Элемента, предназначеный как правило для выделения групп элементов. В качестве таких носителеф исп элементы образующие нерастворимые гидроксиды AL(OH)3; Fe(OH)3;
4) Удерживающий носитель –при выделение из смеси элементов, с целью уменьшения потерь опр. Элемента в исходный раствор воодят так называемый удерживающий носитель.
