Резка металла с помощью ультразвука
На обычных металлорежущих станках нельзя просверлить в металлической детали узкое отверстие сложной формы, например в виде пятиконечной звезды. С помощью ультразвука это возможно, магнитострикционный вибратор может просверлить отверстие любой формы. Ультразвуковое долото вполне заменяет фрезерный станок. При этом такое долото намного проще фрезерного станка и обрабатывать им металлические детали дешевле и быстрее, чем фрезерным станком.
Билет№14
Основные Положения Молекулярно-Кинетической Теории (Опытное Обоснование)
В основе молекулярно-кинетической теории строения вещества лежат три положения:
1. Все тела состоят из частиц (атомов, молекул, ионов и др.);
2. Частицы непрерывно хаотически движутся;
3. Частицы взаимодействуют друг с другом.
Первое положение подтверждают испарение жидкостей и твердых тел, получение фотографий отдельных крупных молекул и групп атомов, косвенные измерения масс и размеров молекул.
Капля нефти объемом 1,0 мм3 может образовать на поверхности воды пленку площадью 3,0 м2. Полагая, что эта пленка является монослоем и имеет толщину в одну молекулу, получаем диаметр молекулы
где М - молярная масса, NA- постоянная Авогадро.
Так как массы молекул очень малы, удобно использовать в расчетах не абсолютные значения масс, а относительные. По международному соглашению массы всех атомов и молекул сравнивают с 1/12 массы атома углерода (углеродная шкала атомных масс).
Относительной молекулярной (или атомной) массой вещества Мr называют отношение массы молекулы (или атома) m0 данного вещества к 1/12 массы атома углерода m0c:
Относительные атомные массы всех химических элементов точно определены. Складывая относительные атомные массы, можно вычислить относительную молекулярную массу:
Чем больше атомов и молекул содержится в макроскопическом теле, тем больше вещества содержится в нем. Число молекул в макроскопических телах огромно, поэтому удобно указывать не абсолютное число атомов или молекул, а относительное. Принято сравнивать число молекул или атомов в данном теле с числом атомов, содержащихся в углероде массой 12 г. Относительное число атомов или молекул в теле характеризует особая физическая величина - количество вещества.
Количеством вещества v называют отношение числа молекул N в данном теле, к числу атомов в 0,012 кг углерода:
Количество вещества измеряется в молях.
Моль равен количеству вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде массой 0,012 кг.
Моль - основная единица Международной системы (СИ). Рекомендуемые кратные и дольные единицы: кмоль, ммоль, мкмоль.
Постоянная Авогадро - число атомов, молекул (структурных элементов) в одном Моле вещества:
NA= 6,02 • 1023 моль-1 ~ 6 • 1023 моль-1.
Наряду с относительной молекулярной массой Мr в физике и химии широко используется понятие "молярная масса". Молярной массой вещества называют массу вещества, взятого в количестве 1 моля, m - масса вещества.
2. Второе положение МКТ о непрерывном движении частиц подтверждают такие явления, как броуновское движение и диффузия.
Броуновское движение - беспорядочное движение малых частиц в жидкости или газе, происходящее под действием молекул окружающей среды.
Причина броуновского движения - тепловое движение молекул среды и отсутствие точной компенсации ударов, испытываемых частицей со стороны окружающих ее молекул. Удары молекул среды приводят частицу в беспорядочное движение: скорость ее меняется по величине и направлению. Вследствие теплового движения частиц наблюдается явление диффузии, которое характеризуется проникновением молекул одного вещества между молекулами другого вещества при их соприкосновении
3. Диффузия лат. diffusio — распространение, растекание, рассеивание, взаимодействие) — процесс взаимного проникновения молекул одного вещества между молекулами другого, приводящий к самопроизвольному выравниванию их концентраций по всему занимаемому объёму[1]. В некоторых ситуациях одно из веществ уже имеет выравненную концентрацию и говорят о диффузии одного вещества в другом. При этом перенос вещества происходит из области с высокой концентрацией в область с низкой концентрацией (против градиента концентрации)
Примером диффузии может служить перемешивание газов (например, распространение запахов) или жидкостей (если в воду капнуть чернил, то жидкость через некоторое время станет равномерно окрашенной). Другой пример связан с твёрдым телом: атомы соприкасающихся металлов перемешиваются на границе соприкосновения. Важную роль диффузия частиц играет в физике плазмы.
Обычно под диффузией понимают процессы, сопровождающиеся переносом материи, однако иногда диффузионными называют также другие процессы переноса: теплопроводность, вязкое трение и т. п.
Скорость протекания диффузии зависит от многих факторов. Так, в случае металлического стержня тепловая диффузия проходит очень быстро. Если же стержень изготовлен из синтетического материала, тепловая диффузия протекает медленно. Диффузия молекул в общем случае протекает ещё медленнее. Например, если кусочек сахара опустить на дно стакана с водой и воду не перемешивать, то пройдёт несколько недель, прежде чем раствор станет однородным. Ещё медленнее происходит диффузия одного твёрдого вещества в другое. Например, если медь покрыть золотом, то будет происходить диффузия золота в медь, но при нормальных условиях (комнатная температура и атмосферное давление) золотосодержащий слой достигнет толщины в несколько микронов только через несколько тысяч лет.\
Билет№15
1. Попробуем получить нетривиальные результаты, используя уравнение Клайперона-Менделеева и основное уравнение МКТ.
Введем понятие средней кинетической энергии молекул:
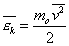 (1)
(1)
Преобразуем основное уравнение МКТ с учетом формулы (1):
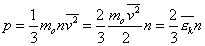 т.е. основное уравнение МКТ запишем так
т.е. основное уравнение МКТ запишем так 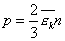 (2)
(2)
Воспользуемся уравнением К.-М. в таком виде:
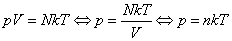 (3)
(3)
Сравним уравнения (2) и (3) и получим, что
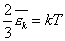 или
или 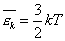 (4)
(4)
Мы выяснили, что от температуры зависит величина средней кинетической энергии молекул. Поэтому говорят, что температура - мера средней кинетической энергии молекул. Это утверждение мы доказали на для идеального газа, но оказывается оно справедливо и для других агрегатных сосятояний вещества.
2. Опыт Штерна — опыт, впервые проведённый немецким физиком Отто Штерном в 1920 году. Опыт явился одним из первых практических доказательств состоятельности молекулярно-кинетической теории строения вещества. В нём были непосредственно измерены скорости теплового движения молекул и подтверждено наличие распределения молекул газов по скоростям.
§ Для проведения опыта Штерном был подготовлен прибор, состоящий из двух цилиндров разного радиуса, ось которых совпадала и на ней располагалась платиновая проволока с нанесённым слоем серебра. В пространстве внутри цилиндров посредством непрерывной откачки воздуха поддерживалось достаточно низкое давление. При пропускании электрического тока через проволоку достигалась температура плавления серебра, из-за чего атомы начинали испаряться и летели к внутренней поверхности малого цилиндра равномерно и прямолинейно со скоростью v, соответствующей подаваемому на концы нити напряжению. Во внутреннем цилиндре была проделана узкая щель, через которую атомы могли беспрепятственно пролетать далее. Стенки цилиндров специально охлаждались, что способствовало оседанию попадающих на них атомов. В таком состоянии на внутренней поверхности большого цилиндра образовывалась достаточно чёткая узкая полоса серебряного налёта, расположенная прямо напротив щели малого цилиндра. Затем всю систему начинали вращать с некой достаточно большой угловой скоростью ω. При этом полоса налёта смещалась в сторону, противоположенную направлению вращения, и теряла чёткость. Измерив смещение s наиболее тёмной части полосы от её положения, когда система покоилась, Штерн определил время полёта, через которое нашёл скорость движения молекул:
§ 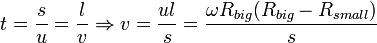 ,
,
§ где s — смещение полосы, l — расстояние между цилиндрами, а u — скорость движения точек внешнего цилиндра.
§ Найденная таким образом скорость движения атомов серебра совпала со скоростью, рассчитанной по законам молекулярно-кинетической теории, а тот факт, что получившаяся полоска была размытой, свидетельствовал в пользу того, что скорости атомов различны и распределены по некоторому закону — закону распределения Максвелла: атомы, двигавшиеся быстрее, смещались относительно полосы, полученной в состоянии покоя, на меньшие расстояния, чем те, которые двигались медленнее.
Билет№16
Постоянная Авогадро
Количество вещества ν равно отношению числа молекул в данном теле к числу атомов в 0,012 кг углерода, то есть количеству молекул в 1 моле вещества.
ν = N / NA
где N – количество молекул в данном теле, NA – количество молекул в 1 моле вещества, из которого состоит тело.
NA – это постоянная Авогадро. Количество вещества измеряется в молях.
Постоянная Авогадро – это количество молекул или атомов в 1 моле вещества. Эта постоянная получила своё название в честь итальянского химика и физика Амедео Авогадро (1776 – 1856).
В 1 моле любого вещества содержится одинаковое количество частиц.
NA = 6,02 * 1023 моль-1
Молярная масса – это масса вещества, взятого в количестве одного моля:
μ = m0 * NA
где m0 – масса молекулы.
Молярная масса выражается в килограммах на моль (кг/моль = кг*моль-1).
Молярная масса связана с относительной молекулярной массой соотношением:
μ = 10-3 * Mr [кг*моль-1]
Масса любого количества вещества m равна произведению массы одной молекулы m0 на количество молекул:
m = m0N = m0NAν = μν
Количество вещества равно отношению массы вещества к его молярной массе:
ν = m / μ
| 2. Массы атомов и молекул малы и составляют величины порядка 10-26 кг (так, масса молекулы воды составляет 3·10-26 кг). Поэтому для характеристики масс атомов и молекул применяются безразмерные величины, получившие название относительной атомной массы элемента и относительной молекулярной массы вещества. Относительной атомной массой (Ar) элемента называется отношение массы атома этого элемента к 1/12 массы атома 12С. Относительной молекулярной массой (Mr) вещества называется отношение массы молекулы этого вещества к 1/12 массы атома 12С. Масса, равная 1/12 массы атома 12С, называется атомной единицей массы (а.е.м.). Обозначим ее mед. Тогда масса атома будет равна Ar·mед, а масса молекулы - Mr·mед. Макроскопическая система должна содержать число частиц сравнимое с числом Авогадро, чтобы ее можно было рассматривать в рамках статистической физики. Числом Авогадро называется число атомов, содержащихся в 12 граммах углерода: NA=6,022·1023 (2) Отношение числа молекул N в макрообъекте к числу Авогадро NA называют количеством вещества: ν=N/NA (3) В качестве единицы количества вещества используется моль, то есть количество вещества, которое содержит столько же частиц (атомов, молекул, ионов), сколько атомов содержится в 12 граммах углерода. Поэтому размерность числа Авогадро - моль-1. Масса одного моля вещества называется молярной массой M. Молярная масса M связана с массой одной молекулы m0 соотношением: M=m0·NA (4) и измеряется в кг/моль. Если m - масса всего вещества, то количество вещества ν в молях равно: ν=m/M (5) Объем одного моля газа (V1) при нормальных условиях (давление p1=101,3 кПа; температура T1=273 К) составляет 22,4·10-3 м3 . Поэтому число молей газа, содержащихся в объеме V, можно записать и так: ν=V/V1 (6) |
Билет№17
1. МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ, взаимод. молекул между собой, не приводящее к разрыву или образованию новых хим. связей. Межмолекулярное взаимодействие определяет отличие реальных газов от идеальных, существование жидкостей и мол. кристаллов.
Модель идеального газа, используемая в молекулярно-кинетической теории газов, позволяет описывать поведение разреженных реальных газов при достаточно высоких температурах и низких давлениях. При выводе уравнения состояния идеального газа размерами молекул и их взаимодействием друг с другом пренебрегают. Повышение давления приводит к уменьшению среднего расстояния между молекулами, поэтому необходимо учитывать объем молекул и взаимодействие между ними. При рассмотренииреальных газов — газов, свойства которых зависят от взаимодействия молекул, надо учитыватьсилы межмолекулярного взаимодействия.
По мере развития представлений о строении атома и квантовой механики, было выяснено, что между молекулами вещества одновременно действуютсилы притяжения и силы отталкивания. Силы отталкивания считаются положительными, а силы взаимного притяжения — отрицательными.
Из анализа качественной зависимости потенциальной энергии взаимодействия молекул от расстояния между ними следует, что если молекулы находятся друг от друга на расстоянии, на котором межмолекулярные силы взаимодействия не действуют (r®¥), то П=0. При постепенном сближении молекул между, ними появляются силы притяжения, которые совершают положительную работу .
Критерием различных агрегатных состояний вещества является соотношениемежду величинами Пmin и kT. Пmin — наименьшая потенциальная энергия взаимодействия молекул — определяет работу, которую нужно совершить против сил притяжения для того, чтобы разъединить молекулы, находящиеся в равновесии.
Таким образом, любое вещество в зависимости от температуры может находиться в газообразном, жидком или твердом агрегатном состоянии, причем температура перехода из одного агрегатного состояния в другое зависит от значения Пmin, для данного вещества. Например, у инертных газов Пmin мало, а у металлов велико, поэтому при обычных (комнатных) температурах они находятся соответственно в газо образном и твердом состояниях.
2. Все вещества могут существовать в трех агрегатных состояниях - твердом, жидкоми газообразном. Четвертым агрегатным состоянием вещества часто считают плазму. Переходы между ними сопровождаются скачкообразным изменением ряда физических свойств (плотности, теплопроводности и др.).
Агрегатное состояние зависит от физических условий, в которых находится вещество. Существование у вещества нескольких агрегатных состояний обусловлено различиями в тепловом движении его молекул (атомов) и в их взаимодействии при разных условиях.
Газ - агрегатное состояние вещества, в котором частицы не связаны или весьма слабо связаны силами взаимодействия; кинетическая энергия теплового движения его частиц (молекул, атомов) значительно превосходит потенциальную энергию взаимодействий между ними, поэтому частицы движутся почти свободно, целиком заполняя сосуд, в котором находятся, и принимают его форму. Любое вещество можно перевести в газообразное, изменяя давление и температуру.
Жидкость - агрегатное состояние вещества, промежуточное между твердым и газообразным. Для нее характерна большая подвижность частиц и малое свободное пространство между ними. Это приводит к тому, что жидкости сохраняют свой объем и принимают форму сосуда. В то же время жидкость обладает рядом только ей присущих свойств, одно из которых - текучесть.
В жидкости молекулы размещаются очень близко друг к другу. Поэтому плотность жидкости гораздо больше плотности газов (при нормальном давлении). Свойства жидкости по всем направлениям одинаковы (изотропны) за исключением жидких кристаллов.
При нагревании или уменьшении плотности свойства жидкости, теплопроводность, вязкость меняются, как правило, в сторону сближения со свойствами газов.
Тепловое движение молекул жидкости состоит из сочетания коллективных колебательных движений и происходящих время от времени скачков молекул из одних положений равновесия в другие. При наличии внешней силы, сохраняющей свое направление более длительное время, чем интервалы между скачками, молекулы перемещаются в направлении этой силы, что и приводит к текучести жидкости.
Твердые тела - агрегатное состояние вещества, характеризующееся стабильностью формы и характером теплового движения атомов. Это движение вызывает колебания атомов (или ионов), из которых состоит твердое тело. Амплитуда колебаний обычно мала по сравнению с межатомными расстояниями.
Структура твердых тел многообразна, но, тем не менее, их можно разделять на кристаллы и аморфные тела.
В кристаллах атомы (или ионы) расположены в пространстве в узлах кристаллической решетки и колеблются около них. Строгая периодичность в расположении атомов приводит к сохранению порядка на больших расстояниях.
В аморфных телах атомы колеблются около хаотически расположенных точек. Свойства аморфных тел: они изотропны, не имеют постоянной температуры плавления, обладают текучестью.
По типам химической связи твердые тела делят на три класса, каждый из которых характеризуется определенным пространственным распределением электронов: 1) ионные кристаллы (NaCl, KaCl); 2) ковалентные (алмаз, Ge, Si); 3) металлические.
Кристаллическая структура твердых тел зависит от сил, действующих между атомами и частицами. Одни и те же атомы могут образовывать различные структуры - серое и белое олово, графит и алмаз.
Полиморфизм - способность некоторых веществ существовать в состояниях с различной атомно-кристаллической структурой (сера, кремнезем имеют более чем две полиморфные модификации).
Одиночные кристаллы называют монокристаллами. У монокристаллов некоторые свойства анизотропны, т. е. зависят от направления (механические, оптические и электрические). Естественная анизотропия - характерная особенность кристаллов; например, пластинка слюды легко расщепляется на тонкие листочки вдоль определенной плоскости (параллельно этой плоскости силы сцепления между частицами слюды наименьшие).
Твердое тело, состоящее из большого числа маленьких кристаллов, называют поликристаллическим. Поликристаллические материалы изотропны.
Плазма - частично или полностью ионизированный газ, в котором плотности отрицательных и положительных зарядов одинаковы. При сильном нагревании любое вещество испаряется, превращается в газ. Если увеличивать температуру и далее, резко усиливается процесс термической ионизации. Молекулы газа начнут распадаться на составляющие их атомы, которые затем превращаются в ионы
Билет№18
