Чт аминокислоты, белки, ферменты, нуклеиновые кислоты
Первичная структура белка
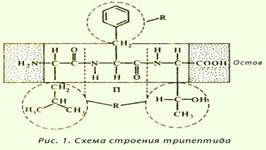 Первичной структурой белков называется линейная полипептидная цепь из аминокислот, соединенных между собой пептидными связями. Первичная структура - простейший уровень структурной организации белковой молекулы. Высокую стабильность ей придают ковалентные пептидные связи между α-аминогруппой одной аминокислоты и α-карбоксильной группой другой аминокислоты.
Первичной структурой белков называется линейная полипептидная цепь из аминокислот, соединенных между собой пептидными связями. Первичная структура - простейший уровень структурной организации белковой молекулы. Высокую стабильность ей придают ковалентные пептидные связи между α-аминогруппой одной аминокислоты и α-карбоксильной группой другой аминокислоты.
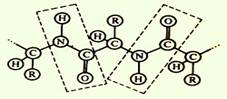
Пептидные группы с участием аминогруппы пролина или гидроксипролина способны образовывать только одну водородную связь . Это сказывается на формировании вторичной структуры белка. Полипептидная цепь на участке, где находится пролин или гидроксипролин, легко изгибается, так как не удерживается, как обычно, второй водородной связью.
Название пептидов складывается из названий входящих в них аминокислот. Две аминокислоты дают дипептид, три — трипептид, четыре — тетрапептид и т. д. Каждый пептид или полипептидная цепь любой длины имеет N-концевую аминокислоту, содержащую свободную аминогруппу, и С-концевую аминокислоту, содержащую свободную карбоксильную группу. Называя полипептиды, перечисляют последовательно все аминокислоты, начиная с N-концевой, заменяя в их названиях, кроме С-концевой, суффикс -ин на -ил (так как аминокислоты в пептидах имеют уже не карбоксильную группу, а карбонильную). Вторичная структура — локальное упорядочивание фрагмента полипептидной цепи, стабилизированное водородными связями. Вторичная структура представляет собой способ укладки полипептидной цепи в упорядоченную структуру благодаря образованию водородных связей между пептидными группами одной цепи или смежными полипептидными цепями. α-спирали — плотные витки вокруг длинной оси молекулы, один виток составляют 3,6 аминокислотных остатка, и шаг спирали составляет 0,54 нм (на один аминокислотный остаток приходится 0,15 нм), спираль стабилизирована водородными связями между H и O пептидных групп, отстоящих друг от друга на 4 звена. Хотя α-спираль может быть как левозакрученной, так и правозакрученной, в белках преобладает правозакрученная. Основные особенности α-спирали:1)спиральная конфигурация полипептидной цепи, имеющая винтовую симметрию;
2) образование водородных связей между пептидными группами каждого первого и четвертого аминокислотных остатков;
3)регулярность витков спирали;4)равнозначность всех аминокислотных остатков в α-спирали независимо от строения их боковых радикалов;5) боковые радикалы аминокислот не участвуют в образовании α-спирали.
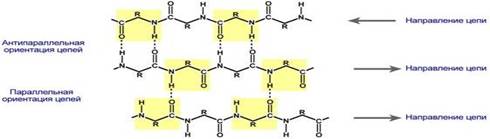
β-листы (β-структура, складчатые слои) — несколько зигзагообразных полипептидных цепей, в которых водородные связи образуются между относительно удалёнными друг от друга (0,347 нм на аминокислотный остаток[3]) в первичной структуре аминокислотами или разными цепями белка, а не близко расположенными, как имеет место в α-спирали. Полипептидные цепи в составе β-листов могут быть направлены N-концами в противоположные стороны (антипараллельная β-структура), в которой имеется β-изгиб, в одну сторону (параллельная β-структура), также возможно существование смешанной β-структуры (состоит из параллельной и антипараллельной β-структуры)[2]. Для образования β-листов важны небольшие размеры боковых групп аминокислот, преобладают обычно глицин и аланин. β-структура является второй по частоте встречаемости в белках после α-спирали. Антипараллельная структура является более стабильной, чем параллельная, т. к. водородные связи в ней короче.
 Коллаген. Главный опорный белок. Он образуется особой, тройной суперспиралью, сложенной из трех полипептидов. При этом внутри каждого полипептида, внутри каждой нити этой тройной спирали водородных связей нет — они есть только между нитями. Это — левая спираль, и период ее равен трем. Каждый 3-й кислотный остаток коллагена – это глицин.
Коллаген. Главный опорный белок. Он образуется особой, тройной суперспиралью, сложенной из трех полипептидов. При этом внутри каждого полипептида, внутри каждой нити этой тройной спирали водородных связей нет — они есть только между нитями. Это — левая спираль, и период ее равен трем. Каждый 3-й кислотный остаток коллагена – это глицин.
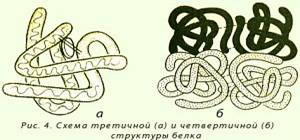 Третичной структурой белка называется способ укладки полипептидной цепи в пространстве. По форме третичной структуры белки делятся в основном на глобулярные и фибриллярные. Глобулярные белки чаще всего имеют эллипсовидную форму, а фибриллярные (нитевидные) белки — вытянутую (форма палочки, веретена). В стабилизации третичной структуры играют роль связи между боковыми радикалами аминокислот. Эти связи можно разделить на: сильные (ковалентные) и слабые (полярные и ван-дер-ваальсовы).Конформация третичной структуры полипептидной цепи определяется свойствами боковых радикалов входящих в нее аминокислот (которые не оказывают заметного влияния на формирование первичной и вторичной структур) и микроокружением, т. е. средой. При укладке полипептидная цепь белка стремится принять энергетически выгодную форму, характеризующуюся минимумом свободной энергии. Поэтому неполярные R-группы, "избегая" воды, образуют как бы внутреннюю часть третичной структуры белка, где расположена основная часть гидрофобных остатков полипептидной цепи. В центре белковой глобулы почти нет молекул воды. Полярные (гидрофильные) R-группы аминокислоты располагаются снаружи этого гидрофобного ядра и окружены молекулами воды. Полипептидная цепь причудливо изгибается в трехмерном пространстве. При ее изгибах нарушается вторичная спиральная конформация. "Ломается" цепь в слабых точках, где находятся пролин или гидроксипролин, поскольку эти аминокислоты более подвижны в цепи, образуя только одну водородную связь с другими пептидными группами. Другим местом изгиба является глицин, R-группа которого мала (водород). Поэтому R-группы других аминокислот при укладке стремятся занять свободное пространство в месте нахождения глицина. В молекуле белка с третичной конфигурацией встречаются участки в виде α-спиралей (спирализованные), β-структур (слоистые) и беспорядочного клубка. Только правильная пространственная укладка белка делает его активным; нарушение ее приводит к изменению свойств белка и потере биологической активности.Четвертичная структура. Некоторые белки построены из нескольких полипептидных цепей, каждая из которых имеет третичную структуру. Для таких белков введено понятие четвертичной структуры, которая представляет собой организацию нескольких полипептидных цепей с третичной структурой в единую функциональную молекулу белка. Такой белок с четвертичной структурой называется олигомером, а его полипептидные цепи с третичной структурой — протомерами или субъединицами
Третичной структурой белка называется способ укладки полипептидной цепи в пространстве. По форме третичной структуры белки делятся в основном на глобулярные и фибриллярные. Глобулярные белки чаще всего имеют эллипсовидную форму, а фибриллярные (нитевидные) белки — вытянутую (форма палочки, веретена). В стабилизации третичной структуры играют роль связи между боковыми радикалами аминокислот. Эти связи можно разделить на: сильные (ковалентные) и слабые (полярные и ван-дер-ваальсовы).Конформация третичной структуры полипептидной цепи определяется свойствами боковых радикалов входящих в нее аминокислот (которые не оказывают заметного влияния на формирование первичной и вторичной структур) и микроокружением, т. е. средой. При укладке полипептидная цепь белка стремится принять энергетически выгодную форму, характеризующуюся минимумом свободной энергии. Поэтому неполярные R-группы, "избегая" воды, образуют как бы внутреннюю часть третичной структуры белка, где расположена основная часть гидрофобных остатков полипептидной цепи. В центре белковой глобулы почти нет молекул воды. Полярные (гидрофильные) R-группы аминокислоты располагаются снаружи этого гидрофобного ядра и окружены молекулами воды. Полипептидная цепь причудливо изгибается в трехмерном пространстве. При ее изгибах нарушается вторичная спиральная конформация. "Ломается" цепь в слабых точках, где находятся пролин или гидроксипролин, поскольку эти аминокислоты более подвижны в цепи, образуя только одну водородную связь с другими пептидными группами. Другим местом изгиба является глицин, R-группа которого мала (водород). Поэтому R-группы других аминокислот при укладке стремятся занять свободное пространство в месте нахождения глицина. В молекуле белка с третичной конфигурацией встречаются участки в виде α-спиралей (спирализованные), β-структур (слоистые) и беспорядочного клубка. Только правильная пространственная укладка белка делает его активным; нарушение ее приводит к изменению свойств белка и потере биологической активности.Четвертичная структура. Некоторые белки построены из нескольких полипептидных цепей, каждая из которых имеет третичную структуру. Для таких белков введено понятие четвертичной структуры, которая представляет собой организацию нескольких полипептидных цепей с третичной структурой в единую функциональную молекулу белка. Такой белок с четвертичной структурой называется олигомером, а его полипептидные цепи с третичной структурой — протомерами или субъединицами
При четвертичном уровне организации белки сохраняют основную конфигурацию третичной структуры (глобулярную или фибриллярную). Например, гемоглобин - белок, имеющий четвертичную структуру, состоит из четырех субъединиц. Каждая из субъединиц — глобулярный белок и в целом гемоглобин тоже имеет глобулярную конфигурацию. Контакты между поверхностями субъединиц возможны только за счет полярных групп аминокислотных остатков, поскольку при формировании третичной структуры каждой из полипептидных цепей боковые радикалы неполярных аминокислот (составляющих большую часть всех протеиногенных аминокислот) спрятаны внутри субъединицы. Между их полярными группами образуются многочисленные ионные (солевые), водородные, а в некоторых случаях и дисульфидные связи, которые прочно удерживают субъединицы в виде организованного комплекса.
Доме́н белка́ — элемент третичной структуры белка, супервторичные структуры, представляющий собой достаточно стабильную и независимую подструктуру белка. В состав домена обычно входит несколько элементов вторичной структуры. Сходные по структуре домены встречаются не только в родственных белках (например, в гемоглобинах разных животных), но и в совершенно разных белках. Доменом называют часть пептидной цепи, образующей как бы самостоятельную глобулу, причем на одной пептидной цепи может быть два или больше доменов. Домены в одном белке могут быть одинаковыми или различными как по структуре, так и по функции. Часто домен по своей структуре и свойствам сходен с отдельным глобулярным белком. Самоорганизация надмолекулярных белковых структур. Внутриклеточное формирование простраственной структуры белков. Гипотеза «расплавленной глобулы». Шапероны, шаперонины. Деградация белков. Убиквитин – белок деградации. Секреция белков.Характерной особенностью белков с четвертичной структурой является их способность ксамоорганизации.Процесс самосборки отличается высокой специфичностью. Протомеры белка «узнают» друг друга и соединяются только между собой комплементарными поверхностями, и ошибочное соединение практически невозможно.После окончания трансляции для того чтобы белок приобрел присущие ему функциональные свойства, полипептидная цепь должна определенным образом свернуться в пространстве, сформировав функционально активную («нативную») структуру. Процесс формирования пространственной структуры белка называется фолдингом.Пространственная (третичная) структура белка характеризуется сочетанием элементов вторичной структуры (α-спиралей, β-слоев), а также гибких участков полипептидной цепи, называемых петлями. Процесс сворачивания полипептидной цепи имеет ступенчатый характер и включает:
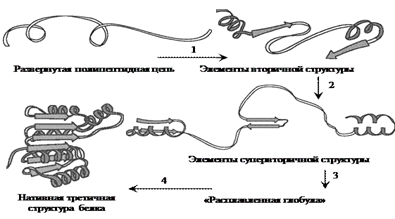
1) формирование элементов вторичной структуры;
2) специфическую ассоциацию некоторых элементов вторичной структуры с образованием супервторичной структуры: это могут быть сочетания нескольких α-спиралей, β-слоев или смешанные комплексы данных элементов;
3) промежуточную стадию, связанную с формированием основных элементов третичной структуры и образованием гидрофобного ядра молекулы. Молекула приобретает пространственную структуру, близкую к структуре нативного белка. Однако она еще не обладает присущей данному белку функциональной активностью. Это состояние, получившее название «расплавленная глобула», отличается от нативного меньшей степенью упорядоченности структуры (рис. 44);
4) образование нативной третичной структуры белка.Гипотеза расплавленной глобулы. В рамках этой концепции выделяют несколько этапов самосборки белков. 1. В развернутой полипептидной цепи с помощью водородных связей и гидрофобных взаимодействий образуются отдельные участки вторичной структуры, служащие как бы затравками для формирования полных вторичных и супервторичных структур. 2. Когда число этих участков достигает определенной пороговой величины, происходит переориентация боковых радикалов и переход полипептидной цепи в новую более компактную форму, причем число нековалентных связей значительно увеличивается. Характерной особенностью этой стадии является образование специфических контактов между атомами, находящимися на удаленных участках полипептидной цепи, но оказавшихся сближенными в результате образования третичной структуры. 3. На последнем этапе формируется нативная конформация белковой молекулы, связанная с замыканием дисульфидных связей и окончательной стабилизацией белковой конформации.Сворачивание полипептида в клетке сопровождается ферментативными модификациями цепи. Деформилаза отщепляет формильную группу концевого метионина вскоре после выхода N-конца растущей цепи из рибосомы. Аминопептидаза способна отщеплять N-концевой метионин. Мембранная сигнальная пептидаза отщепляет сигнальный пептид. Несколько ферментов принимают участие в гликозилировании белка. Кроме ферментов в формировании пространственной структуры белка участвуют специальные белки, увеличивающие эффективность сворачивания полипептидной цепи в нативную конформацию. . Эти белки, связываясь с развернутой или частично развернутой конформацией полипептидной цепи, не дают ей «запутаться», образовать неправильные структуры. Они удерживают частично развернутый белок, способствуют его переносу в разные субклеточные образования, а также создают условия для его эффективного сворачивания. Эти белки получили название «молекулярные шапероны». Прочно фиксированная на шаперонах полипептидная цепь не способна к сворачиванию в нативную структуру, так как не обладает необходимой для этого подвижностью. Главная функция этих белков состоит в удержании вновь синтезируемых белков от неспецифической агрегации и в их передаче другому «белку-помощнику», шаперонину, роль которого - обеспечить оптимальные условия для эффективного сворачивания.
Если третичная структура белков не может быть восстановлена, они разрушаются клеткой. Ферменты, осуществляющие деградацию белков, называются протеазами. По месту атаки молекулы субстрата протеолитические ферменты делятся на эндопептидазы и экзопептидазы:*Эндопептидазы, или протеиназы, расщепляют пептидные связи внутри пептидной цепи. Они узнают и связывают короткие пептидные последовательности субстратов и относительно специфично гидролизуют связи между определёнными аминокислотными остатками.*Экзопептидазы гидролизуют пептиды с концов цепи: аминопептидазы — с N-конца, карбоксипептидазы — с С-конца. Наконец, дипептидазы расщепляют толькодипептиды.Выделяют несколько классов протеаз, среди них сериновые протеазы, аспарагиновые протеазы, цистеиновые протеазы и металлопротеазы[59].Особый тип протеазы — протеасома, крупная мультисубъединичная протеаза, присутствующая в ядре и в цитоплазме эукариот, архей и некоторых бактерий.
Для того, чтобы белок-мишень расщепился протеасомой, он должен быть помечен путём присоединения к нему маленького белка убиквитина. Реакция присоединения убиквитина катализируется ферментами убиквитинлигазами. Присоединение первой молекулы убиквитина к белку служит для лигаз сигналом для дальнейшего присоединения молекул убиквитина. В результате к белку оказывается присоединена полиубиквитиновая цепь, которая связывается с протеасомой и обеспечивает расщепление белка-мишени[60][61]. В целом, эта система получила название убиквитин-зависимой деградации белка. Деградация 80—90 % внутриклеточных белков происходит при участии протеасомы.
 Деградация белка в пероксисомах важна для протекания многих клеточных процессов, включая клеточный цикл, регуляцию экспрессии генов и ответ на окислительный стресс.Секреция (лат. secretio «отделения, выделение») – процесс производства и выделение клеткой или железой любых веществ – секретов; этот процесс присутствует во всех живых организмах. Когда речь идет о процессе секреции в клетке, чаще всего подразумевается секреция белков, так как за большого размера и необходимую специфичность эти молекулы требуют использования сложных систем секреции. Клеточная секреция присутствует у эукариот, бактерий и архей.Клетки эукариот имеют очень развитую систему, предназначенную для секреции белков. Белки для секреции, синтезируются рибосомами, прикрепленными к грубому эндоплазматического ретикулума. В процессе синтеза, эти белки сквозь мембрану в люмена (полости) эндоплазматического ретикулума, где они подвергаются посттрансляционным модификациям и где молекулярные шапероны помогают сворачиванию белка. Неправильно свернутые белки обычно опознаются и перемещаются обратно в цитозоля для деградации протеазомою. Везикулы, наполненные свернутыми должным образом белками форме и с мембран ЭР и транспортируются в аппарат Гольджи. В аппарате Гольджи белки подальше модифицируются, в частности расщепление и вуглуводневих групп. Затем белки перемещаются в секреторные пузырьки, которые путешествуют по цитоскелету к краю клетки. Последние модификации могут происходить в секреторных пузырьках (например инсулин расщепления проинсулина). Наконец везитулы сливаются с клеточной мембраной в процесса, известного как экзоцитоз, выделяя свое содержимое за пределы клетки. В течение всего описанного цикла поддерживается строгий биохимический контроль pH.Свойства белков: растворимость, изоэлектрическая точка, денатурация и ренатурация. Основные методы выделения, фракционирования и изучения размеров и формы белковых молекул.
Деградация белка в пероксисомах важна для протекания многих клеточных процессов, включая клеточный цикл, регуляцию экспрессии генов и ответ на окислительный стресс.Секреция (лат. secretio «отделения, выделение») – процесс производства и выделение клеткой или железой любых веществ – секретов; этот процесс присутствует во всех живых организмах. Когда речь идет о процессе секреции в клетке, чаще всего подразумевается секреция белков, так как за большого размера и необходимую специфичность эти молекулы требуют использования сложных систем секреции. Клеточная секреция присутствует у эукариот, бактерий и архей.Клетки эукариот имеют очень развитую систему, предназначенную для секреции белков. Белки для секреции, синтезируются рибосомами, прикрепленными к грубому эндоплазматического ретикулума. В процессе синтеза, эти белки сквозь мембрану в люмена (полости) эндоплазматического ретикулума, где они подвергаются посттрансляционным модификациям и где молекулярные шапероны помогают сворачиванию белка. Неправильно свернутые белки обычно опознаются и перемещаются обратно в цитозоля для деградации протеазомою. Везикулы, наполненные свернутыми должным образом белками форме и с мембран ЭР и транспортируются в аппарат Гольджи. В аппарате Гольджи белки подальше модифицируются, в частности расщепление и вуглуводневих групп. Затем белки перемещаются в секреторные пузырьки, которые путешествуют по цитоскелету к краю клетки. Последние модификации могут происходить в секреторных пузырьках (например инсулин расщепления проинсулина). Наконец везитулы сливаются с клеточной мембраной в процесса, известного как экзоцитоз, выделяя свое содержимое за пределы клетки. В течение всего описанного цикла поддерживается строгий биохимический контроль pH.Свойства белков: растворимость, изоэлектрическая точка, денатурация и ренатурация. Основные методы выделения, фракционирования и изучения размеров и формы белковых молекул.
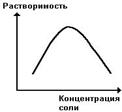 Белки бывают растворимые и нерастворимые в воде. Растворимость белков зависит от их структуры, величины рН, солевого состава раствора, температуры и других факторов и определяется природой тех групп, которые находятся на поверхности белковой молекулы. К нерастворимым белкам относятся кератин (волосы, ногти, перья), коллаген (сухожилия), фиброин (щелк, паутина). Многие другие белки растворимы в воде. Растворимость определяется наличием на их поверхности заряженных и полярных группировок (-СОО-, -NH3+, -OH и др.). Заряженные и полярные группировки белков притягивают к себе молекулы воды, и вокруг них формируется гидратная оболочка, существование которой обусловливает их растворимость в воде. На растворимость белка влияет наличие нейтральных солей (Na2SO4, (NH4)2SO4 и др.) в растворе. При малых концентрациях солей растворимость белка увеличивается, так как в таких условиях увеличивается степень диссоциации полярных групп и экранируются заряженные группы белковых молекул, тем самым снижается белок-белковое взаимодействие, способствующее образованию агрегатов и выпадению белка в осадок. При высоких концентрациях солей растворимость белка снижается (рис. 16) вследствие разрушения гидратной оболочки, приводящего к агрегации молекул белка.Существуют белки, которые растворяются только в растворах солей и не растворяются в чистой воде, такие белки называют глобулины. Существуют и другие белки – альбумины, они в отличие от глобулинов хорошо растворимы в чистой воде. Растворимость белков зависит и от рН растворов. Минимальной растворимостью обладают белки в изоэлектрической точке, что объясняется отсутствием электростатического отталкивания между молекулами белка. На растворимость белка оказывает влияние и температура. При действии высокой температуры многие белки выпадают в осадок вследствие нарушения их структуры.
Белки бывают растворимые и нерастворимые в воде. Растворимость белков зависит от их структуры, величины рН, солевого состава раствора, температуры и других факторов и определяется природой тех групп, которые находятся на поверхности белковой молекулы. К нерастворимым белкам относятся кератин (волосы, ногти, перья), коллаген (сухожилия), фиброин (щелк, паутина). Многие другие белки растворимы в воде. Растворимость определяется наличием на их поверхности заряженных и полярных группировок (-СОО-, -NH3+, -OH и др.). Заряженные и полярные группировки белков притягивают к себе молекулы воды, и вокруг них формируется гидратная оболочка, существование которой обусловливает их растворимость в воде. На растворимость белка влияет наличие нейтральных солей (Na2SO4, (NH4)2SO4 и др.) в растворе. При малых концентрациях солей растворимость белка увеличивается, так как в таких условиях увеличивается степень диссоциации полярных групп и экранируются заряженные группы белковых молекул, тем самым снижается белок-белковое взаимодействие, способствующее образованию агрегатов и выпадению белка в осадок. При высоких концентрациях солей растворимость белка снижается (рис. 16) вследствие разрушения гидратной оболочки, приводящего к агрегации молекул белка.Существуют белки, которые растворяются только в растворах солей и не растворяются в чистой воде, такие белки называют глобулины. Существуют и другие белки – альбумины, они в отличие от глобулинов хорошо растворимы в чистой воде. Растворимость белков зависит и от рН растворов. Минимальной растворимостью обладают белки в изоэлектрической точке, что объясняется отсутствием электростатического отталкивания между молекулами белка. На растворимость белка оказывает влияние и температура. При действии высокой температуры многие белки выпадают в осадок вследствие нарушения их структуры.
Изоэлектрическая точка. Заряд белковой молекулы зависит от содержания в ней кислых и основных аминокислот, а точнее, от ионизации кислых и основных групп бокового радикала этих аминокислот.Изоэлектрическая точка каждого белка определяется соотношением кислых и основных групп боковых радикалов аминокислот: чем выше соотношение кислые/основные аминокислоты в белке, тем ниже его изоэлектрическая точка. У кислых белков рН1 < 7, у нейтральных рН1 около 7, а у основных рН1 > 7. При значениях рН среды ниже его изоэлектрической точки белок будет нести положительный заряд, а выше — отрицательный заряд. Усредненная изоэлектрическая точка всех белков цитоплазмы лежит в пределах 5,5. Знание изоэлектрической точки очень важно для понимания стабильности белков в растворах, так как в изоэлектрическом состоянии белки наименее устойчивы. Незаряженные частицы белка могут слипаться друг с другом и выпадать в осадок. Денатурация белка.Денатурация – это процесс нарушения высших уровней организации белковой молекулы (вторичного, третичного, четвертичного) под действием различных факторов.
При этом полипептидная цепь разворачивается и находится в растворе в развернутом виде или в виде беспорядочного клубка.При денатурации утрачивается гидратная оболочка и белок выпадает в осадок и при этом утрачивает нативные свойства.Денатурацию вызывают физические факторы: температура, давление, механические воздействия, ультразвуковые и ионизирующие излучения; химические факторы: кислоты, щелочи, органические растворители, алкалоиды, соли тяжелых металлов.Различают 2 вида денатурации:1.Обратимая денатурация – ренатурация или ренактивация – это процесс, при котором денатурированный белок, после удаления денатурирующих веществ вновь самоорганизуется в исходную структуру с восстановлением биологической активности.2.необратимая денатурация – это процесс, при котором биологическая активность не восстанавливается после удаления денатурирующих агентов.
Выделение белков начинают с тончайшего измельчения (гомогенизации) ткани вплоть до разрушения клеточных стенок. Для этого используют специальные шаровые мельницы, различного типа гомогенизаторы, проводят растирание с кварцевым песком. Хорошие результаты дают методы разрушения клеточных оболочек путем попеременного замораживания и размораживания ткани или обработки ферментными препаратами (лизоцимом), а также методы продавливания ткани через мельчайшие отверстия (пресс-метод). После тонкого измельчения материала переходят к следующему этапу – экстракции белков. Белки извлекают чаще всего водой, 8–10%-ми растворами различных солей, разнообразными буферными системами (фосфатными, боратными, цитратными и др.), смесями органических реагентов (глицерина, одноатомных спиртов, уксусной кислоты, ацетона, фенола и др.) с водой. После экстракции смеси белков из биологического материала проводят разделение полученной смеси на индивидуальные белки. Фракционирование белков ведут разными способами: с использованием солей, органических растворителей, электрофоретически, хроматографически, методом молекулярных сит и пр.Метод фракционирования белков солевыми растворами основан на том, что каждый индивидуальный белок разделяемой смеси осаждается из нее при определенной концентрации той или иной соли. Процесс осаждения белка из раствора под действием соли называют высаливанием. Для фракционирования белков широко применяют водные растворы метилового и этилового спиртов, ацетон и другие органические растворители.
Метод электрофореза, используемый для фракционирования белков, основан на способности различных белков с разной скоростью перемещаться в растворе, по влажной фильтровальной бумаге или в другой твердой среде (крахмале, агар-агаре, полиакриламиде) под действием постоянного электрического тока. Скорость передвижения белковых молекул определенного вида к аноду или катоду зависит от их электрического заряда, молекулярной массы и формы, ионной силы, показателя рН и состава буферного раствора, а также приложенного потенциала.Хроматографический метод разделения белковых смесей или очистки белка от примесей заключается в пропускании фракционируемой смеси белков через хроматографическую колонку, заполненную адсорбентом (крахмалом, целлюлозой и ее производными, ионообменными смолами и т.д.). Для элюции адсорбировавшихся белков используют солевые растворы различной концентрации. Выход индивидуальных белков после фракционирования контролируют, проводя цветные реакции или измеряя поглощение белковых растворов в ультрафиолетовой области спектра.Фракционирование белков методом молекулярных сит (гельфильтрации) основано на различной скорости перемещения белковых молекул через колонку, заполненную специальным сетчатым полимером (сефадексом). В зависимости от молекулярной массы белков внутренний объем ячеек сефадекса в той или иной степени доступен для белковых молекул. Крупные молекулы белков, не способные проникнуть внутрь ячеек, выносятся из колонки элементом первыми, а мелкие молекулы белка, проникшие внутрь ячеек, задерживаются в них и выходят из колонки вслед за первыми в порядке уменьшения их молекулярной массы. Поэтому сефадекс называют также “антиситом”.По составу белки можно разделить на простые и сложные, первые содержат в молекуле только аминокислоты, вторые — еще и другие структуры (добавочные или простетические группы).
Простые белки по растворимости и пространственному строению разделяют на глобулярные и фибриллярные.
Глобулярные белки отличаются шарообразной формой молекулы (эллипсоид вращения), растворимы в воде и в разбавленных солевых растворах. Хорошая растворимость объясняется локализацией на поверхности глобулы заряженных аминокислотных остатков, окруженных гидратной оболочкой, что обеспечивает хороший контакт с растворителем. К этой группе относятся все ферменты и большинство других биологически активных белков, исключая структурные.
Среди глобулярных белков можно выделить'1) альбумины — растворимы в воде в широком интервале рН (от 4 до 8,5), осаждаются 70-100%-ным раствором сульфата аммония;2) полифункциональные глобулины с большей молекулярной массой, труднее растворимы в воде, растворимы в солевых растворах, часто содержат углеводную часть;
3) гистоны — низкомолекулярные белки с высоким содержанием в молекуле остатков аргинина и лизина, что обусловливает их основные свойства;4) протамины отличаются еще более высоким содержанием аргинина (до 85%), как и гистоны, образуют устойчивые ассоциаты с нуклеиновыми кислотами, выступают как регуляторные и репрессорные белки — составная часть нуклеопротеинов;5) проламины характеризуются высоким содержанием глутаминовой кислоты (30-45%) и пролина (до 15%), нерастворимы в воде, растворяются в 50-90%—яом этаноле;6) глутелины содержат около 45% глутаминовой кислоты, как и проламины, чаще содержатся в белках злаков.Фибриллярные белки характеризуются волокнистой структурой, практически не растворимы в воде и солевых растворах. Полипептидные цепи в молекулах расположены параллельно одна другой. Участвуют в образовании, структурных элементов соединительной ткани (коллагены, кератины, эластины).Сложные белки (протеиды) содержат наряду с протеиногенными аминокислотами органический или неорганический компонент иной природы — простетическую группу. Она связана с полипептидной цепью ковалентно, гетеропо-лярно или координационно. Важнейшие представители: гликопротеины (нейтральные сахара, аминосахара, кислые производные моносахаридов), липопротеины (триацилглицериды, фосфолипиды и холестерол), металлопротеины (ион металла, связанный ионной или координационной связью), фосфопротеины (остатки фосфорной кислоты, связанные через остаток серина или треонина), нуклеопротеины (нуклеиновые кислоты), хромопротеины (окрашенный компонент — пигмент или хромоген).Функции белков. Каталитическая или ферментативная. Все химические превращения в живом организме протекают при участии катализаторов. Биологические катализаторы (ферменты) по химической природе белки, следовательно, катализируют в организме химические превращения, из которых складывается обмен веществ.Транспортная функция. Белки транспортируют или переносят биологически значимые соединения в организме. В одних случаях транспортируемое соединение сорбируется белковой молекулой. Это защищает от разрушения и обеспечивает перенос с током крови (например, транспорт альбумином некоторых гормонов, витаминов, лекарственных соединений). Этот вид транспорта называют пассивным. В других случаях пассивный транспорт сочетается с депонированием (запасанием) тех или иных соединений (например, трансфер-рин плазмы крови не только переносит железо, но и запасает (накапливает) его при избытке). С помощью мембранных белков переносятся соединения из зон с низкой концентрацией в зону с высокой. Это сопряжено с заметным потреблением энергии и называется активным транспортом (например, транспорт ионов натрия из цитоплазмы и калия в цитоплазму).
Механохимическая функция — способность некоторых белков изменять конформацию, уменьшать длинник молекулы, т.е. укорачивать или сокращать молекулы. Такие белки называют сократительными (некоторые мышечные белки). Название вытекает из того, что сократительные белки выполняют механическую работу за счет энергии химических связей.
Структурная (пластическая) функция выполняется белками — элементами клеточных мембран (эти белки могут обнаруживать каталитическую или транспортную активность), но главным образом фибриллярными белками. Последние в составе соединительных тканей обеспечивают их прочность и эластичность' кератин шерсти и волос, коллагены сухожилий, кожи, хрящей, стенок сосудов и связывающих тканей.Гормональная функция (функция управления) реализуется гормонами пептидной или белковой природы. Они, влияя на продукцию или активность белков-ферментов, изменяют скорость катализируемых ими химических реакций, т.е. в конечном счете управляют обменными процессами. Защитная функция белков реализуется антителами, интерферонами и фибриногеном.
Антитела — соединения белковой природы, синтез которых индуцируется в процессе иммунного ответа — реакции организма на проникновение во внутреннюю среду посторонних белков или других антигенных компонентов (например, высокомолекулярных углеводов). Антитела, соединяясь с антигеном, образуют нерастворимый комплекс, делая антиген безопасным для организма.Интерфероны — гликопротеины, синтезирующиеся клеткой после проникновения в нее вируса. В отличие от антител интерфероны взаимодействуют не с антигеном, а вызывают образование внутриклеточных ферментов Они блокируют синтез вирусных белков, препятствуя копированию вирусной информации. Это приостанавливает размножение вируса.Фибриноген — растворимый белок плазмы, который на последней стадии процесса свертывания крови трансформируется в фибрин — нерастворимый белок. Фибрин образует каркас тромба, ограничивающего кровопотерюПлазмин — белок плазмы крови, катализирующий расщепление фибрина. Это обеспечивает восстановление проходимости сосуда, закупоренного фибриновым сгустком.
Энергетическая функциябелков обеспечивается за счет части аминокислот, высвобождающихся при расщеплении белка в тканях. В процессе окислительно-восстановительного распада аминокислоты высвобождают энергию и синтезируют энергоноситель — АТФ. На долю белка приходится около 18% энергопотребления у человека.
Ферменты
Роль ферментов Ферменты выступают в роли катализаторов практически во всех биохимических реакциях.Они необходимы для переваривания пищевых продуктов, стимуляции деятельности головного мозга, процессов энергообеспечения клеток, восстановления органов и тканей.
Классификация. КФ 1: Оксидоредуктазы, катализирующие перенос электронов, то есть окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа.КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.КФ 3: Гидролазы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза.КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов, а также обратные реакции.КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата с образованием изомерных форм.КФ 6: Лигазы, катализирующие образование химических связей C—C, C—S, C—O и C—N между субстратами за счёт реакций конденсации, сопряжённых с гидролизом АТФ. Пример: ДНК-полимераза.Второе число в наименовании фермента отражает подкласс, третье — подподкласс, а четвёртая — порядковый номер фермента в его подподклассе.[9]Будучи катализаторами, все ферменты ускоряют как прямую, так и обратную реакции, поэтому, например, лиазы способны катализировать и обратную реакцию — присоединение по двойным связям. Например, алкогольдегидрогеназаимеет номер КФ 1.1.1.1. – это оксидоредуктаза, действует на ОН-группу донора с НАД в качестве акцептора с первым порядковым номером в своем подподклассе;лактатдегидрогеназа– КФ 1.1.1.27, действует на ОН-группу донора с НАД в качестве акцептора с порядковым номером 27 в своем подподклассе.Специфичность, т.е. высокая избирательность действия ферментов, основана на комплементарности структуры субстрата и активного центра фермента.
-Стереоспецифичность- катализ только одного из стереоизомеров-Абсолютная специфичность – фермент производит катализ только одного вещества. Например, расщепление мочевины уреазой.
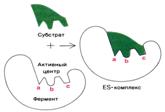 - Групповая специфичность – катализ субстратов с общими структурными особенностями, т.е. при наличии определенной связи или химической группыCпецифичность связывания субстрата с ферментом зависит от строго определённого расположения атомов в активном центре. Субстрат входит в активный центр, если он соответствует ему по форме. Существует две модели, описывающие взаимодействие субстрата с активным центром:
- Групповая специфичность – катализ субстратов с общими структурными особенностями, т.е. при наличии определенной связи или химической группыCпецифичность связывания субстрата с ферментом зависит от строго определённого расположения атомов в активном центре. Субстрат входит в активный центр, если он соответствует ему по форме. Существует две модели, описывающие взаимодействие субстрата с активным центром:
а) Модель жёсткого соответствия («ключ – замок»), предложена Э. Фишером в 1890 году. Активный центр считается заранее подогнанным под форму молекулы субстрата (рисунок 5.3). Эта модель не утратила своего значения для понимания некоторых свойств ферментов, например, их способности к строго определённому связыванию двух или большего числа субстратов или для объяснения кинетики насыщениясубстратом.
б) Модель индуцированнного соответствия («рука – перчатка»), предложена Кошлендом в 1950-е годы. Согласно этой модели, субстрат вызывает (индуцирует) конформационные изменения фермента, и лишь в результате этих изменений аминокислотные остатки фермента принимают пространственную ориентацию, необходимую для связывания субстрата и катализа (рисунок 5.4). При этом другие аминокислотные остатки могут погрузиться вглубь молекулы фермента.
 Изоферменты.Изоферменты, или изоэнзимы — это различные по аминокислотной последовательности изоформы или изотипы одного и того же фермента, существующие в одном организме, но, как правило, в разных его клетках, тканях или органах.Они гомологичны по аминокислотной последовательности. Например, амилаза — панкреатическая амилаза отличается по аминокислотной последовательности и свойствам от амилазы слюнных желёз, кишечника и других органов.
Изоферменты.Изоферменты, или изоэнзимы — это различные по аминокислотной последовательности изоформы или изотипы одного и того же фермента, существующие в одном организме, но, как правило, в разных его клетках, тканях или органах.Они гомологичны по аминокислотной последовательности. Например, амилаза — панкреатическая амилаза отличается по аминокислотной последовательности и свойствам от амилазы слюнных желёз, кишечника и других органов.
Строение ферментов.Белковая часть сложного фермента получила название апофермент, небелковая часть — кофактор. Кофакторы могут иметь разную химическую природу и отличаться по прочности связи с апоферментом. В роли кофактора могут выступать ионы различных металлов, а также другие неорганические ионы.Органические вещества неаминокислотной природы, используемые в роли кофакторов, называются коферментами. Кофермент вместе с апоферментом образуют холофермент.Кофермент + Апофермент ↔ Холофермент.В некоторых случаях в условиях живой клетки равновесие в этой реакции сильно сдвинуто вправо и кофермент прочно связан со своей белковой частью, они не разделяются при выделении и очистке. Такой кофермент называется простетическойгруппой. Функцией кофермента является участие в катализируемой реакции, причём количество кофермента и его химическое строение внешне остаются неизменными. коферменты могут быть охарактеризованы как переносчики определённых атомов, электронов или химических групп на соответствующий акцептор. Строение апофермента определяет специфичность этой реакции, а строение кофермента – её тип. Многие коферменты и простетические группы ферментов являются производными витаминов — органических веществ, которые не синтезируются в организме человека и должны поступать в составе пищевых продуктов. Они называются витаминными коферментами. В молекуле такого кофермента активным компонентом, соединяющимся с переносимой группой, служит именно витамин. Остальная часть молекулы кофермента обеспечивает специфическое связывание с апоферментом в строго определённой ориентации.Активный центр. Активный центр – участок молекулы фермента, который связывает субстраты и от которого зависит специфичность каталитического действия ферментов; активный центр содержит функциональные группы остатков аминокислот и коферментов, простр<
