Волновые свойства электрона. Квантовые числа,s-, p-,d-,f-состояния электронов. Электронные орбитали.
Атомные частицы обладают одновременно и корпускулярными, и волновыми св-ми.
Луи де Бройль p=mv длина волны h/mvh-постоянная Планка 6.6 *1034 Дж*с.
Волновыесв-ва: дифракция и интерференция.
Корпускулярныесв-ва: электрон действует как частица, как единое целое. Движ.–пульсирующее. Сост.любого электрона в атоме может быть охарактеризовано набором 4 квантовых чисел: n, l, m, s.Гл.кв.ч.характеризует общий уровень эн.эл-на. Принимает знач. от 1 до 7 (соотв.буквенным обозначениям: k,l,m,n,o,p,q).Эл-е уровни подразделяются на подуровни. Эл-ны одного и того же подуровня различны по величине момента кол-ва дв-я mvr ( r – радиус орбиты).Число подуровней=числу уровн(макс.ч.подуровней–4).Побочное (орбитальное)кв.числохар-етэнергетич.сост. электрона на подуровне (l=n-1).Магн.к.ч.опр. ориентацию эл-го облака в пространстве (+3,+2,+1,0, -1, -2, -3).Спиновое к.ч. характеризует напр.вр-я электрона. (+1/2 и -1/2). Наиб.ч. эл-ов на подуровне вычисл.по формуле 2n2.макс.число – 32. Распр.эл-ов по уровням и подуровням изобр. с помощью электронных формул или ячеек. Пример: Mg-1s22s22p63s2.
Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
Принцип Паули: в атоме не может быть 2 электронов с одинаковым набором всех 4 к.ч.
У двух электронов могут быть попарно одинаковыми 3 числа, но они обязаны различаться по четвертому.
Наибольшее число электронов Z в оболочке с главным квантовым числом. 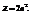
Максимальное число электронов на одном уровне известных ныне электронов – 32.
Ограничение принципа Паули:внешний электронный уровень атомов (кроме элемента №46 – палладий) может состоять максимум из двух подуровней – S и P.
То есть максимально возможное число электронов на внешнем уровне отвечает конфигурации 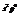 (8 электронов).
(8 электронов).
На s-2, на p(3орбиты)-6, на d(5орбит)-10, на f(7орбит)-14эл-ов.
Ионная (электронная связь).
В случае возникновения ионной связи между атомами или группами атомов преобладает электростатическое взаимодействие. Она возникает между атомами элементов, значительно отличающихся по величине электроотрицательности. 
Элементы, входящие в состав ионного соединения, всегда существуют в виде ионов, а не нейтральных атомов. Также нужно отметить, что полного разделения зарядов нет и имеет место частичнаяковалентность.Валентность в ионных соединениях определяется по числу зарядов слагающих их ионов.Ионы проводят электр. ток в растворах и расплавах и являются проводниками второго рода.
15.Направленность ковалентной связи ᵹ- и π-связи. Гибридизация атомныхорбиталей.
Гибридизация атомных орбиталей.К.с. возникает м/у элементами с одинаковым или близким знач-м эн.сродства к эл-ну.Перекрывание облаков при обр-ниик.с. возможно только при опред.их взаимной ориентации в пространстве – отсюда направл-ть связей, приводящая к опред. форме молекул. При этом обл. перекрывания расп-сяопр-м обр-м по отн-ю к взаимодейств-м атомам. 1.Молекулы типа AA, BB, АВ.Характерен для водорода, галогенов и соед. «галоген+водород». Молекулы имеют линейчатую структуру. Хим.св. действ.пократчайш.расстоянию(сигма-связь).2.Молекулы типа A2B.Характерен для соед., образ-х элем-ми главной подгруппы 6-ой группы: Н2О, Н2S,H2O-валентный угол 1050H2S-валентный угол92033’ 3. Молекулы типаA3B. Характерен для соед., образ-х элем-ми гл.подгр.5-й группы (N, P, As, Sb, Bi).Мол-ла аммиака (NH3) имеет форму пирамиду с треуг-м основании.4.Молекулы типа A4B. Гл.подгр.4-й гр.(Si,C,Ge,Sn, Pb)Молекула метана имеет форму тетраэдра (по вершинам – атомы водорода, атом углерода –в центре).5. Молекулы типа AB3.Гл.подгруппа 3-ей гр.(B,Al,Ga,In, Tl). Мол-лаBCl3имеет вид равностор.треуг-ка.6.Мол-лы типа AB2.Хар-рен для некоторых соед., образ-ми элем-ми гл.подгруппы 2гр.. ВеCl2(линейн.структура, угол–180).Если в мол-ле имеется кратная связь м/у атомами (2-ная или 3-ная),то только одна связь яв-ся прочной-пи-связь.Остальные–сигма-связи. Пример.Рассм. мол-лу этилена (С2Н4). неполная гибридизация М/у атомами углерода одна из связей «пи». Все остальне– «сигма».
