Химическое равновесие в растворах электролитов
1. Знать понятия:
дисперсная система, грубодисперсная система, коллоидный раствор, истинный раствор, растворение, насыщенный раствор, ненасыщенный раствор, пересыщенный раствор, растворимость, концентрация растворов, массовая, мольная и атомная доля растворенного вещества, молярность, моляльность, нормальность (эквивалентная концентрация).
Растворитель, растворенное вещество, идеальный раствор, перекристаллизация. Диссоциация, степень электролитической диссоциации, электролиты и неэлектролиты, гидролиз, степень гидролиза. Протолиз.
Кислоты и основания по теории С.Аррениуса и Бренстеда-Лоури, сопряженные пары кислот и оснований, константы равновесия в растворах электролитов: константа диссоциации, Ка, Кв ,ПР, константа гидролиза, ионное произведение воды. Кислотность среды, рН.
Знать опытные факты, послужившие основанием для разработки теории электролитической диссоциации (ТЭД) Аррениуса.
Знать основные положения ТЭД Аррениуса.
Знать основные положения протолитической теории Бренстеда-Лоури.
5. Уметь:
1) рассчитывать концентрацию растворов и переводить в другие способы ее выражения (массовую долю в молярность, нормальность; молярность, нормальность в массовую долю); приготовить раствор с заданной массовой долей, молярностью и нормальностью;
2) вычислять растворимость, массу кристаллизующегося вещества при изменении температуры раствора; объяснять влияние природы вещества, присутствия посторонних или одноименных ионов, температуры и давления на растворимость твердых веществ и газов в жидкостях; объяснять сущность процесса перекристаллизации и осуществлять его практически;
3) составлять уравнения реакций электролитической диссоциации кислот, оснований и солей (средних, кислых и основных), реакций ионного обмена в водных растворах в ионном и молекулярном виде;
4) объяснять сущность кислотно-основного взаимодействия в водных растворах с точки зрения теории Аррениуса и Бренстеда-Лоури;
5) записывать выражение константы диссоциации средних и слабых электролитов, кислотности, основности, произведения растворимости;
6) прогнозировать направление реакций ионного обмена с помощью теорий С.Аррениуса и Бренстеда-Лоури;
7) экспериментально определять рН водных растворов и теоретически рассчитывать рН и степень протолиза в водных растворах кислот, оснований и солей, пользуясь справочными данными;
8) объяснять влияние температуры, одно- и разноименных ионов, присутствия металлов на равновесие в водных растворах электролитов;
9) объяснять и прогнозировать силу кислоты на основании правила Л.Полинга и теории поляризации.
6. Задачи для решения:
Примеры решения задач
Задача 1
Определите рН в 0,012 М растворе гидроксида бария при 25 0С.
Решение: Гидроксид бария – сильный электролит и в разбавленном растворе диссоциирует практически полностью согласно уравнению реакции:
Ba(OH)2 = Ba2+ + 2OH-,
рН такого раствора можно вычислить по следующей формуле:
рН = 14 – рОН = 14 + lg [OH-] = 14 + lg (2×0,012) = 12,38.
Ответ: 0,012 М раствор гидроксида бария имеет рН, равный 12.38.
Задача 2
Определите рН в 0,002 М растворе хлорноватистой кислоты при 250С.
Решение. Хлорноватистая кислота –слабый электролит и в водном растворе диссоциирует обратимо по уравнению реакции:
HClO + H2O ↔ ClO- + H3O+.
Константа равновесия этой реакции – это константа кислотности Кa.
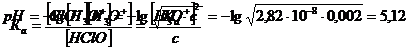
Ответ: 0,002 М раствор хлорноватистой кислоты имеет рН 5,12.
Задача 3
Определите рН 0,002 М раствора сульфата хрома (III) при 250С.
Решение: Сульфат хрома (III) в растворе практически необратимо диссоциирует на ионы хрома (III) и сульфат – ионы. Катионы хрома (III) затем подвергаются обратимому протолизу, выполняя функцию слабой кислоты, в результате этого среда становится кислой. Указанный процесс изображают следующими уравнениями реакций:
Cr2(SO4)3 = 2Cr3+ + 3SO42-,
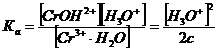 |
Cr3+×H2O + H2O ® CrOH2+ + H3O+, это равновесие описывается следующей константой:
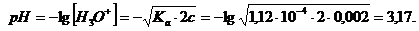
Ответ: 0,002 М раствор сульфата хрома(III) имеет рН 3,17.
Задача 4
Определите рН 0.002 М раствора цианида бария при 250С.
Решение. Цианид бария в растворе практически необратимо диссоциирует на катионы бария (II) и цианид-ионы, цианид-ионы подвергаются обратимому протолизу, выполняя функцию слабого основания. В результате среда раствора становится щелочной. Процессы диссоциации и протолиза можно выразить следующими уравнениями реакций:
Ba(CN)2 = Ba2+ + 2CN-,
CN- + H2O ® HCN + OH-,
последнее равновесие описывается константой основности:
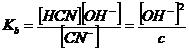 ;
;
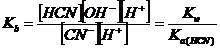 =
= 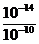 =10-4
=10-4
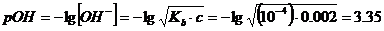 .
.
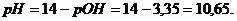
Ответ: 0,002 М раствор цианида бария имеетрН 10,65.
Задача 5
Определите степень диссоциации слабой кислоты НА в 0,01 М растворе с рН 3,38 при 250С.
Решение: Уравнениереакции диссоциациислабой кислоты имеет вид:
НА + Н2О ® А- + Н3О+,
Степень диссоциации слабой кислоты можно вычислить из следующего уравнения:
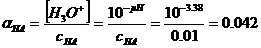
Ответ. Степень диссоциации 0,01 М раствора слабой кислоты НА равна 0,042 или 4,2%.
Задача 6
Определите степень протолиза в 0,002 М растворе гидрокарбоната натрия при 250С.
Решение. Диссоциация гидрокарбоната натрия описывается уравнением:
NaHCO3 = Na+ + HCO3-,
Анион HCO3- является амфолитом, поэтому в растворе протекают два процесса протолиза:
(I) HCO3- + H2O ® CO32- + H3O+;
(II) HCO3= + H2O ® H2CO3 + OH-.
Константа равновесия первого процесса – это константа кислотности КаII, согласно справочным данным она равна 4,68×10-11. Константу равновесия второго процесса можно рассчитать по уравнению:
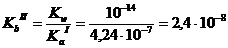
KbII>KaI, поэтому расчет проводим по уравнению (II).
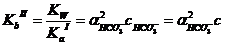
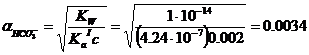
Ответ. Степень протолиза ионов HCO3- в водном растворе гидрокарбоната натрия равна 0,0034 или 0,34%.
Задача 7
Рассчитайте величину произведения растворимости фторида магния, если его растворимость в воде (L) равна 0,001 моль/л при некоторой температуре.
Решение.
В растворе фторида магния устанавливается следующее равновесие:
MgF2(тв) ↔ Mg2+ + 2F-, указанное равновесие характеризуется константой (ПР).
ПР = [Mg2+][F-]2 = S(2S)2 = 4S3 = 4(0,001)3 = 4×10-9.
Ответ: Произведение растворимости фторида магния равно 4×10-9.
Задача 8
Рассчитайте равновесную молярную концентрацию (моль/л) анионов в насыщенном растворе карбоната серебра (I) при 250С.
Решение.
При 250С в насыщенном растворе существует равновесие:
Ag2CO3(тв) ↔ 2Ag+ + CO32-;
ПР = [Ag+]2[ CO32-] = í2[CO32-]}2[CO32-] = 4[CO32-]3;
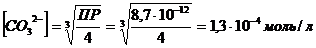
Ответ:Равновесная концентрация ионов CO32- в насыщенном растворе карбоната серебра (I) при 250С равна 1,3×10-4 моль/л.
Задача 9
Определите рН насыщенного раствора гидроксида кальция при 250С.
Решение.
В насыщенном растворе гидроксида кальция существует равновесие:
Ca(OH)2(тв) ↔ Ca2+ + 2OH-
Так как из уравнения реакции диссоциации следует, что [Ca2+] = ½[OH-], то
ПР = [Ca2+][OH-]2 = ½[OH-][OH-]2 = ½[OH-]3;
pH = 14 – pOH = 14 + lg[OH-];
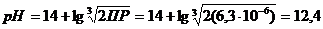
Ответ.При 250С насыщенный раствор гидроксида кальция имеет рН 12,4.
Задача 10
Написать уравнение реакции взаимодействия водных растворов плавиковой кислоты и гидрофосфата натрия. Обосновать термодинамическую вероятность протекания реакции.
Решение.
HF + Na2HPO4 ®
1. HF + H2O ® F- + H3O+; KIравн = Ka(HF) = 6,67∙10-4;
2. HPO42- + H3O+ ® H2PO4- + H2O; KIIравн = 
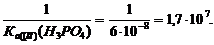

_____________________________________
HF + HPO42- ® F- + H2PO4-
Кравн = KI∙KII = 6,67∙10-4∙1,7∙107 = 1,1∙104. Кравн > 1, следовательно, реакция возможна в стандартных условиях.
Молекулярное уравнение реакции:
HF + Na2HPO4 = NaF + NaH2PO4.
Задача 11
Написать уравнение реакции взаимодействия водных растворов карбоната кальция и уксусной кислоты. Обосновать термодинамическую вероятность протекания реакции.
Решение.
CaCO3 + CH3COOH ®
1. CaCO3 ® Ca2+ + CO32- KI = ПР(CaCO3);
2. CH3COOH ® CH3COO- + H+ KII = Ka(CH3COOH);
3. 2H+ + CO32- ® H2CO3 KIII = 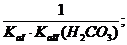
________________________________________________
CaCO3 + 2CH3COOH = Ca2+ + 2CH3COO- + H2O + CO2.
Молекулярное уравнение реакции:
CaCO3 + 2CH3COOH = Сa(CH3COO)2 + H2O + CO2.
K = KI∙(KII)2∙KIII = 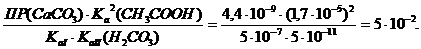
Константа равновесия реакции меньше единицы, значит реакция термодинамически невозможна в стандартных условиях.
Задача 12
Написать уравнение реакции взаимодействия водных растворов нитрата свинца и карбоната натрия. Обосновать термодинамическую вероятность протекания реакции.
Решение.
Pb(NO3)2 + Na2CO3 + H2O ®
В водном растворе соли могут вступать в реакцию обмена согласно уравнению
Pb2+ + CO32- ® PbCO3;
Kравн = 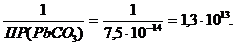
Вместе с тем взаимодействующие соли в водном растворе могут вступать в реакции протолиза согласно следующим уравнениям:
Pb2+ + H2O ↔ PbOH+ + H+;
CO32- + H2O ↔ HCO3- + OH-.
Одна из солей гидролизуется по катиону, другая по аниону, образующиеся ионы H+ и OH- взаимодействуют друг с другом с образованием молекул воды, что приводит смещению равновесия реакций протолиза солей в сторону продуктов реакции, и гидролиз может протекать необратимо, до конца. Поэтому, помимо реакции осаждения, в данном случае возможна реакция совместного (полного, необратимого) гидролиза солей. Рассчитаем константу равновесия этой реакции и сравним ее с константой равновесия реакции осаждения.
При совместном гидролизе протекают следующие процессы:
1) Pb2+ + H2O → PbOH+ + H+; К1 = Ka(Pb2+∙H2O/PbOH+) = 7,08∙10-7.
2) CO32- + 2H+ ® CO2 + H2O; К2 = 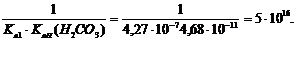
Образующиеся в результате протолиза ионы могут взаимодействовать с образованием малодиссоциирующих веществ:
2PbOH+ + CO32- ® (PbOH)2CO3; K= 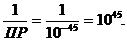
или
Pb2+ + 2OH- ® Pb(OH)2; K = 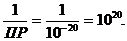
Сопоставляя величины констант равновесия реакций осаждения, приходим к выводу, что наиболее вероятна первая реакция, приводящая к образованию основной соли:
3) 2PbOH+ + CO32- ® (PbOH)2CO3; K3= 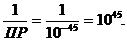
Итоговое уравнение реакции совместного гидролиза:
2Pb2+ + 2CO32- + H2O ® (PbOH)2CO3 + CO2, или, в молекулярном виде
2Pb(NO3)2 + 2Na2CO3 + H2O ® (PbOH)2CO3 + CO2 + 4NaNO3.
Константа равновесия этого процесса
К = К12∙ К2∙ К3 = (7,08∙10-7)2∙5∙1016∙1045 = 2,5∙1049.
Константа совместного гидролиза гораздо больше, чем константа осаждения карбоната свинца, поэтому протекает реакция совместного гидролиза.
5.1. Рассчитайте рН 0,1М растворов:
| а | б | в | г | д |
| HCOOH | HNO2 | HF | HN3 | CH3COOH |
| H2S | H3AsO4 | H2Se | H3PO4 | H2TeO3 |
| HBrO | H3AsO3 | HCN | H2N2O2 | HClO |
5.2. Рассчитайте рН раствора гидроксида аммония, если концентрация раствора равна:
а) 0,075 М; б) 0,005 М; в) 0,1 М; г) 0.025 М; д) 0.01 М; е) 0,05 М.
5.3. Определите рН указанных растворов щелочи М(ОН)2:
а) 0,0074; б) 0,0029 М; в) 0,0018 М; г) 0,0055 М; д) 0,0036 М; е) 0,0041 М.
5.4. Определите рН растворов селеновой кислоты, если концентрация раствора равна:
а) 0,023 М; б) 0,0078 М; в) 0,0037 М; г) 0,0052 М; д) 0,044 М; е) 0,0015 М.
5.5. Рассчитайте рН растора объемом 2,5 л, если в нем одновременно содержатся 0,0032 моль азотной кислоты и следующее количество вещества (моль) серной кислоты:
а) 0,0015; б) 0,0083; 0,0027; г) 0,0034; д) 0,0051; е) 0,0072.
5.6. Не прибегая к расчету, укажите в каждом наборе ту соль (из трех), в растворе которой (при одинаковой концентрации и температуре) рН будет больше:
| а | б | в | г | д | е | ж | з | и | к |
| Cu(NO3)2 | KBrO | NH4NO3 | Rb2S | NaN3 | FeSO4 | Ba(HCOO)2 | Pb(NO3)2 | AlCl3 | CsNO2 |
| Pb(NO3)2 | KCl | Rb2SO3 | NH4Cl | NaNO2 | CuSO4 | Ba(CN)2 | NH4NO3 | FeCl3 | CsCN |
| Ba(NO3)2 | KClO | Rb2CO3 | NH4ClO4 | NaOCN | ZnSO4 | Ba(NO2)2 | Ba(NO3)2 | GaCl3 | CsNO3 |
5.7. Определите рН 0,1М растворов солей:
| а | б | в | г | д | е |
| ZnBr2 | Cu(NO3)2 | CdSO4 | Pb(NO3)2 | FeSO4 | Be(ClO4)2 |
| AlCl3 | In(NO3)3 | CrCl3 | KCr(SO4)2 | Sc(NO3)3 | KAl(SO4)2 |
| Cr2(SO4)3 | Sc2(SeO4)3 | Al2(SO4)3 | Y2(SO4)3 | La2(SeO4)3 | In2(SO4)3 |
| CsNO2 | KF | NaBrO | KHCOO | RbCN | LiCH3COO |
| K2Se | Li2SO3 | Rb2CO3 | Na2SeO3 | K2AsO4 | Cs2TeO3 |
| Ba(NO2)2 | Ca(ClO)2 | Sr(CN)2 | Sr(NO2)2 | Ba(ClO)2 | Ca(CN)2 |
| KHS | NaH2AsO3 | CsHCO3 | Na2H4TeO6 | Na2HPO4 | K2HasO4 |
| NaH2PO4 | CsHCO3 | KH2AsO4 | LiHSO3 | KH2PO4 | NaHSeO3 |
5.8.Не прибегая к расчету, укажите, в растворе какой соли каждого набора (при постоянной концентрации и температуре) степень протолиза больше.
| а | б | в | г | д | е | ж | з |
| Cs2HPO4 | Rb2CO3 | Ba(HS)2 | K3AsO4 | Na2S | NaHSO4 | Na2S | K2SO3 |
| Cs3PO4 | RbHCO3 | BaS | K2HAsO4 | NaHSe | Na2SO3 | Na2Se | K2SeO3 |
5.9.Рассчитайте значение произведения растворимости, если известна растворимость (моль/л) вещества МА3 в воде при некоторой температуре: а) 1,2×10-3; б) 2,7×10-4; в) 0,034; г) 5,6×10-6; д) 8,3×10-4; е) 7,9×10-5.
5.10. Рассчитайте значение произведения растворимости, если известна растворимость (моль/л) вещества М2А в воде при некоторой температуре: а) 1,2×10-3; б) 2,7×10-4; в) 0,034; г) 5,6×10-6; д) 8,3×10-4; е) 7,9×10-5.
5.11. Рассчитайте значение произведения растворимости, если известна растворимость (моль/л) вещества М2А3 в воде при некоторой температуре: а) 1,2×10-3; б) 2,7×10-4; в) 0,034; г) 5,6×10-6; д) 8,3×10-4; е) 7,9×10-5.
5.12. Рассчитайте равновесную молярную концентрацию (моль/л) катионов в насыщенном растворе указанных солей при 250С:
| а | б | в | г | д |
| Ag2MoO4 | Ag2CrO4 | Ag2CO3 | Ag2C2O4 | Ag2SO4 |
| Tl2C2O4 | Tl2SeO4 | Tl2S | Tl2C rO4 | Tl2Se |
5.13. Рассчитайте равновесную молярную концентрацию (моль/л) анионов в насыщенном растворе указанных солей при 250С:
| а | б | в | г | д |
| BaF2 | MgF2 | PbCl2 | CaF2 | SrF2 |
| Ca(IO3)2 | Pb(BrO3)2 | Pb(IO3)2 | Ba(BrO3)2 | Cu(IO3)2 |
5.14. Рассчитайте растворимость (моль/л) следующих веществ при 250С.
| а | б | в | г |
| Tl3PO4 | Ag3AsO4 | Li3PO4 | Ag3AsO3 |
| Pb3(AsO4)2 | Ca3(PO4)2 | Cu3(AsO4)2 | Ba3(PO4)2 |
5.15. Рассчитайте значение ПР гидроксида металла M(OH)2, если известен водородный показатель его насыщенного раствора при 250С: а) 9,54; б) 9,17; в) 10,68; г) 9,76; д) 9,34; е) 10,24.
5.16. Определите рН насыщенного раствора указанного гидроксида при 250С.
| а | б | в | г | д |
| Mg(OH)2 | Cu(OH)2 | Mn(OH)2 | Fe(OH)2 | Co(OH)2 |
| Sc(OH)3 | Y(OH)3 | La(OH)3 | Ce(OH)3 | Nd(OH)3 |
5.17. Рассчитайте ПР, если известна массовая доля указанной соли в насыщенном растворе при некоторой температуре (плотность раствора принять равной 1 г/мл)
| Вариант | а | б | в | г | д |
| Соль | Pb(N3)2 | Ni(IO3)2 | Ag2WO4 | Ag2CO3 | Cd(CN)2 |
| w, % | 0,057 | 0,205 | 0,012 | 0,0086 | 0,057 |
5.18. Написать уравнения следующих реакций в ионной форме, рассчитать их константы равновесия:
1) Pb(CH3COO)2 + HCl ®
2) Al(OH)3 + KOH ®
3) Ca(CH3COO)2 + Na3PO4 ®
4) CH3COOH + Zn(OH)2 ®
5) CrCl3 + Ba(OH)2 ®
6) CuSO4 + H2S ®
5.19.Написать в молекулярной форме уравнения реакций, соответствующие следующим ионным уравнениям, рассчитать их константы равновесия:
1) Ca2+ + CO32- ® CaCO3
2) Al3+ + OH- ® Al(OH)3
3) Al(OH)3 + OH- ® [AL(OH)6]3-
4) Al(OH)3 + H+ ® Al3+ + H2O
5.20.Вычислить рН 0,46%-ного раствора муравьиной кислоты. Плотность раствора принять равной 1 г/см3.
5.21.Вычислить рН раствора, полученного растворением 1,12 л (н.у.) аммиака в 500 мл воды.
5.22.Вычислить рН 0,2 М раствора сернистой кислоты, приняв степень диссоциации кислоты равной 28% и учитывая лишь первую стадию диссоциации.
5.23.Вычислить рН раствора, полученного растворением в 1 л воды 0,44 г углекислого газа, учитывая лишь первую стадию диссоциации угольной кислоты.
5.24.Учитывая величины ПР труднорастворимых веществ, оценить, в какую сторону сдвинуто равновесие в следующих системах:
1) CaSO4 + Na2CO3 = CaCO3 + Na2SO4
2) BaSO4 + Na2CO3 = BaCO3 + Na2SO4
5.25.Вычислить ПР иодида свинца, если известно, что растворимость его при комнатной температуре равна 0,058 г на 100 г раствора.
5.26.Растворимость ортофосфата серебра равна 6,4 ∙ 10-4 г на 100 г раствора. Вычислить его ПР.
5.27.ПР карбоната серебра равно 6,15∙10-12. Вычислить растворимость этой соли на литр и в граммах на 100 г раствора.
5.28.Пользуясь величинами ПР для солей AgI, PbS, BaCO3, Ag2CO3, PbCl2, Ca3(PO4)2, сравнить их растворимость.
5.29.Будет ли выпадать осадок при добавлении к 100 мл 0,02 н. раствора сульфата калия 100 мл 0,01 н. раствора хлорида кальция?
5.30.Будет ли выпадать осадок при смешивании 100 мл 0,02 М раствора нитрата свинца с 200 мл 0,2 н. раствора соляной кислоты?
5.31.Будет ли выпадать осадок при смешивании 500 мл 0,01 н. раствора хлорида бария и 250 мл 0,1 н. раствора фтороводородной кислоты?
5.32.Будет ли выпадать осадок при добавлении к 200 мл 0,5 %-ного раствора хлорида цинка (r ~ 1г/мл) 18 мл 0,1 н. раствора аммиака?
5.33.Какое вещество будет выпадать в осадок при добавлении к раствору, содержащему в 1 л 0,01 моль сульфата натрия и 0,001 моль карбоната натрия, равного объема 0,001 М раствора хлорида кальция?
5.34.Какое или какие вещества будут выпадать в осадок, если к 1 л раствора, содержащего по 0,001 моль нитратов свинца и железа (II), добавить 0,5 л 0,01 М раствора сульфида железа?
5.35.Сколько молей ионов стронция будут оставаться в растворе после выпадения осадка, если слить равные объемы 0,01 н. раствора нитрата стронция и 0,02 н. раствора сульфата натрия?
5.36.Как зависит способность соли к протолизу от радиуса, заряда, поляризующего действия и поляризуемости катиона и аниона?
5.37.Почему многозарядные катионы, например Pb4+, Sn4+ и др., в водном растворе могут существовать лишь при низких значениях рН?
5.38.В каких случаях гидролиз может осложняться процессами полимеризации продуктов и образования многоядерных комплексов? Рассмотреть на примерах гидролиза хлоридов железа (III), олова (II), сурьмы (III) и силиката натрия.
5.39.При добавлении каких электролитов к водному раствору сульфита натрия гидролиз этой соли усиливается? Какие электролиты способны подавить гидролиз сульфита натрия?
5.40.Чем объяснить (привести расчет), что в водном растворе среднего ортофосфата натрия среда щелочная; гидрофосфата – слабощелочная; дигидрофосфата – слабокислая?
5.41.Почему водные растворы сульфида и гидросульфида натрия одинаковой молярной концентрации имеют разные рН: рН в растворе сульфида выше, чем гидросульфида?
5.42.Как объяснить, что водный раствор гидрокарбоната натрия имеет слабощелочную среду, а водный раствор гидросульфита натрия – слабокислую, хотя обе соли – соли слабых кислот?
5.43.Оценить реакцию среды в разбавленных растворах NH4CH3COO, (NH4)2CO3, NH4HCO3, (NH4)2S, NH4HS.
5.44.В каком растворе в каждой из указанных пар солей при одинаковой их молярной концентрации величина рН ниже: CrCl2 или CrCl3; CrCl3 или NaCrO2; NaCrO2 или Na2CrO4; BeSO4 или MgSO4; BeSO4 или Na2BeO2; Na3SbO4 или Na3SbO3?
5.45.Почему при смешении водных растворов сульфата алюминия и сульфида натрия, а также растворов нитрата алюминия и карбоната калия в осадок выпадает одно и то же вещество?
5.46.Почему при действии водного раствора сульфида натрия на раствор соли магния выделяется сероводород; при действии растворов хлорида аммония на раствор силиката натрия образуется осадок кремниевой кислоты?
5.47.Почему в водных растворах нельзя получить средние ацетаты олова (II), железа (III) и висмута (III); сульфиды магния, алюминия и хрома (III); сульфиты олова (II), алюминия и железа (III); средние карбонаты меди (II), ртути (II), алюминия, олова (II) и железа (III); средние силикаты висмута (III), ртути (II) и т. д.? Какие продукты могут выпадать в осадок в каждом из случаев?
5.48.Написать в ионной форме уравнения реакций, протекающих в водных растворах:
1) MgCl2 + Na2CO3 ® 4) KCr(SO4)2 + Na2S ®
2) CuSO4 + Na2CO3 ® 5) Pb(NO3)2 + Na2S ®
3) SnCl2 + Na2CO3 ® 6) AlCl3 + (NH4)2S ®
5.49.Какие из пар солей в водных растворах взаимно усиливают гидролиз: FeCl3 и Na2SO3; Al(CH3COO)3 и MgCl2; Cr2(SO4)3 и Na2S; Al(NO3)3 и ZnCl2; Al(NO3)3 и Na2S; Al(NO3)3 и Na2CO3? Написать уравнения реакций, мотивирующие ответ.
5.50.Чем определяется возможность гидролиза труднорастворимых солей? Подвергаются ли гидролизу соли PbS, FeS, Cr2S3?
5.51.Используя значения констант диссоциации соответствующих кислот, оценить, не проводя расчетов, какая из солей наиболее подвержена гидролизу в водном растворе:
| KHCOO | KCH3COO | KCN | KF | KNO2 | KClO | KBrO | |
| Кдисс | 2∙10-4 | 1.8∙10-5 | 5∙10-10 | 1∙10-4 | 5∙10-4 | 3∙10-8 | 2∙10-9 |
