Физические свойства воды и льда
Вода имеет молекулярную массу примерно равную 18,02 и может существовать в состояниях жидкости, пара и льда, характеризующихся следующими показателями фазовых переходов:
| Точка при 101,3 кПа (1 атм), °С замерзания (плавления) | 0,00 |
| кипения | 100,00 |
| Тройная точка | |
| температура, °С | 0,0099 |
| давление, Па (мм рт. ст.) | 610,4 (4,579) |
| Теплота, кДж/моль (ккал/моль) | |
| плавления при 0°С | 6,01 (1,435) |
| парообразования при 100°С | 40,63 (9,704) |
| сублимации при 0°С | 50,91 (12,16) |
Как видно из этих данных, для воды характерны высокая температура кипения и плавления, высокие значения теплоты фазовых переходов (плавления, парообразования, сублимации). По этим свойствам вода существенно отличается от гидридов некоторых элементов, расположенных близко к кислороду в периодической системе (СН4, NH3, HF, H2S, HC1). Это иллюстрируется некоторыми сведениями, представленными в табл. 10.1.
Вода обладает аномально высокой теплоемкостью. Это имеет большое значение в жизни природы — в ночное время, а также при переходе
Таблица 10.1. Физические свойства некоторых гидридов
| Вещество | Точка плавления, °С | Точка кипения, °С | Теплота парообразования при 100 °С, ккал/моль |
| CH4 | -184 | -161 | 2,20 |
| NH3 | -78 | -33 | 5,55 |
| HF | -92 | +19 | 7,22 |
| Н20 | +100 | 9,70 |
от лета к зиме вода остывает медленно, а днем или при переходе от зимы к лету так же медленно нагревается, являясь, таким образом, регулятором температуры на земном шаре.
Вода обнаруживает необычное свойство расширяться при замерзании, вследствие чего плотность льда ниже, чем воды при той же температуре (табл. 10.2), что нехарактерно для других веществ при переходе из жидкого состояния в твердое. Среди других аномалий воды следует отметить высокое значение поверхностного натяжения и диэлектрической постоянной и значительную теплопроводность (табл. 10.2). Теплопроводность воды выше, чем других жидкостей, а льда — больше, чем других неметаллических твердых веществ. Следует также отметить, что теплопроводность льда при 0°С приблизительно в четыре раза больше, чем воды при той же температуре, т. е. лед проводит тепло значительно быстрее, чем иммобилизованная (неподвижная) вода, находящаяся в тканях. Если при этом учесть, что температуропроводность льда на порядок выше, чем воды, становится понятным, почему ткани замерзают быстрее, чем оттаивают, если задается одинаковая (но обратная) разность температур.
Таблица 10.2. Влияние температуры на некоторые свойства воды и льда
| Показатели | Вода при температуре, ° С | Лед при температуре, ° С | ||
| -20 | ||||
| Плотность, г/см 3 | 0,9982 | 0,9998 | 0,9168 | 0,9193 |
| Давление водяного пара, Па (мм рт. ст.) | 2337 (17,53) | 610,4 (4,58) | 610,4 (4,580) | 103,4 (0,77) |
| Вязкость, Па ∙ с | 1,002 ∙ 10-3 | 1,787 ∙ 10-3 | — | — |
| Поверхностное натяжение, Н/мм | 72,75 ∙ 10-3 | 75,6 ∙ 10 -3 | — | — |
| Теплоемкость, Дж/кг ∙ К | 4,18 | 4,22 | 2,10 | 1,95 |
| Теплопроводность, Дж/м ∙ с ∙ К | 5,98 ∙ 102 | 5,64 ∙102 | 22,40 ∙ 102 | 24,33 ∙ 102 |
| Температуропроводность, м2/с | 1,4 ∙ 10-5 | 1,3 ∙ 10-5 | 1,1 ∙10-4 | 1,1 ∙10-4 |
| Диэлектрическая постоянная | 80,36 |
462 :: 463 :: Содержание
463 :: 464 :: 465 :: Содержание
Диаграмма состояния воды
Диаграмма состояния (или фазовая диаграмма) представляет собой графическое изображение зависимости между величинами,
характеризующими состояние системы, и фазовыми превращениями в системе (переход из твердого состояния в жидкое, из жидкого в газообразное и т. д.).
Для однокомпонентных систем обычно используются диаграммы состояния, показывающие зависимость фазовых превращений от температуры и давления; они называются диаграммами состояния в координатах Р—t.
На рис. 10.1 приведена в схематической форме (без строгого соблюдения масштаба) диаграмма состояния воды. Любой точке на диаграмме отвечают определенные значения температуры и давления.
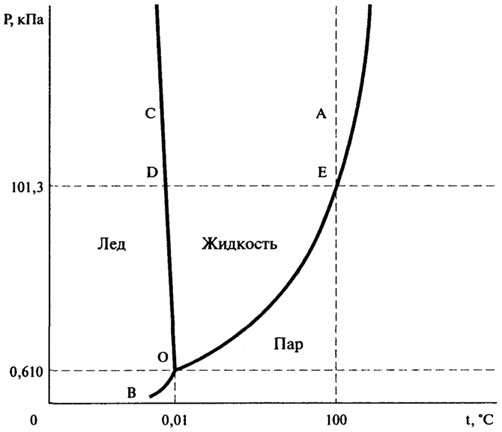
Рис. 10.1. Диаграмма состояния воды в области невысоких давлений
Диаграмма показывает те состояния воды, которые термодинамически устойчивы при определенных значениях температуры и давления. Она состоит из трех кривых, разграничивающих все возможные температуры и давления на три области, отвечающие льду, жидкости и пару.
Кривая ОА представляет зависимость давления насыщенного водяного пара от температуры: точки кривой показывают те пары значений температуры и давления, при которых жидкая вода и водяной пар находятся в равновесии друг с другом. Кривая ОА называется кривой равновесия жидкость — пар или кривой кипения.
Кривая ОС — кривая равновесия твердое состояние — жидкость, или кривая плавления, — показывает те пары значений температуры и давления, при которых лед и жидкая вода находятся в равновесии.
Кривая ОВ — кривая равновесия твердое состояние — пар, или кривая сублимации. Ей отвечают те пары значений температуры и давления, при которых в равновесии находятся лед и водяной пар.
Все три кривые пересекаются в точке О. Координаты этой точки — это единственная пара значений температуры и давления, при которых в равновесии могут находиться все три фазы: лед, жидкая вода и пар. Она носит название тройной точки.
Тройная точка отвечает давлению водяного пара 0,610 кПа (4,58 мм рт. ст.) и температуре О,О ГС.
Диаграмма состояния воды имеет значение при разработке технологических режимов для получения пищевых продуктов. Например, как следует из диаграммы, если лед нагревается при давлении меньше чем 0,610 кПа (4,58 мм рт.ст.), то он непосредственно переходит в пар. Это является основой при разработке способов получения пищевых продуктов сушкой замораживанием.
Одной из особенностей воды, отличающих ее от других веществ, является понижение температуры плавления льда с ростом давления. Это обстоятельство отражается на диаграмме. Кривая плавления ОС на диаграмме состояния воды идет вверх влево, тогда как почти для всех других веществ она идет вверх вправо.
Превращения, происходящие с водой при атмосферном давлении, отражаются на диаграмме точками или отрезками, расположенными на горизонтали, отвечающей 101,3 кПа (760 мм рт. ст.). Так, плавление льда или кристаллизация воды отвечает точке D, кипение воды — точке Е, нагревание или охлаждение воды — отрезку DE и т. п.
463 :: 464 :: 465 :: Содержание
465 :: 466 :: 467 :: 468 :: Содержание
